
广西壮族自治区贵百河—武鸣高中2024-2025学年高二上学期10月月考化学试卷(Word版附答案)
展开
这是一份广西壮族自治区贵百河—武鸣高中2024-2025学年高二上学期10月月考化学试卷(Word版附答案),共9页。试卷主要包含了本试卷分选择题和非选择题两部分等内容,欢迎下载使用。
(考试时间:75分钟 满分:100分)
注意事项:
1.本试卷分选择题和非选择题两部分。答卷前,考生务必将自己的姓名、学校、班级、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 P-31 S-32 Fe-56 Cu-64
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题意要求的。
1.化学与生产、生活密切相关,下列有关说法正确的是( )
A.工业合成氨温度为400~500是因为升高温度有利于提高反应物的平衡转化率
B.石油的裂化、裂解,煤的干馏、气化都属于化学变化
C.多糖、蛋白质、油脂属于有机高分子化合物
D.用作信息高速公路的石英光导纤维是一种新型的有机高分子材料
2.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.标准状况下,4.48LNO和3.2g O2充分反应,产物的分子数为0.2NA
B.1ml C2H6O含有的C-H键为5NA
C.1ml/L CH3COOH溶液中,CH3COOH分子的数目为NA
D.1ml Cu和等物质的量S共热充分反应后转移的电子数为NA
3.关于下列说法正确的是( )
A.若31g白磷的能量比31g红磷多b kJ,则白磷转化为红磷的热化学方程式为P4(白磷,s)===4P(红
磷,s) ΔH=-4b kJ/ml
B.若S(s)+O2(g) === SO2(g) ΔH1;2SO2(g)+O2(g)===2SO3(g) ΔH2,硫的燃烧热为
C.已知中和热∆H=-57.3 kJ/ml,则NaOH(aq)+CH3COOH(aq)===CH3COONa(aq)+H2O(l)
∆H<-57.3 kJ/ml
D.若NH3(g)+HCl(g) === NH4Cl(s)常温下能自发则该反应的∆H>0
4.下列离子方程式正确的是( )
A.硫化钠和硝酸混合:S2-+2H+ === H2S↑
B.氢氧化钡溶液与硫酸铜反应:Ba2++SO42- === BaSO4↓
C.石灰水与过量碳酸氢钠溶液反应:2HCO3-+ Ca2++2OH- === CaCO3↓+ 2H2O+CO32-
D.足量的铁与稀硝酸反应:Fe+NO3-+4H+ === Fe3++NO↑+2H2O
5.对于反应“CO+NO2CO2+ NO”,其速率方程为v=kc2(NO2),k为速率常数,只与温度有关,则下列说法正确的是( )
A.升高温度,v正增大,v逆减小
B.增大CO的浓度,化学反应速率不变
C.反应达到平衡后,缩小体积,平衡正向移动
D.该反应速率由反应物共同影响
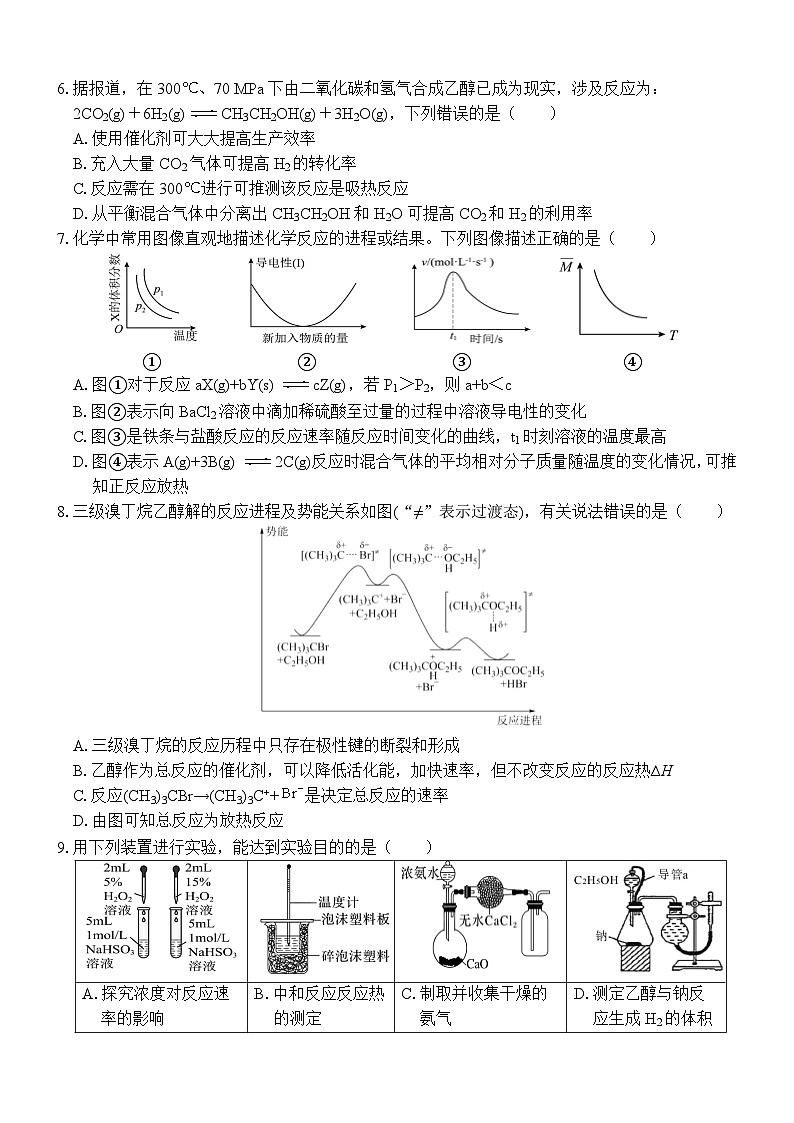
6.据报道,在300、70 MPa下由二氧化碳和氢气合成乙醇已成为现实,涉及反应为:
2CO2(g)+6H2(g)CH3CH2OH(g)+3H2O(g),下列错误的是( )
A.使用催化剂可大大提高生产效率
B.充入大量CO2气体可提高H2的转化率
C.反应需在300进行可推测该反应是吸热反应
D.从平衡混合气体中分离出CH3CH2OH和H2O可提高CO2和H2的利用率
7.化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )
① ② ③ ④
A.图①对于反应aX(g)+bY(s)cZ(g),若P1>P2,则a+b<c
B.图②表示向BaCl2溶液中滴加稀硫酸至过量的过程中溶液导电性的变化
C.图③是铁条与盐酸反应的反应速率随反应时间变化的曲线,t1时刻溶液的温度最高
D.图④表示A(g)+3B(g)2C(g)反应时混合气体的平均相对分子质量随温度的变化情况,可推
知正反应放热
8.三级溴丁烷乙醇解的反应进程及势能关系如图(“≠”表示过渡态),有关说法错误的是( )
A.三级溴丁烷的反应历程中只存在极性键的断裂和形成
B.乙醇作为总反应的催化剂,可以降低活化能,加快速率,但不改变反应的反应热∆H
C.反应(CH3)3CBr→(CH3)3C++是决定总反应的速率
D.由图可知总反应为放热反应
9.用下列装置进行实验,能达到实验目的的是( )
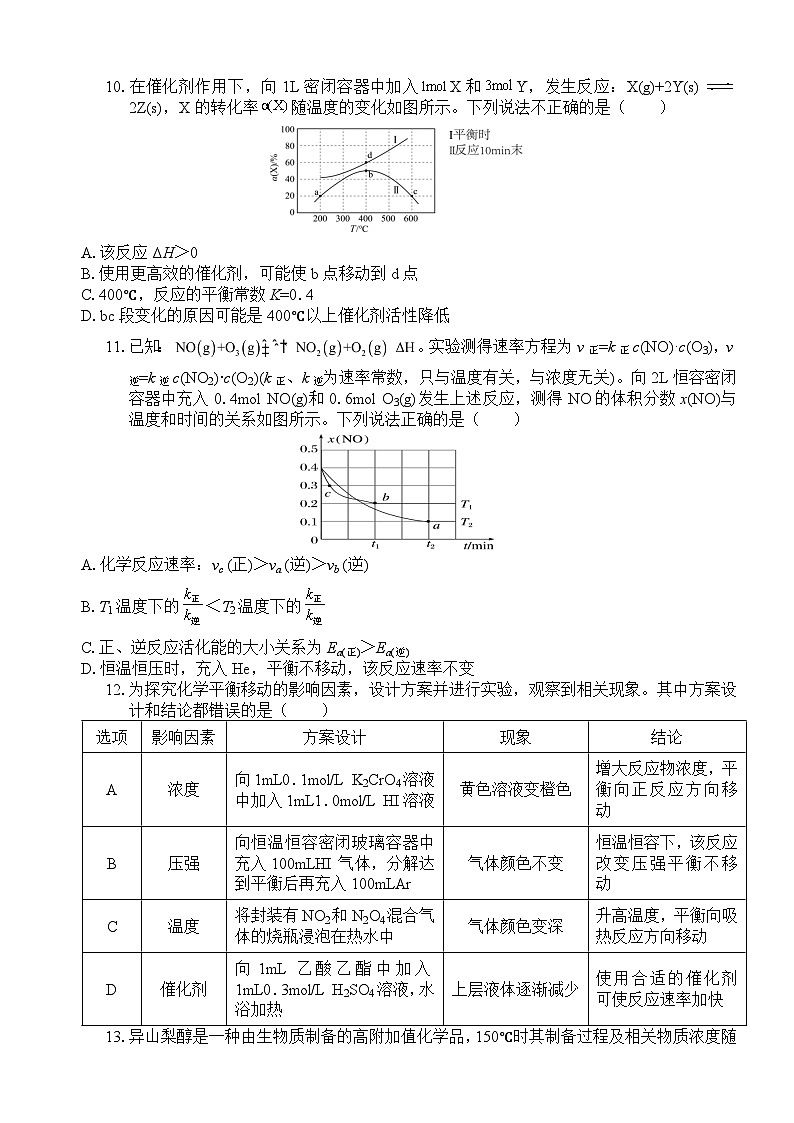
10.在催化剂作用下,向1L密闭容器中加入X和Y,发生反应:X(g)+2Y(s)2Z(s),X的转化率随温度的变化如图所示。下列说法不正确的是( )
A.该反应ΔH>0
B.使用更高效的催化剂,可能使b点移动到d点
C.400℃,反应的平衡常数K=0.4
D.bc段变化的原因可能是400℃以上催化剂活性降低
11.已知:。实验测得速率方程为v正=k正c(NO)·c(O3),v逆=k逆c(NO2)·c(O2)(k正、k逆为速率常数,只与温度有关,与浓度无关)。向2L恒容密闭容器中充入0.4ml NO(g)和0.6ml O3(g)发生上述反应,测得NO的体积分数x(NO)与温度和时间的关系如图所示。下列说法正确的是( )
A.化学反应速率:vc (正)>va (逆)>vb (逆)
B.T1温度下的<T2温度下的
C.正、逆反应活化能的大小关系为Ea(正)>Ea(逆)
D.恒温恒压时,充入He,平衡不移动,该反应速率不变
12.为探究化学平衡移动的影响因素,设计方案并进行实验,观察到相关现象。其中方案设计和结论都错误的是( )
13.异山梨醇是一种由生物质制备的高附加值化学品,150℃时其制备过程及相关物质浓度随时间变化如图所示,15h后异山梨醇浓度不再变化。下列说法正确的是( )
A.3h时,反应②正、逆反应速率相等
B.0~3h平均速率(1,4-失水山梨醇)=0.014ml∙Kg-1∙h-1
C.该温度下的平衡常数:①>②
D.反应②加入催化剂增大其平衡转化率
14.部分弱电解质的电离常数如下表,下列说法正确的是( )
A.HSO3-和HCO3-在水溶液中不能大量共存
B.NaClO溶液中通入少量CO2:2ClO- +CO2+H2O === 2HClO+CO
C.向氯水中分别加入等浓度的NaHCO3和NaHSO3溶液,均可提高氯水中HClO的浓度
D.25℃,反应HCOOH+ClO- === HClO+HCOO- 的平衡常数约为6.1×103
二、非选择题:共4题,共计58分。
15.(14分)回答下面的问题。
(1)下列反应中能量变化与图一致的是_______(填字母)。(2分)
A.铝热反应
B.灼热的木炭与二氧化碳反应
C.生石灰与水反应
D.氢氧化钡晶体和氯化铵晶体反应
(2)在无氧环境下,CH4经催化脱氢芳构化可以直接转化为高附加值的芳烃产品。一定温度下,CH4芳构化时同时存在如下反应:
i.CH4(g)→C(s)+2H2(g) ∆H1=+74.6kJ∙ml-1 ∆S=+80.84J∙ml-1∙K-1
ii.6CH4(g)→C6H6(l)+9H2(g) ∆H2
回答下列问题:
①反应ⅰ在1000K时_______(选填“能”或“不能”)自发进行。(2分)
②已知25℃时有关物质的燃烧热数据如表,则反应ⅱ的∆H2= kJ∙ml-1(用含a、
b、c的代数式表示)。(2分)
(3)一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,回答下列问题:
①a、b、c三点溶液的pH的大小: 。(2分)
②用湿润的pH试纸测量a处溶液的pH,测量结果 (填
“偏大”、“偏小”或“不变”)。(2分)
③用蒸馏水稀释c处的溶液,则下列各式表示的数值随水量的增
加而减小的是___________。(2分)
A.B.电离度α(CH3COOH)
C.n(H+) D.
(4)相同条件下,将pH=3的硫酸溶液和醋酸溶液,分别稀释成pH=5,加水后的体积:前者
后者(填“>”、“<”或“=”)。(2分)
16.(15分)工业上用软锰矿(主要成分是MnO2,含有Al2O3、SiO2等杂质),制备KMnO4的流程如下:
已知:①K2MnO4固体和溶液均为墨绿色;酸性环境下能发生歧化反应。
(1)K2MnO4中Mn的化合价是 。(1分)
(2)为了提高煅烧速率,可采取的措施有 。(答2点即可)
(2分)
(3)熔融煅烧时将空气改用KClO也能达到目的,写出KClO与软锰矿反应的主要化学方程式: 。(2分)
(4)向浸取后的溶液中通入CO2,调节其pH,经过滤得滤渣Ⅰ,滤渣Ⅰ的成分是 。
(2分)整个流程中可以循环利用的物质是 。(2分)
(5)写出歧化一步发生的离子反应方程式: 。(2分)
(6)“歧化”时,下列物质能代替冰醋酸的是: (填序号)。(2分)
①浓盐酸 ②H2SO3 ③稀硫酸 ④HI
(7)“操作Ⅱ”可通过 、 ,过滤、洗涤、干燥等一系列操作获得KMnO4晶体。(每空1分)
17.(14分)硫代硫酸钠(Na2S2O3)俗称大苏打或海波,在碱性条件下稳定,遇酸易分解。将SO2通入按一定比例配成的Na2S和Na2CO3的混合溶液中,便可得到Na2S2O3,同时生成CO2。
Ⅰ.制备Na2S2O3·5H2O
(1)仪器A的名称为 (1分),装置D的作用是 (1分),B中的试剂最好选用 (填字母)。(2分)
A.稀H2SO4 B.NaOH溶液 C.饱和NaHSO3溶液 D.饱和NaHCO3溶液
(2)C中将Na2S和Na2CO3配成溶液再通入SO2,便可制得Na2S2O3和CO2,写出反应的离子方程式为 。(2分)
(3)为保证硫代硫酸钠的产量,实验中产生的SO2不能过量,原因是
(2分)
(4)反应终止后,C中的溶液经蒸发浓缩即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、
Na2SO4等杂质,检测产品中是否含有Na2SO4杂质的实验操作和现象:
。(2分)
Ⅱ.探究Na2S2O3的部分化学性质
Ⅲ.Na2S2O3的应用
已知:。
某同学探究与稀H2SO4反应的速率影响因素时,设计了如下系列实验:
(5) 。(2分)
(6)通过对比实验①和②,验证 对反应速率的影响,因此测定变浑浊的时间t1 t2(填“>、“<”或“=”)。(每空1分)
18.(15分)Ⅰ.工业上利用甲醇和水蒸气催化重整法可制备氢气。
(1)知:
反应1:CH3OH(g)CO(g)+2H2(g) ∆H1=+90.0 kJ∙ml-1 K1
反应2:CO(g)+H2O(g)CO2(g)+H2(g) ∆H2=-41.0 kJ∙ml-1 K2
则反应3:CH3OH(g)+H2O(g)CO2(g)+3H2(g) K= (用含K1、K2的代数式表示)。
(2分)
(2)以CuO—ZnO—Al2O3催化剂进行甲醇重整制氢时,固定其它条件不变,改变水、甲醇的物质的量比,甲醇平衡转化率及CO选择性的影响如图所示。
①当水、甲醇比大于0.8时,CO选择性下降的原因是 。
(2分)
②当水、甲醇比一定时,温度升高,CO选择性有所上升,可能原因是 。
(2分)
(3)在t℃下,在1L密闭容器中,当投入的CH3OH和H2O均为1ml时,甲醇平衡转化率为80%、CO选择性为60%。则c(CO)= ml∙L-1。(2分)
Ⅱ.用CO2和H2可以合成甲醇。其主要反应为
反应Ⅰ CO2(g)+3H2(g)CH3OH(g)+H2O(g)
反应Ⅱ CO2(g)+H2(g)CO(g)+H2O(g)
在恒容密闭容器内,充入1ml CO2和3ml H2,测得平衡时CO2转化率,CO和CH3OH
选择性随温度变化如图所示[选择性]。
(4)270℃时主要发生的反应是 (填“Ⅰ”或“Ⅱ”)。(2分)
(5)以下温度中,甲醇产率最高的是 。(2分)
A.210℃ B.230℃ C.250℃ D.270℃
(6)将1ml CO2和1ml H2充入某容积不变的绝热密闭容器中,发生反应Ⅱ。下列能判断反应Ⅱ达到平衡的是________(填字母)。(2分)
A.容器内气体的压强不变
B.容器内平衡常数不变
C.断开2个O-H键的同时形成2个C=O键
D.容器内气体的平均相对分子质量不变
(7)在不改变投料的情况下,既能加快反应速率,又能提高CH3OH产率的方法有
(填一种方法即可)。(1分)A.探究浓度对反应速
率的影响
B.中和反应反应热
的测定
C.制取并收集干燥的
氨气
D.测定乙醇与钠反
应生成H2的体积
选项
影响因素
方案设计
现象
结论
A
浓度
向1mL0.1ml/L K2CrO4溶液中加入1mL1.0ml/L HI溶液
黄色溶液变橙色
增大反应物浓度,平衡向正反应方向移动
B
压强
向恒温恒容密闭玻璃容器中充入100mLHI气体,分解达到平衡后再充入100mLAr
气体颜色不变
恒温恒容下,该反应改变压强平衡不移动
C
温度
将封装有NO2和N2O4混合气体的烧瓶浸泡在热水中
气体颜色变深
升高温度,平衡向吸热反应方向移动
D
催化剂
向1mL乙酸乙酯中加入1mL0.3ml/L H2SO4溶液,水浴加热
上层液体逐渐减少
使用合适的催化剂可使反应速率加快
弱电解质
HClO
HCOOH
H2SO3
H2CO3
电离常数(25℃)
K=2.95×10-8
Ka=1.8×10-4
K1=1.54×10-2
K2=1.02×10-7
Ka1=4.3×10-7
Ka2=5.6×10-11
物质
CH4(g)
C6H6(l)
H2(g)
∆H/(kJ‧ml-1)
a
b
c
编号
0.1ml/L Na2S2O3溶液的体积/
0.1ml/LH2SO4溶液的体积/
水的体积/
水浴温度/℃
测定变浑浊时间/s
①
10.0
15.0
0
35
t1
②
10.0
10.0
V1
35
t2
③
15.0
0
45
t3
2023级“贵百河—武鸣高中”10月高二年级新高考月考测试
化学参考答案
一、选择题(每题3分,共42分)
二、非选择题:共4小题,共58分(除特别说明外每空2分)
15.(14分)
(1)BD(写对一个得1分,错选或多选不给分)
(2)①能
②6a-b-9c
(3)①c>a>b
②偏小
③AD(写对一个得1分,错选或多选不给分)
(4)<
16.(15分)
(1)+6(1分)
(2)软锰矿粉碎、搅拌等
(3)MnO2+KClO+2KOHK2MnO4+KCl+H2O(条件或者配平不对扣1分,只写对反应物和生成物得1分)
(4)H2SiO3、Al(OH)3(写对一个得1分) MnO2
(5)3MnO42-+4CH3COOH=== 2MnO4-+MnO2+2H2O +4CH3COO-(配平不对扣1分,只写对反应物和生成物得1分)
(6)③
(7)蒸发浓缩(1分) 冷却结晶(1分,写“结晶”而已不给分)
17.(14分)
(1)圆底烧瓶(1分) 安全瓶,防倒吸(1分) C
(2)CO32-+2S2-+4SO2=== 3S2O32-+CO2
(3)若SO2过量,溶液显酸性,产物Na2S2O3遇酸易分解,导致产率下降
(4)取少量产品溶于足量稀盐酸,静置,取上层清液,再滴加BaCl2溶液,若出现沉淀,则说明含有Na2SO4杂质 (合理即给分)
(5)1∶2
(6)H2SO4浓度(或浓度)(1分) < (1分)
18.(15分)
(1)K1K2
(2)①加水的用量(或增大水、甲醇比),促进反应2或反应3正向进行,CO2选择性上升,CO选择性下降。
②反应1为吸热反应,升高温度,反应1正向移动,n(CO)增大,反应2为放热反应,升高温度,反应2逆向进
行,n(CO)增大,导致CO选择性上升。
(3)0.48
(4)I
(5)C
(6)AB
(7)加压(或缩小容器体积)(1分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
B
D
A
C
B
C
D
B
D
C
B
A
C
D
相关试卷
这是一份[化学]广西“贵百河—武鸣高中”2024~2025学年高二上学期10月新高考月考试题(有答案),共9页。
这是一份广西“贵百河—武鸣高中”2024-2025学年高二上学期10月新高考月考化学试题,文件包含化学2023级“贵百河武鸣高中”10月高二月考docx、化学2023级“贵百河武鸣高中”10月高二月考参考答案docx等2份试卷配套教学资源,其中试卷共9页, 欢迎下载使用。
这是一份广西“贵百河—武鸣高中”2024-2025学年高二上学期10月新高考月考 化学试题,文件包含试卷2023级“贵百河武鸣高中”10月高二年级新高考月考测试pdf、答案2023级“贵百河武鸣高中”10月高二月考参考答案pdf等2份试卷配套教学资源,其中试卷共9页, 欢迎下载使用。










