

山西省2024届高三上学期教学质量检测化学试题(原卷版)
展开考生注意:
1.答题前,考生务必将自己的姓名、考生号填写在试卷和答题卡上,并将考生号条形码粘贴在答题卡上的指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Al 27 Cl 35.5 Cr 52
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1. 化学技术可以改善环境、造福人类。下列说法正确的是
A 生活垃圾焚烧尾气经脱硫脱硝后排放,能达到零污染
B. 汽车尾气排放系统中安装催化转化器可减少污染
C. 大量使用一次性口罩、防护服等,体现绿色环保理念
D. 我国科学家成功实现二氧化碳人工合成淀粉,这降低了“光化学烟雾”的形成
2. 下列化学用语表示正确的是
A. 基态氧原子的价电子轨道表示式:
B. 分子的模型:
C. 的电子式:
D. 中子数为10的氧原子:
3. 柠檬酸铁铵[]可用作铁质强化剂,以铁、硫酸、柠檬酸、过氧化氢、氨水等为原料可制备柠檬酸铁铵。下列说法中错误的是
A. 第一电离能:
B. 过氧化氢分子中只存在键
C. 基态的核外电子中,两种自旋状态的电子数之比为
D. 中氮原子的轨道与氢原子的轨道重叠形成键
4. 汽车已经成为人类不可缺少的交通工具,但汽车尾气是大气主要污染源。某科研机构将汽车尾气中的和设计成如图所示的燃料电池,实现了和的无害转化。
下列说法正确的是
A. 石墨I为负极,发生还原反应
B. 电池工作时,向石墨II电极处移动
C. 石墨II电极反应式为
D. 石墨I生成时,外电路中通过电子
5. 咖啡的有效成分咖啡因的结构简式如图所示。
下列说法正确的是
A. 咖啡因属于芳香烃B. 咖啡因含酯基,能发生水解反应
C. 咖啡因分子中含3种不同环境的氢原子D. 咖啡因的分子式为
6. 某药物成分的结构如图所示,其中、、、为原子序数依次增大的短周期主族元素,且元素原子的最外层电子数等于、和元素原子的最外层电子数之和。下列说法正确的是
A. 简单离子半径:
B. 与形成化合物比与形成的化合物稳定
C. 与另外三种元素均能组成原子个数比为的化合物
D. 形成的单质一定属于共价晶体
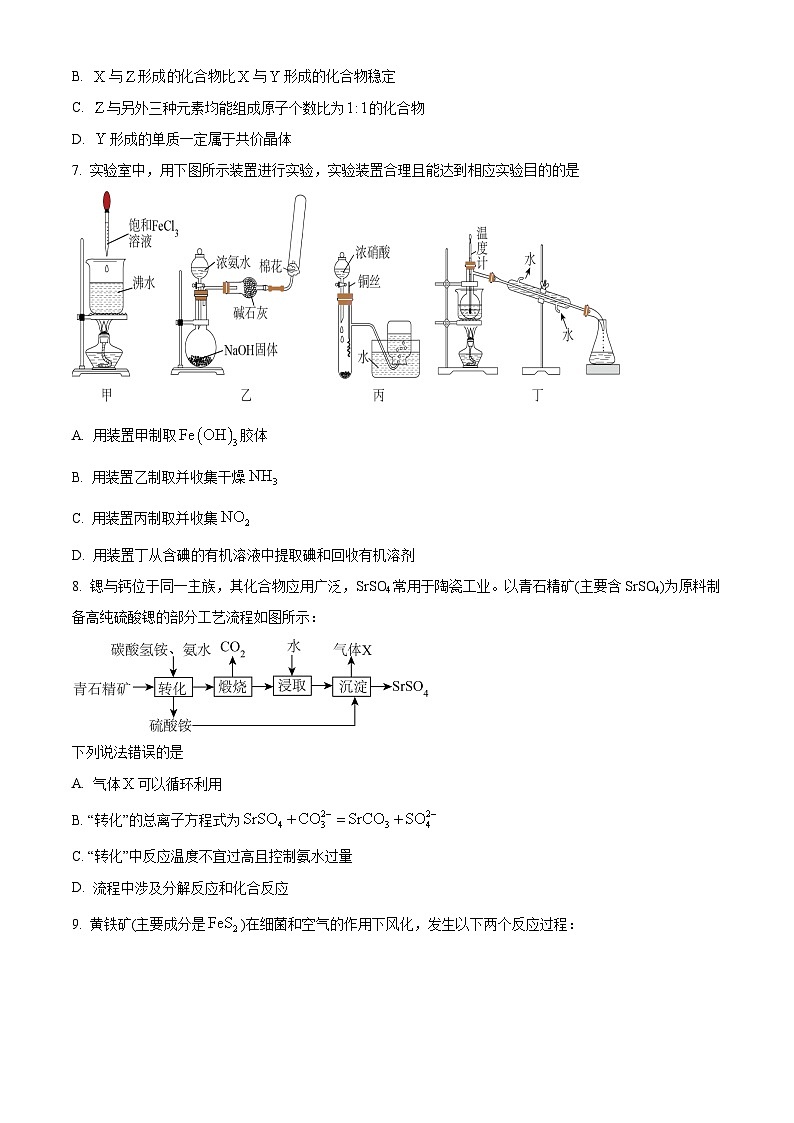
7. 实验室中,用下图所示装置进行实验,实验装置合理且能达到相应实验目的的是
A. 用装置甲制取胶体
B. 用装置乙制取并收集干燥
C. 用装置丙制取并收集
D. 用装置丁从含碘的有机溶液中提取碘和回收有机溶剂
8. 锶与钙位于同一主族,其化合物应用广泛,SrSO4常用于陶瓷工业。以青石精矿(主要含SrSO4)为原料制备高纯硫酸锶的部分工艺流程如图所示:
下列说法错误的是
A. 气体可以循环利用
B. “转化”的总离子方程式为
C. “转化”中反应温度不宜过高且控制氨水过量
D. 流程中涉及分解反应和化合反应
9. 黄铁矿(主要成分是)在细菌和空气的作用下风化,发生以下两个反应过程:
下列说法正确的是
A. 的模型与空间结构不一致
B. 反应I和Ⅱ中,元素和都被氧化
C. 反应Ⅱ中参加反应的
D. 反应I和Ⅱ中,氧化转移的电子数之比为
10. 已知25℃时,某些物质的燃烧热数据如表:
下列热化学方程式书写正确的是
A.
B.
C.
D.
11. 和在某催化剂表面合成甲醇的反应历程如图所示,其中“*”表示吸附在催化剂表面的物质,“”表示过渡态。
设为起始时的投料比,即。下列说法正确的是
A. 决速步骤的反应方程式为
B. 升高温度,该反应的正反应速率增大,逆反应速率减小
C. 该反应在高温下易自发进行
D. 若在同温同压下增大,则平衡体系中的体积分数一定增大
12. 已知氯化铝的熔点为、氟化铝的熔点为,氯化铝二聚体的空间填充模型如图1所示,氟化铝的晶胞结构(晶体密度为,阿伏加德罗常数为)如图2所示。下列说法正确的是
A. 图1中物质的分子式为B. 氟化铝中的配位数为6
C. 晶胞参数D. 氯化铝、氟化铝均为离子晶体
13. 工业上常用丙烷脱氢制备丙烯,反应为。在两个体积均为的恒容密闭容器中分别充入,测得的浓度()与温度、时间的关系如下表所示。
下列叙述正确的是
A. 上述丙烷脱氢反应的B. 升高温度,上述反应的平衡常数减小
C. 时,丙烷的平衡转化率为D. 时,平衡常数为4.0
14. 时,一水合二甲胺[]的,叠氮酸()的(为电离常数)。的溶液中,、、、随变化(加入盐酸或溶液)的关系如图所示。下列说法正确的是
A. 曲线代表随的变化
B. 原溶液中
C. 原溶液中
D. 图中点对应的溶液
二、非选择题:本题共5小题,共58分。
15. 某兴趣小组利用铁在氧气中燃烧的产物磁性氧化铁做如下实验:
(1)磁性氧化铁与铝在一定条件下发生反应时,氧化剂与还原剂的物质的量之比为___________。将磁性氧化铁完全溶于较浓的盐酸中,得到棕黄色的浓溶液,其反应的离子方程式为___________,取少量所得溶液加入双氧水,其反应的离子方程式为___________。
(2)取适量(1)中所得的棕黄色溶液于试管中,向其中加入稍过量的铁粉,发生主要反应的离子方程式为___________;静置后向上层清液中加入溶液,并放置一段时间,观察到的实验现象为___________。
(3)另取(1)中所得的棕黄色溶液于试管中,向其中通入足量的氯气,所发生反应的化学方程式为___________。若取少量所得溶液加入氢氧化钠溶液中则得到氢氧化铁沉淀,再进行下列反应制得绿色消毒剂高铁酸盐:(未配平),配平该方程式并用单线桥法标出其中电子转移的方向和数目:___________。
16. 以淀粉为原料合成F和J的简易流程如下:
回答下列问题:
(1)淀粉的分子式为___________。
(2)检验麦芽糖中含有醛基的常用试剂是___________(填名称)。
(3)葡萄糖在酶的催化下转变为乙醇的化学方程式为___________。
(4)E→F反应类型是___________。G中含有的官能团名称是___________。
(5)H→J的化学方程式为___________。
17. 铟()是一种主要用于生产低共熔合金、半导体和电光源等的原料。从铅、锌的冶炼过程中产生的高铟烟灰(主要含、、、、)中提取铟的流程如图所示:
已知:“氧化酸浸”后滤液中铟以的形式存在,与相似,易水解;二价金属离子不容易被萃取剂捕获。
回答下列问题:
(1)位于元素周期表的第5周期Ⅲ族,基态原子核外的价电子排布式为___________,的第三电离能___________(填“>”“<”或“=”)的第三电离能,元素位于元素周期表的___________区。
(2)“氧化酸浸”时加热的目的是___________,“氧化酸浸”过程中的硫元素被氧化为,该过程中参与反应的离子方程式为___________,滤渣1中除含过量的外,还有___________(填化学式)。
(3)“还原”过程中加入锌粉的目的是___________,上述流程图中可以循环利用的物质是___________。
(4)“萃取”过程中的有机萃取剂可用表示,使进入有机相,萃取过程发生的反应为,平衡常数为。“萃取”时萃取率的高低受溶液的影响很大,已知与萃取率()的关系符合公式:。当时,萃取率为,若将萃取率提升到,应调节溶液的___________(已知,忽略萃取剂浓度的变化,结果保留三位有效数字)。
18. 减少排放并实现的有效转化是科研的热点。以下几种为常见的利用方法,回答下列问题:
I.利用干重整反应不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。该反应一般认为通过如下步骤来实现:
i.
ii.[为吸附活性炭]
反应过程的能量变化如图所示:
(1)干重整反应的总热化学方程式为___________,其反应速率由反应ⅰ决定,则反应ⅱ的逆反应活化能应小于___________。
II.以氧化铟()作催化剂,可实现催化加氢制甲醇。
已知:①催化剂中时具有活性,而时无活性。
②与在活化的催化剂表面同时发生如下反应:
反应iii:主反应
反应iv:副反应
(2)工业上以原料气通过催化剂表面方法生产甲醇,是造成催化剂失活的重要原因,为了减少催化剂的失活,可以采用的方法是___________。
(3)反应iii、iv的平衡常数的随的变化曲线如图所示:
由图可知,代表反应iii的曲线是___________(填“”或“”),原因是___________;升高温度,反应iv的平衡常数___________(填“增大”“减小”或“不变”)。
(4)在恒温恒容密闭容器中,按物质的量比加入和,发生反应iii和反应iv,初始压强为。相同时间内的转化率、甲醇的产率在不同温度下的变化如图所示(不考虑温度对催化剂的影响):
①在以上,升高温度,甲醇的产率降低的原因是___________。
②时,反应已处于平衡状态,此时容器内压强为,则反应ⅳ的平衡常数___________(结果用分数表示)。
19. 三氯化铬是常用的媒染剂和催化剂,易潮解,高温下易被氧气氧化。实验室中用如图所示装置(夹持装置略)制取三氯化铬(、为气流控制开关)。
已知:①气体有毒,能被溶液吸收,。
②在碱性条件下具有较强还原性,能被等氧化剂氧化为。
③某些物质的颜色、状态、熔点、沸点如下表:
回答下列问题:
(1)制备的实验步骤如下:
i.连接装置,检查装置气密性,装入药品,打开、,通入并通入冷凝水。
ii.加热管式炉的反应管至。
iii.关闭(为打开状态),加热,温度保持在之间。
iv.加热反应管继续升温至,反应所生成的将升华并凝聚在反应管的右端,直到装置中反应完全,切断管式炉的电源。
v.停止加热装置,打开,关闭,继续通入直至装置中无液滴滴下,停止通入冷凝水。
vi.装置冷却后,结束制备实验。
①步骤i中,通的作用为________。步骤ⅲ中加热通常采用的加热方式是_________。
②步骤iv中装置中反应完全的标志是___________。
(2)装置中发生反应的化学方程式为___________。
(3)装置、的作用是___________。
(4)准确称取无水三氯化铬样品置于烧杯中,加水定容于容量瓶中。移取于碘量瓶中,加热至沸,慢慢加入(足量),待溶液变成黄色后,再加水至,充分加热煮沸,冷却后用溶液中和至呈橙红色,再加入足量溶液,加塞摇匀充分反应后,铬元素只以存在,暗处静置后,加入指示剂,用标准溶液滴定至终点,消耗标准溶液(已知杂质不参加反应,且)。
①向碘量瓶中加入后,发生反应的离子方程式为___________。
②该样品中无水三氯化铬的质量分数为___________(用含、、的代数式表示)。物质
燃烧热
-285.8
-393.5
-395.0
-3267.5
时间
温度
0
5
10
15
20
25
物质
颜色、状态
熔点
沸点/
绿色晶体
—
—
紫色晶体
—
—
无色液体
山西省怀仁市第一中学校2024-2025学年高三上学期摸底考试化学试题 (原卷版+解析版): 这是一份山西省怀仁市第一中学校2024-2025学年高三上学期摸底考试化学试题 (原卷版+解析版),文件包含山西省怀仁市第一中学校2024-2025学年高三上学期摸底考试化学试题原卷版docx、山西省怀仁市第一中学校2024-2025学年高三上学期摸底考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共34页, 欢迎下载使用。
2024届合肥市高三第三次教学质量检测 化学试题(原卷版+含解析): 这是一份2024届合肥市高三第三次教学质量检测 化学试题(原卷版+含解析),共8页。
山西省2024届高三上学期教学质量检测化学试题: 这是一份山西省2024届高三上学期教学质量检测化学试题,共20页。












