




高考化学一轮复习第5章非金属及其化合物第21讲硫酸硫及其化合物的相互转化课件
展开1.硫酸的物理性质(1)纯硫酸是一种无色油状液体,沸点高,难挥发。(2)溶解性:浓硫酸与水以任意比互溶,溶解时可放出大量的热。(3)浓硫酸的稀释方法: __________________________________________________________。
将浓硫酸沿器壁慢慢注入水中,并用玻璃棒不断搅拌
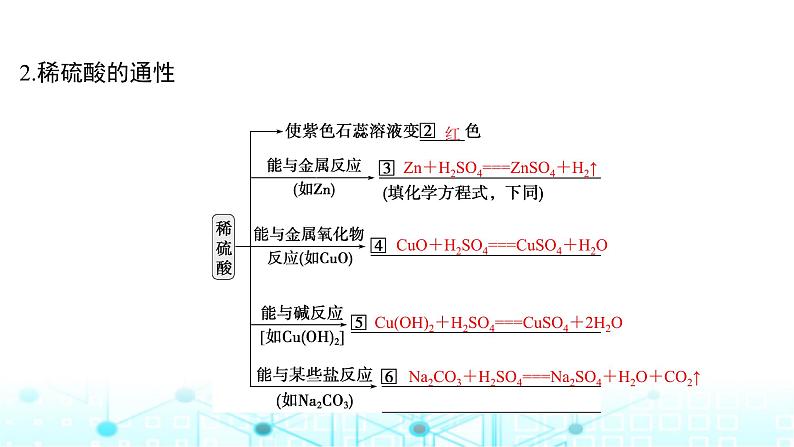
Zn+H2SO4===ZnSO4+H2↑
CuO+H2SO4===CuSO4+H2O
Cu(OH)2+H2SO4===CuSO4+2H2O
Na2CO3+H2SO4===Na2SO4+H2O+CO2↑
答案:(1)× (2)× (3)× (4)× (5)× (6)×
答案:(1)吸水性 (2)强氧化性 (3)强酸性 (4)脱水性
3.用如图所示的装置进行下列实验,将①中溶液滴入②中,预测②中的现象与实验结论相符的是( )
解析:将浓硫酸滴入浓盐酸中,浓硫酸稀释放出大量的热,促进了氯化氢的挥发,A项错误;浓硫酸与铜反应需在加热条件下进行,B项错误;浓硫酸使胆矾失去结晶水,体现的是浓硫酸的吸水性,该过程中有新物质生成,为化学变化,C项错误。
4.现有一瓶Na2SO3溶液,可能部分被氧化,某同学进行如下实验:取少量该溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,白色沉淀不溶解。对此实验的下列叙述正确的是( )A.此次实验确定Na2SO3已部分被氧化B.实验中加入Ba(NO3)2溶液后得到的白色沉淀一定是BaSO4C.实验中加入足量稀硝酸后得到的白色沉淀是BaSO4和BaSO3的混合物D.此次实验不能确定Na2SO3是否部分被氧化
解析:若Na2SO3部分被氧化变质,则滴入Ba(NO3)2溶液,生成的白色沉淀中一定有亚硫酸钡和硫酸钡,加入足量稀硝酸后,亚硫酸钡被氧化成硫酸钡,即此时的白色沉淀是硫酸钡,所以此次实验不能确定Na2SO3是否部分被氧化。
考点二 硫及其化合物的相互转化 1.通过“价—类”二维图认识硫及其化合物的关系
2.以化合价为线索厘清硫及其化合物的转化规律(1)相同价态硫的转化是通过酸、碱反应实现的。
(2)不同价态硫的转化是通过氧化还原反应实现的。当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态,即台阶式升降,可用下图表示:
1.某小组同学设计实验实现几种价态硫元素的转化。可选用的实验药品如下:①Na2SO3溶液;②浓硫酸;③Na2S 溶液;④稀硫酸;⑤酸性KMnO4溶液;⑥品红溶液;⑦铜片。
(1)实验ⅰ选择的药品是①和________(填序号),证明实现转化的现象是__________________,该转化利用了Na2SO3的______________性。(2)实验ⅱ实现了________价S向________价S的转化。(3)实验ⅲ中发生反应的化学方程式是________________,证明实现转化的现象是______________________。
2.物质的类别和核心元素的化合价是研究物质性质的两个重要角度。下图是硫元素的“价—类”二维图。
根据图示回答下列问题:(1)X的化学式为________,将X与SO2混合,可生成淡黄色固体,该反应中氧化产物与还原产物的质量之比为________。(2)过量的Fe粉与一定量W的浓溶液混合加热反应,生成________(填化学式)气体。转化①可由S粉与热的W的浓溶液反应实现,反应的化学方程式为_________________________________。解析:X为硫元素的气态氢化物,且硫元素的化合价为-2价,故X的化学式为H2S。将H2S与SO2混合,可生成淡黄色固体硫,反应的化学方程式是2H2S+SO2===3S+2H2O,S既是氧化产物又是还原产物,且氧化产物与还原产物的物质的量之比为2∶1,故二者的质量之比也为2∶1。答案:H2S 2∶1
(2)过量的Fe粉与一定量W的浓溶液混合加热反应,生成________(填化学式)气体。转化①可由S粉与热的W的浓溶液反应实现,反应的化学方程式为________________________________________________________。解析:W是硫酸,过量的Fe粉与一定量浓硫酸混合加热反应,首先生成的气体是SO2,随着反应的进行,硫酸浓度变小,后期有H2生成。
(3)欲制备Na2S2O3,从氧化还原角度分析,下列合理的是________(填字母)。A.Na2S+S B.Na2SO3+SC.Na2SO3+Na2SO4 D.SO2+Na2SO3(4)工业制硫酸中,转化②是在________(填设备名称)进行的。进行转化③时,不用水而用98.3%的浓硫酸吸收SO3,原因是___________________。(5)NaHSO4溶液显强酸性,向NaHSO4溶液中滴入Ba(OH)2溶液,恰好使溶液呈中性,发生反应的离子方程式为________________________。
1.(2022·高考全国乙卷)某白色粉末样品,可能含有Na2SO4、Na2SO3、Na2S2O3和Na2CO3。取少量样品进行如下实验:①溶于水,得到无色透明溶液;②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气味的气体逸出,离心分离;③取②的上层清液,向其中滴加BaCl2溶液有沉淀生成。该样品中确定存在的是( )A.Na2SO4、Na2S2O3 B.Na2SO3、Na2S2O3C.Na2SO4、Na2CO3 D.Na2SO3、Na2CO3
2.(2022·新高考湖北卷)硫代碳酸钠能用于处理废水中的重金属离子,可通过如下反应制备:2NaHS(s)+CS2(l)===Na2CS3(s)+H2S(g)。下列说法正确的是( )A.Na2CS3不能被氧化B.Na2CS3溶液显碱性C.该制备反应是熵减过程D.CS2的热稳定性比CO2的高
解析:A.Na2CS3中硫元素的化合价为-2价,还原性较强,能被氧化,故A错误;B.O与S同主族,类比Na2CO3溶液可得Na2CS3溶液显碱性,故B正确;C.由化学方程式可知,固体与液体反应生成气体,该制备反应是熵增过程,故C错误;D.S的原子半径比O的大,则C===S的键长比C===O的键长长、键能小,即CS2的热稳定性比CO2的低,故D错误。
3.(2021·新高考辽宁卷)含S元素的某钠盐a能发生如下转化。下列说法错误的是( ) A.a可能为正盐,也可能为酸式盐B.c为不溶于盐酸的白色沉淀C.d为含极性键的非极性分子D.反应②中还可能生成黄色沉淀
B.c为BaSO4,故c为不溶于盐酸的白色沉淀,B正确;C.d为SO2,由SO2易溶于水并根据“相似相溶”规律可知,d是含有极性键的极性分子,C错误;D.盐a为Na2SO3、NaHSO3或Na2S2O3等,当发生反应Na2S2O3+2HCl===2NaCl+S↓+SO2↑+H2O时,反应②中可能生成黄色沉淀,D正确。
4.(2023·浙江6月选考)工业上煅烧含硫矿物产生的SO2可以按如下流程脱除或利用。
请回答:(1)富氧煅烧燃煤产生的低浓度的SO2可以在炉内添加CaCO3通过途径Ⅰ脱除,写出反应的化学方程式:_________________________。
(2)煅烧含硫量高的矿物得到高浓度的SO2,通过途径Ⅱ最终转化为化合物A。①下列说法正确的是________。A.燃煤中的有机硫主要呈正价B.化合物A具有酸性C.化合物A是一种无机酸酯D.工业上途径Ⅱ产生的SO3也可用浓硫酸吸收②一定压强下,化合物A的沸点低于硫酸的原因是____________。答案:①BCD ②硫酸分子能形成更多的分子间氢键
2025届高考化学一轮复习 第四章 非金属及其化合物 第4讲 硫酸 含硫物质的转化 课件: 这是一份2025届高考化学一轮复习 第四章 非金属及其化合物 第4讲 硫酸 含硫物质的转化 课件,共1页。
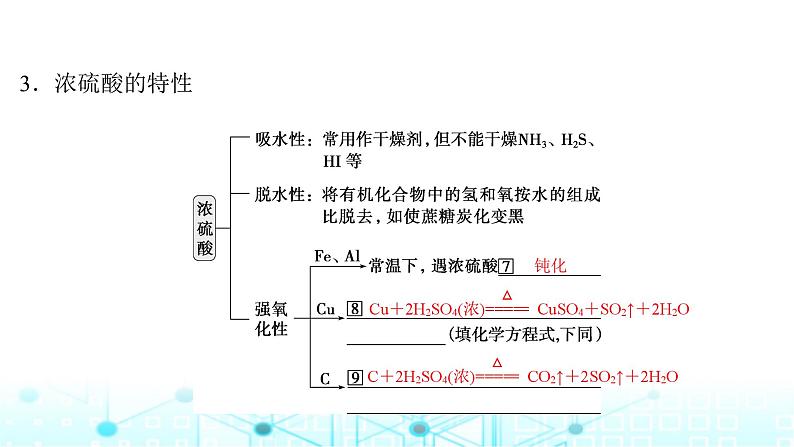
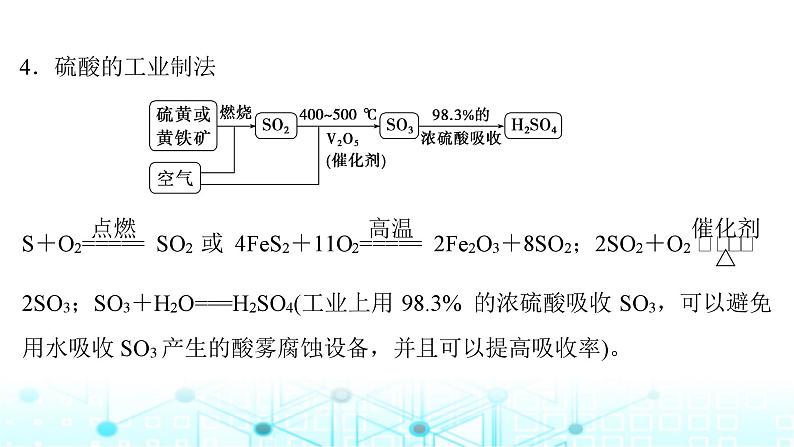
2025届高考化学一轮总复习第5章非金属及其化合物第21讲硫酸硫及其化合物的相互转化课件: 这是一份2025届高考化学一轮总复习第5章非金属及其化合物第21讲硫酸硫及其化合物的相互转化课件,共36页。PPT课件主要包含了稀硫酸的通性,浓硫酸的特性,硫酸的工业制法等内容,欢迎下载使用。
备战2025届新高考化学一轮总复习第4章非金属及其化合物第18讲硫酸含硫物质之间的转化课件: 这是一份备战2025届新高考化学一轮总复习第4章非金属及其化合物第18讲硫酸含硫物质之间的转化课件,共44页。PPT课件主要包含了课标指引,目录索引,素养发展进阶,必备知识•梳理,浓硫酸,玻璃棒,pH试纸变黑,BaCl2,关键能力•提升等内容,欢迎下载使用。












