



第15讲 核外电子排布、离子的形成-暑期初二升初三化学衔接自学课讲义(人教版)
展开1、帮助孩子系统梳理上学期所学知识。带领孩子构建完备、扎实牢固的知识体系;
2、帮助孩子预习新学期功课。提前掌握重难点、考点、易错点,领先一步提高学习效率;
3、假期持续稳定的学习。避免孩子长时间沉迷于电视、手机,养成坏习惯,影响新学期学习。
第15讲 原子结构、相对原子质量
【学习目标】
1.知道原子核外电子是分层排布的
2.了解原子结构示意图的含义;了解原子最外层电子数与原子种类及化学性质的关系
3.了解离子的形成过程,知道离子与原子的区别与联系。
【基础知识】
1.在多电子原子中,核外电子有不同的运动状态,能量高的电子离核远 ,能量低的电子离核 近核外电子的这种分层运动又叫做 分层排布 。
2.原子结构示意图的各部分的含义是什么?
3.核外电子排布的简单规律:
(1)第一电子层最多容纳 2 个电子,第二电子层最多容纳 8 个电子)
(2)最外层电子数不超过 8 个(只有一个电子层的,电子不超过 2 个)
(3)电子总是先排在能量低的电子层里,排满后,再排布在能量高的电子层里。
电子先排满第__1_层,再排第__2_层,排满第__2_层,再排第__3_层。(按照能量由低到高的顺序分层排布)
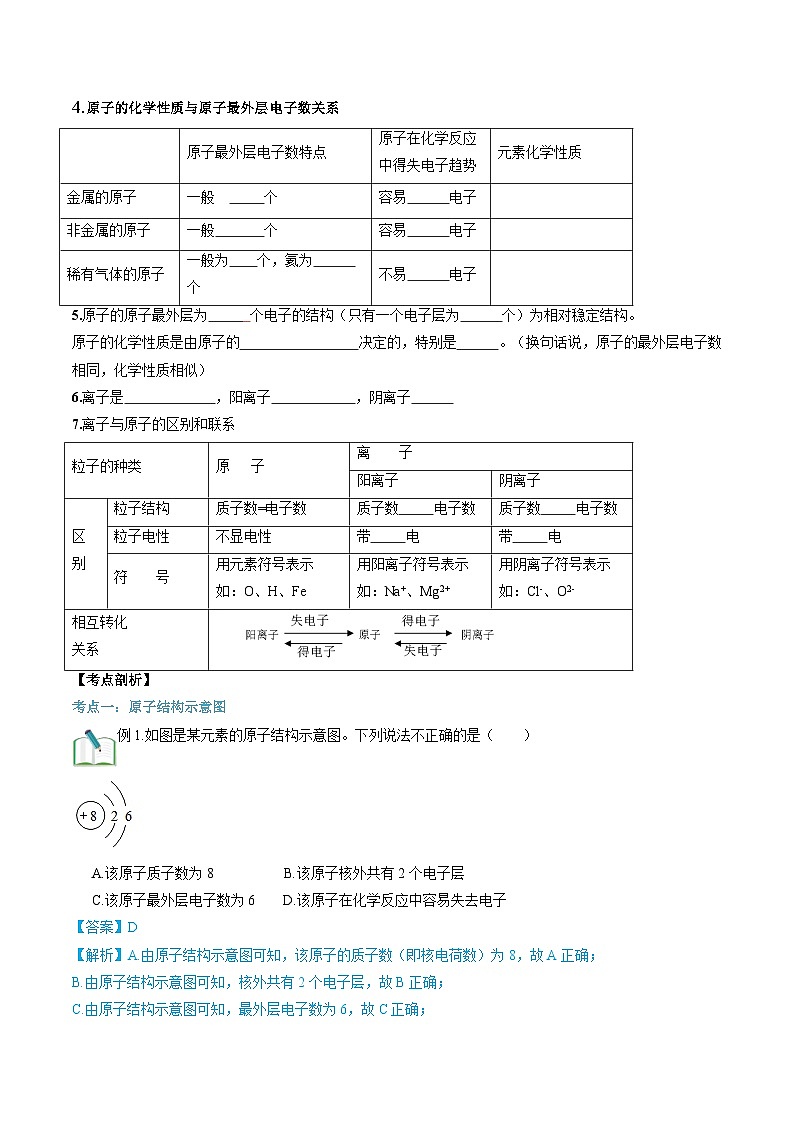
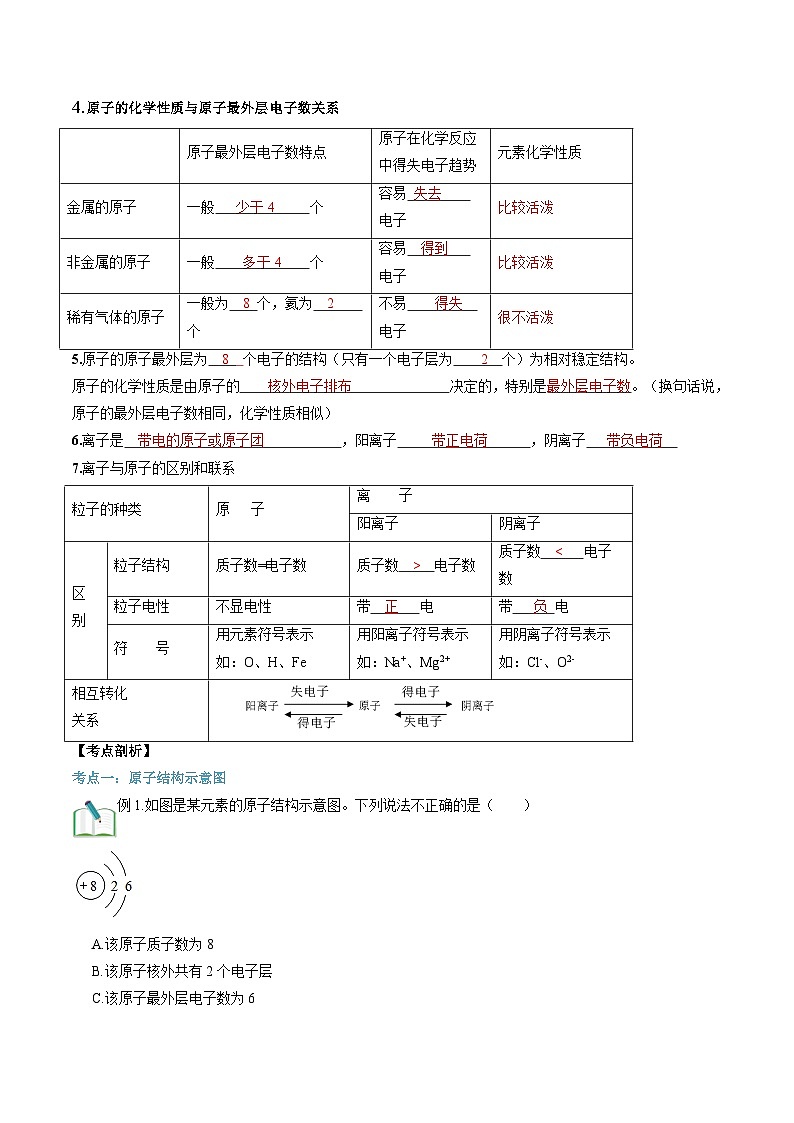
4.原子的化学性质与原子最外层电子数关系
5.原子的原子最外层为 个电子的结构(只有一个电子层为 个)为相对稳定结构。
原子的化学性质是由原子的 决定的,特别是 。(换句话说,原子的最外层电子数相同,化学性质相似)
6.离子是 ,阳离子 ,阴离子
7.离子与原子的区别和联系
【考点剖析】
考点一:原子结构示意图
例1.如图是某元素的原子结构示意图。下列说法不正确的是( )
A.该原子质子数为8 B.该原子核外共有2个电子层
C.该原子最外层电子数为6 D.该原子在化学反应中容易失去电子
【答案】D
【解析】A.由原子结构示意图可知,该原子的质子数(即核电荷数)为8,故A正确;
B.由原子结构示意图可知,核外共有2个电子层,故B正确;
C.由原子结构示意图可知,最外层电子数为6,故C正确;
D.该原子的最外层电子数>4,在化学反应中容易得到电子达到稳定结构,故D不正确。故选D。
考点二:核外电子排布
例2. 原子核外电子的排布规律
(1)电子在原子核外一定区域内出现,这些区域叫做“电子层”,核外电子是在不同的电子层内运动的,此现象叫做_______,按电子_______高低,分别排布在离核从近到远的电子层内,电子能量_____排在离核近的层里,电子的能量______排在离核远的层里,离核最远的电子层叫作_______。
(2)原子的第一层最多排_____电子,第二层最多排______电子,最外层电子数最多不超过8个电子,只有1层的不超过2个电子。
【答案】(1) 核外电子的分层排布 能量 低 高 最外层
(2) 2个 8个
【解析】(1)核外电子经常出现的区域称电子层,核外电子在不同的电子层内运动的现象,叫做核外电子的分层排布,按电子能量高低,分别排布在离核从近到远的电子层内,能量低的电子在离核较近的区域运动,能量高的电子在离核 较远的区域运动,离核最远的电子层叫作最外层。
(2)由核外电子排布的规律可知,第一层上最多2个电子,第二层上最多8个电子,最外层最多不超过8个电子,只有1层时不超过2个电子。
考点三:离子的形成
例3.图1是锂原子结构示意图。锂在化学反应中容易___(填“得”或“失”)电子,带 电荷,叫做 ;钠原子结构示意图如图2所示,x=___;研究表明,电池充电快慢与构成该电池的金属离子半径成正比,电池容量相同的Li、Na、K三种电池(Li、Na、K离子半径如图3所示),充电最快的是___电池。
【答案】 失 1个单位正 锂离子 11 钾/K
【详解】由锂原子结构示意图可知,锂原子的最外层电子数为1,小于4,在化学反应中容易失电子,带1个单位正电荷叫做锂离子;原子中质子数=核外电子数,则x=2+8+1=11;根据图示可知,离子半径锂离子<钠离子<钾离子,电池充电快慢与构成该电池的金属离子半径成正比,则钾电池充电速度最快,故填:失;11;钾或K。
【过关检测】
1.下列是几种粒子的结构示意图,其中属于阴离子的是( )
A. B. C. D.
2.如图是四种粒子的结构示意图,下列说法正确的是( )
A.①③④具有相对稳定结构
B.①表示的是阳离子
C.②在化学反应中易得到电子
D.③与氯离子核外电子排布相同
3.用原子结构示意图可简明、方便地表示原子的结构。如图是铝原子的结构示意图,下列说法不正确的是( )
A.铝原子核外有3个电子层
B.铝原子的核电荷数为13
C.铝原子的最外层电子数为3
D.铝原子易失去电子形成阴离子
4.下图为某粒子的结构示意图,有关该粒子的说法中,错误的是( )
A.该粒子的原子核内有19个质子
B.该粒子的核外有四个电子层
C.该粒子最外层上有一个电子
D.该粒子是带负电的阴离子
5.下列说法不正确的是( )
A.在多个电子的原子里,电子是分层排布的
B.具有稳定结构的粒子一定是稀有气体元素的原子
C.非金属元素的原子的最外电子层上电子一般多于4个
D.原子结构示意图可简明、方便地来表示原子的结构
6.某原子的结构示意图为:,下列说法正确的是( )
A.该原子的核外电子数为6 B.该原子核内中子数为8
C.该原子属于金属元素的原子 D.该元素的原子序数为8
7.下列有关粒子结构示意图的说法正确的是( )
A.①和④粒子易失去最外层电子达到相对稳定结构 B.①和③都表示原子
C.②和③属于同一周期元素的不同粒子 D.②和③化学性质相似
8.某粒子结构示意图如图所示,下列有关说法不正确的是( )
A.氯原子的质子数为17
B.氯原子第一层有2个电子
C.如图表示的是氯原子的结构示意图
D.一个氯原子得到一个电子后变成氯离子
9.我国在砷化镓太阳能电池研究方面国际领先。镓的原子结构示意图如下,下列说法正确的是( )
A.镓原子由31个质子和电子构成B.镓原子带31个单位的正电荷
C.原子核外的电子分5层排布D.镓原子在反应中趋于失去电子
10.如图中是四种粒子的结构示意图,请回答下列问题。
(1)A中数字“8”表示___________。
(2)以上四种粒子的结构示意图中,表示离子的是___________(填字母,下同)。
(3)容易得到1个电子的是___________。
(4)具有相对稳定结构的原子是___________。
(5)D中x=___________。
(6)属于同种元素的是___________。
11.“用微粒的眼光看世界”是我们学习化学的重要思想方法。请回答下列问题:
(1)如图1所示是某物质在三态变化时的分子示意图,物质处在C点为___________(填“固”、’“液”或“气”)态。
(2)如图2表示构成物质的粒子之间的关系。
①图中甲是__________。
②金属由原子直接构成。某种核原料铀-235,已知其原子核内含有92个质子和143个中子,则该原子核外有__________个电子。
(3)某同学利用碘进行了如下实验:
①把少量的固体碘放在湿润的馒头上,发现馒头会变蓝色;
②再取少量的碘溶解在水中,用馒头去蘸取碘液发现馒头也会变蓝色。
现取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,这时把湿润的馒头放在碘蒸气中,预测现象___________。原子最外层电子数特点
原子在化学反应中得失电子趋势
元素化学性质
金属的原子
一般 个
容易 电子
非金属的原子
一般 个
容易 电子
稀有气体的原子
一般为 个,氦为 个
不易 电子
粒子的种类
原 子
离 子
阳离子
阴离子
区
别
粒子结构
质子数=电子数
质子数 电子数
质子数 电子数
粒子电性
不显电性
带 电
带 电
符 号
用元素符号表示
如:O、H、Fe
用阳离子符号表示
如:Na+、Mg2+
用阴离子符号表示
如:Cl-、O2-
相互转化
关系
第13讲 分子和原子-暑期初二升初三化学衔接自学课讲义(人教版): 这是一份第13讲 分子和原子-暑期初二升初三化学衔接自学课讲义(人教版),文件包含第13讲分子和原子原卷版docx、第13讲分子和原子解析版docx等2份学案配套教学资源,其中学案共20页, 欢迎下载使用。
第10讲 氧气-暑期初二升初三化学衔接自学课讲义(人教版): 这是一份第10讲 氧气-暑期初二升初三化学衔接自学课讲义(人教版),文件包含第10讲氧气原卷版docx、第10讲氧气解析版docx等2份学案配套教学资源,其中学案共20页, 欢迎下载使用。
第08讲 空气的组成-暑期初二升初三化学衔接自学课讲义(人教版): 这是一份第08讲 空气的组成-暑期初二升初三化学衔接自学课讲义(人教版),文件包含第08讲空气的组成原卷版docx、第08讲空气的组成解析版docx等2份学案配套教学资源,其中学案共20页, 欢迎下载使用。












