
北京市第一○一中学2023-2024学年高三下学期三模化学+试题
展开 这是一份北京市第一○一中学2023-2024学年高三下学期三模化学+试题,共14页。试卷主要包含了05,下列化学用语或图示表达正确的是,下列对物质性质解释合理的是,某小组利用下图装置探究的性质等内容,欢迎下载使用。
2024.05
友情提示
本试卷分为I卷、II卷两部分,共19个小题,共10页,满分100分;答题时间为90分钟;请将答案写在答题纸上,交答题纸。
可能用到的相对原子质量:H 1 C 12 O 16 F 19 Mg 24 K 39 Mn 55 Fe 56
I卷 选择题(共42分)
每小题只有一个选项符合题意。
1.“齐天圣鼓”又称“猴鼓”,相传起源于唐朝,堪称中原一绝,是中国非物质文化遗产之一。猴鼓的结构如下图所示。下列说法不正确的是( )
A.牛皮面的主要成分是蛋白质,耐高温
B.竹钉的组成成分纤维素属于天然高分子
C.桐油是从桐籽中提炼出来的油脂,属于酯类
D.铜质鼓环不宜采用铁质铆钉固定
2.下列化学用语或图示表达正确的是( )
A.乙烯分子中的键:B.次氯酸的电子式:
C.的VSEPR模型:D.基态原子的价电子排布式:
3.中国化学遴选了118名青年化学家作为“元素代言人”组成“中国青年化学家元素周期表”。元素(钋)与S同主族,由暨南大学陈填烽代言,其原子序数为84。下列说法正确的是( )
A.位于元素周期表的第4周期B.原子半径:
C.的中子数为126D.只有还原性
4.下列解释事实的离子方程式不正确的是( )
A.向氢氧化镁悬浊液中滴加氯化铵溶液,沉淀溶解:
B.电解饱和食盐水,两极(碳棒)均产生气体:
C.向酸性的淀粉-碘化钾溶液中滴加适量双氧水,溶液变蓝:
D.向氢氧化钡溶液中滴加稀硫酸,一段时间后混合溶液的导电能力接近于0:
5.下列对物质性质解释合理的是( )
6.甲醛水溶液久置会发生聚合,生成低聚甲醛,反应如下(均为放热反应):
;
下列说法正确的是( )
A.低聚甲醛为直线型分子
B.低聚甲醛的生成可能导致甲醛溶液出现浑浊
C.加热久置的甲醛溶液不可能使甲醛再生
D.向久置的甲醛溶液中加入酸性溶液,若褪色证明甲醛有剩余
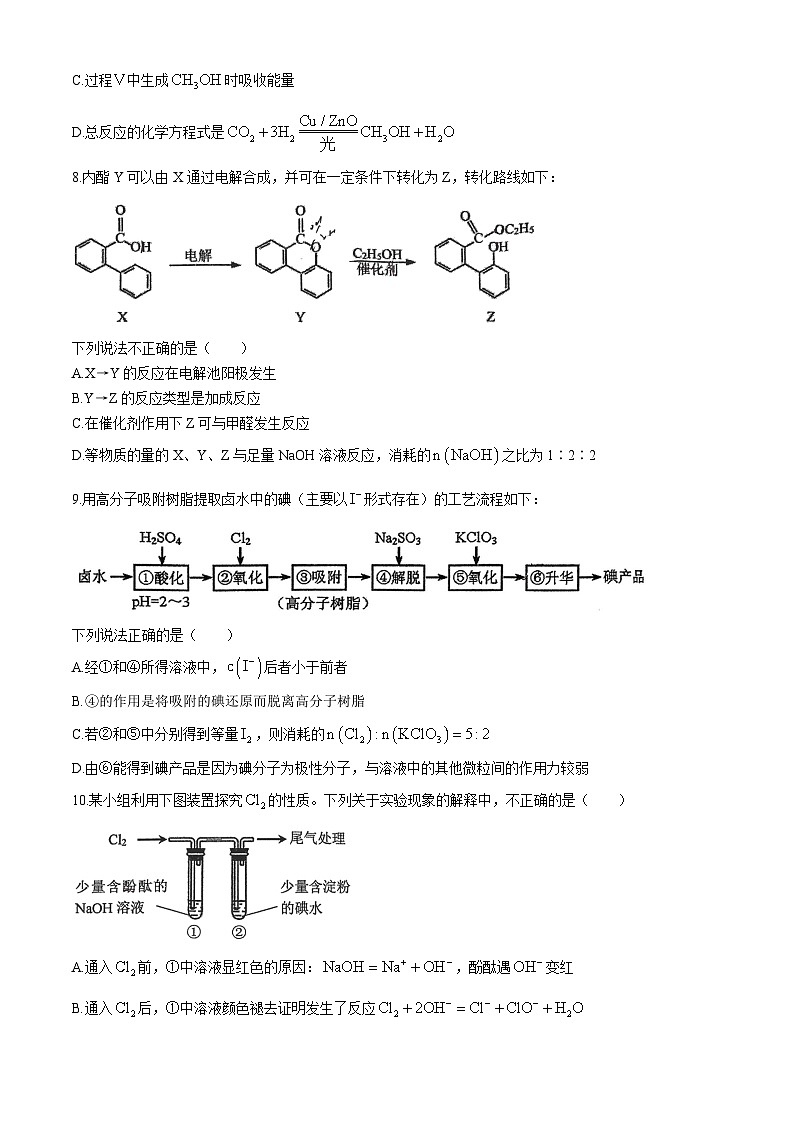
7.科研人员利用作催化剂,在光照条件下实现了和合成,该反应历程示意图如下。
下列说法不正确的是( )
A.过程Ⅰ中表面上进行的吸附与转化
B.过程Ⅱ中存在极性键的断裂与形成
C.过程Ⅴ中生成时吸收能量
D.总反应的化学方程式是
8.内酯Y可以由X通过电解合成,并可在一定条件下转化为Z,转化路线如下:
下列说法不正确的是( )
A.X→Y的反应在电解池阳极发生
B.Y→Z的反应类型是加成反应
C.在催化剂作用下Z可与甲醛发生反应
D.等物质的量的X、Y、Z与足量NaOH溶液反应,消耗的之比为1∶2∶2
9.用高分子吸附树脂提取卤水中的碘(主要以形式存在)的工艺流程如下:
下列说法正确的是( )
A.经①和④所得溶液中,后者小于前者
B.④的作用是将吸附的碘还原而脱离高分子树脂
C.若②和⑤中分别得到等量,则消耗的
D.由⑥能得到碘产品是因为碘分子为极性分子,与溶液中的其他微粒间的作用力较弱
10.某小组利用下图装置探究的性质。下列关于实验现象的解释中,不正确的是( )
A.通入前,①中溶液显红色的原因:,酚酞遇变红
B.通入后,①中溶液颜色褪去证明发生了反应
C.通入前,②中溶液显蓝色的原因:淀粉遇碘单质变蓝
D.通入后,②中溶液颜色褪去的原因可能是:
11.利用如图装置(夹持装置略)进行实验,X、Y中所选试剂不能达到实验目的的是( )
12.一种新型水介质电池,为解决环境和能源问题提供了一种新途径,其工作示意图如下。下列说法不正确的是( )
A.放电时,金属锌为负极
B.放电时,被转化为储氢物质
C.充电时,电池总反应为:
D.充电时,双极隔膜产生的向右室移动
13.“丁烯裂解法”是一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。发生的反应为:主反应:;副反应:。测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)变化的趋势如图所示,下列说法正确的是( )
A.300℃~400℃范围内,温度升高,压强减小,丙烯的平衡产率提高
B.主副反应的正反应方向均为吸热过程
C.450℃时,主反应的催化剂活性最好
D.将乙烯分离出去有助于增大丙烯的平衡产率
14.小组同学查阅资料发现,与可发生反应,生成无色的配合物。于是设计以下实验进行了证实。
下列说法正确的是( )
A.实验a与实验b中的的作用相同
B.实验a与实验b中的的溶解度相同
C.实验c与实验d做对比可进一步证实资料内容
D.实验c的试管中存在平衡移动,而实验d试管中没有
Ⅱ卷 非选择题(共58分)
15.(10分)氟化镁钾()是一种具有优良光学性能的材料,其晶胞结构如下。以该晶胞结构为基础,将相似离子取代或部分取代,可合成多种新型材料。
(1)晶体中,每个位于( )个距离最近的F构成的( )空隙中。填选项字母_____。
a.3 三角形b.4 正四面体c.6 正八面体d.8 立方体
(2)半径与接近,将部分由取代,可以带来电荷不平衡性和反应活性,从而合成新型催化剂材料。
①基态价电子的轨道表示式为__________。
②)某实验室合成新型催化剂材料(是平衡电荷引入的填隙阴离子,不破坏原有晶胞结构)。已知晶胞棱长为a。若要合成厚度为301、面积为1的催化剂材料,理论上需要掺杂的约为__________。
(,,设阿伏加德罗常数约为)
(3)我国科研工作者以晶体结构为框架,依据“体积匹配原则”合成了具有独特电学性能的晶体。其框架中的由取代,位置嵌入有机阳离子,位置沿棱方向嵌入直线型。已知与的结构简式如下:
①中心N原子的杂化方式为___________。
②的转动不会影响晶体骨架,这是因为除离子键外,该晶体中微粒间还存在着其他相互作用。如邻近的与之间还存在着___________,上述相互作用不会随的转动改变。
(4)与镁离子半径接近的锂离子在可充电电池中应用广泛,如、等可作为聚乙二醇锂离子电池的电极材料。电池放电时,沿聚乙二醇分子中的碳氧链向正极迁移的过程如图所示(图中阴离子未画出)。
①从原子结构的角度解释锂离子半径与镁离子半径接近的原因______________。
②从化学键角度看,迁移过程发生___________(填“物理”或“化学”)变化。
③相同条件下,电极材料中的迁移速率比中的快,原因是___________。
16.(11分)资源化利用是解决资源和能源短缺、减少碳排放的一种途径。
Ⅰ.制甲醇,过程如下:
ⅰ.催化剂活化:(无活性)(有活性)
ⅱ.与在活化后的催化剂表面可逆的发生反应①,其反应历程如图1。同时伴随反应②:
图1 图2
(1)反应①每生成1放热49.3,写出其热化学方程式:___________。
(2)与混合气体以不同的流速通过反应器,气体流速与转化率、选择性的关系如图2。
已知:选择性(生成所用的)(转化的)。
流速加快可减少产物中的积累,减少反应___________(用化学方程式表示)的发生,从而减少催化剂的失活,提高甲醇选择性。
(3)对于以上制甲醇的过程,以下描述正确的是___________(填序号)。
A.反应中经历了、键的形成和断裂
B.加压可以提高的平衡转化率
C.升高温度可以提高甲醇在平衡时的选择性
Ⅱ.一种以甲醇和二氧化碳为原料,利用()和纳米片()作催化电极,电化学法制备甲酸(甲酸盐)的工作原理如图所示。
(4)①阴极表面发生的电极反应式为___________。
②若有1通过质子交换膜,则理论上生成的和共___________。
(5)电解部分甲醇后,将阴阳极的电解液混合,加入过量氢氧化钠后蒸干溶液,再向所得固体中加入过量稀硫酸,溶解后得200溶液。取20溶液,加入溶液,充分反应后,再加入过量溶液和5滴淀粉溶液,用溶液滴定至终点,消耗溶液体积为。
已知:;。
①滴定终点的现象为___________。
②假设电流效率为100%,则电解池装置中通过的电子的物质的量为___________。
③若不加入氢氧化钠,直接蒸干溶液,则②中的计算结果将__________(填“偏高”、“偏低”或“不变”)。
17.(10分)某研究小组以甲苯为起始原料,按下列路线合成某利尿药物M。
已知:
(代表烃基或H原子)
(1)A为苯的同系物,A→B的化学方程式为__________。
(2)B→D的反应试剂及条件为__________。
(3)D→E的反应类型为__________。
(4)下列说法正确的是__________。
a. A的一氯代物共有3种
b J在一定条件下可以生成高分子化合物
c. K的核磁共振氢谱共有6个峰
(5)F→G,H→J两步反应的设计目的是__________。
(6)已知L→M的转化过程分两步,转化关系如下图所示。
L + N → P → M
请写出N和P的结构简式:__________、__________。
18.(12分)新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂()做电极材料。对废旧电极(含杂质、石墨粉)回收并获得高纯的工业流程图如下:
资料:碳酸锂在水中的溶解度:
(1)过程ⅰ研磨粉碎的目的是___________。
(2)过程ⅱ加入足量溶液的目的是除去,相关离子方程式为___________。
(3)过程ⅲ采用不同氧化剂分别进行实验,均采用含量为3.7%的原料,控制为3.5,浸取1.5h后,实验结果如下表所示:
①实验2中,能与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为___________。
②过程ⅱ最终选择作为氧化剂,原因是___________。
③过程ⅲ得到的浸出液循环两次的目的是___________。
(4)浸出液中存在大量和。结合平衡移动原理,解释过程ⅳ得到磷酸铁晶体的原因_______。
(5)对比过程ⅳ和ⅴ,说明过程ⅳ不用饱和溶液的原因:___________。
(6)过程ⅵ的操作为:将粗品加水溶解,蒸发结晶至有大量固体析出,___________。
19.(15分)化学小组实验探究与悬浊液的反应。
资料:ⅰ.(无色),易被氧气氧化为。
ⅱ.很不稳定,易转化为。
ⅲ.在酸性溶液中易转化为、。
实验一:Ⅰ.向溶液中加入浓溶液,制得悬浊液,测得。
Ⅱ.向悬浊液中通入产生大量白色沉淀A,测得。
(1)产生的离子方程式是______________________________。
(2)推测白色沉淀A中可能含有、、、、。为检验白色沉淀成分,进行实验二。
实验二:将实验一中所得的白色沉淀A过滤、洗涤,并进行如下实验。
①经检验白色沉淀A中无、,试剂a为______________。
②根据上述实验推测白色沉淀A为,推测依据是______________。
③产生白色沉淀A的离子方程式是____________________________。
④实验二中无色溶液变为蓝色溶液的离子方程式为____________________________。
(3)为排除实验一溶液中的影响,小组同学进行了实验三
实验三:Ⅰ.向溶液中加入浓溶液,过滤,洗涤沉淀,取洗涤液,____________(填操作和现象)。将洗净的固体加水得悬浊液,测得。
Ⅱ.向悬浊液中通入至过量,观察到局部先产生少量浅黄色沉淀,而后转化为紫红色固体,溶液变为绿色[含],测得溶液。
Ⅲ.向溶液中通入2至过量,无明显现象。
①补全步骤Ⅰ中的操作和现象。
②经确认浅黄色沉淀为,紫红色固体为。与悬浊液发生了氧化还原反应。结合化学用语解释产生的原因___________。
③解释实验三中步骤Ⅲ与步骤Ⅱ现象不同的原因___________。
(4)综合上述实验,与二价铜反应的产物与___________等因素有关(答出两点即可)。
北京一零一中2023—2024学年度第二学期
高三化学三模参考答案
15.(10分)
(1)c
(2)① ②
(3)① ②配位键
(4)①电子层数:,但核电荷数:,两离子的原子核对最外层电子的吸引力相近,故两者离子半径相近(2分)
②化学
③和均为离子化合物,结构相似,阴阳离子带电量均相同,离子半径大,阴阳离子间吸引力更弱,故更易迁移(2分)
16.(11分)
(1) (2分)
(2)
(3)AB(2分)
(4)①(或)(2分)
②0.75
(5)①最后半滴溶液滴下时,溶液由蓝色变为无色,半分钟内不变蓝
②
③偏低
17.(10分)
(1)(浓)(2分)
(2),(或)(2分)(3)还原反应
(4)bc(2分)(5)保护,防止被氧化
(6)N:
P:(写一种即可)
18.(12分)
(1)增大接触面积,加快反应速率
(2)(2分)
(3)①(2分)
②的浸出率较高,且较环保(或节约酸和氧化剂的用量)(2分)
③提高浸出液中浓度(或提高氧化剂和酸的利用率/节约后续纯碱的用量)
(4)结合,减小,,,这两个电离平衡均正向移动,增大,与结合形成磷酸铁晶体(2分)
(5)过程ⅳ若使用饱和溶液,其中较大,易形成沉淀与磷酸铁沉淀一同析出,减少高纯的产量
(6)趁热过滤,用热水洗涤,干燥
19.(15分)
(1)
(2)①溶液
②)白色沉淀溶于氨水得到无色溶液,静置变蓝,说明无,含;加入溶液无明显现象,说明不含、;加入足量稀硝酸和硝酸银溶液,产生白色沉淀说明含有。(注:设计方案时需要考虑先加溶液,产生白色沉淀后,再加盐酸,试剂操作时,加入溶液无现象,已经说明不含、)(2分)
③(2分)
④(2分)
(3)①加入溶液,无沉淀生成(2分)
②)生成的不稳定分解为,过量溶液酸性增强,发生反应
(2分)
③碱性条件下的还原性增强(合理给分)
(4)是否存在、溶液、的通入量(2分)
选项
性质
解释
A
热稳定性:
中存在氢键
B
熔点:晶体硅
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)





