

2024年黑龙江省大庆市第五十五中学中考一模化学试题
展开A.冰融化成水
B.防毒面具中充填活性炭以吸附毒气
C.一定条件下将石墨制成金刚石
D.工业上通过分离液态空气制氧气
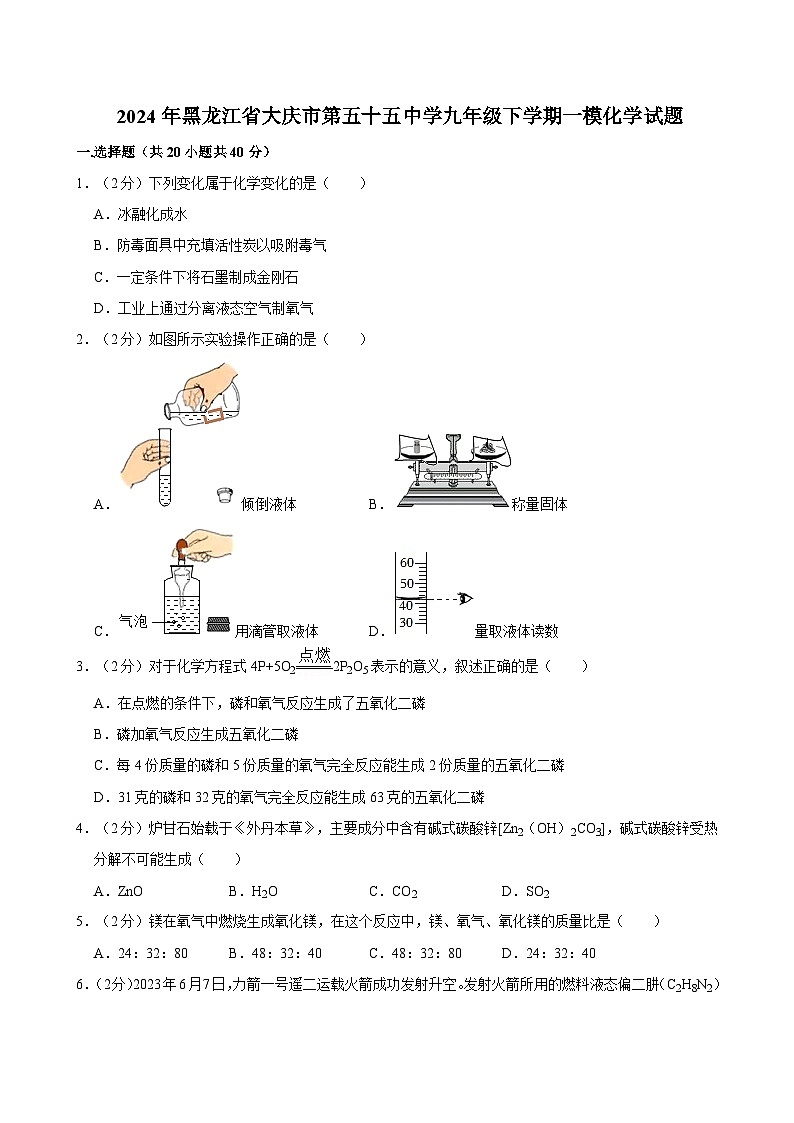
2.(2分)如图所示实验操作正确的是( )
A.倾倒液体B.称量固体
C.用滴管取液体D.量取液体读数
3.(2分)对于化学方程式4P+5O22P2O5表示的意义,叙述正确的是( )
A.在点燃的条件下,磷和氧气反应生成了五氧化二磷
B.磷加氧气反应生成五氧化二磷
C.每4份质量的磷和5份质量的氧气完全反应能生成2份质量的五氧化二磷
D.31克的磷和32克的氧气完全反应能生成63克的五氧化二磷
4.(2分)炉甘石始载于《外丹本草》,主要成分中含有碱式碳酸锌[Zn2(OH)2CO3],碱式碳酸锌受热分解不可能生成( )
A.ZnOB.H2OC.CO2D.SO2
5.(2分)镁在氧气中燃烧生成氧化镁,在这个反应中,镁、氧气、氧化镁的质量比是( )
A.24:32:80B.48:32:40C.48:32:80D.24:32:40
6.(2分)2023年6月7日,力箭一号遥二运载火箭成功发射升空。发射火箭所用的燃料液态偏二肼(C2H8N2)与N2O4发射的反应为C2H8N2+2N2O43N2↑+2X↑+4H2O,则X为( )
A.CB.COC.CO2D.H2CO3
7.(2分)“微观﹣宏观﹣符号”三重表征是化学独特的表示物质及其变化的方法。如图是液化石油气成分之一燃烧前后分子种类变化的微观示意图,下列说法正确的是( )
A.生成丙与丁物质的质量比为11:6
B.反应前后各元素的化合价均不变
C.参加反应甲与乙的分子个数比为1:1
D.甲中碳、氢元素质量比为3:8
8.(2分)C60是1985年科学家发现的一种物质,下列关于它的叙述中,错误的是( )
①每个C60分子由60个碳原子构成 ②每个C60分子由60个碳元素组成 ③C60是一种单质 ④C60是一种化合物。
A.①③B.②④C.②③D.①④
9.(2分)在化学反应A+2B═C+D中,11.2gA和14.6gB恰好完全反应,生成25.4gC,同时得到D的质量是( )
A.11.2gB.0.4gC.0.8gD.14.6g
10.(2分)经测定某物质中只含有碳元素,关于该物质的说法正确的是( )
A.一定是金刚石B.一定是混合物
C.一定是一种碳单质D.一定不是化合物
11.(2分)下列关于化学反应2X+Y═2Z的叙述,错误的是( )
A.Z一定是化合物
B.若X和Y的相对分子质量分别为M和N,则Z的相对分子质量为(M+N)
C.在反应中X、Y、Z三种物质的粒子数目比为2:1:2
D.若agX完全反应生成bgZ,则同时消耗(b﹣a)gY
12.(2分)学会识图能发展科学思维。下列图像与反应过程的变化趋势对应正确的是( )
A.AB.BC.CD.D
13.(2分)在反应A+3B═2C+3D中,A、B的相对分子质量之比为5:6,若2.5gA与一定量的B恰好完全反应后,生成3.8gD。则生成C的质量为( )
A.9.6gB.7.7gC.6.8gD.8.8g
14.(2分)在密闭容器中点燃H2和O2的混合气体10克,完全反应后生成水9克,则原混合气体中H2和O2的质量可能是( )
A.H24克,O26克B.H25克,O25克
C.H22克,O28克D.H23克,O27克
15.(2分)下列关于碳单质用途的叙述中,错误的是( )
①橡胶里添加炭黑能增加耐磨性
②干电池里的碳棒是石墨制成的
③电冰箱除味剂是活性炭
④防毒面具用焦炭吸收有毒气体
⑤制糖工业用炭黑来吸附有色物质
⑥金刚石不仅能刻画玻璃,还能装在钻头上钻凿坚硬的岩层.
A.②①③B.②③④C.③④D.④⑤
16.(2分)在一个密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得密闭容器内仍然是A、B、C、D四种物质,测得有关数据如下表:关于此反应的认识不正确的是( )
A.X值为13
B.C可能是该反应的催化剂
C.B一定是化合物
D.该反应中D、B的相对分子质量之比一定为4:5
17.(2分)应用质量守恒定律进行判断:取A、B、C三种物质各20g,在一定条件下充分化合只能生成42g新物质D。若增加5gA,充分反应后原反应物中只有C剩余。下列说法错误的是( )
A.该反应是化合反应
B.第一次反应停止后,C剩余15g
C.反应中A和B的质量比是5:4
D.两次反应后,生成D的总质量为52.5g
18.(2分)现有碳酸钠和氯化钠的固体混合物17g,其中含氧元素2.4g,则原固体混合物中氯元素的质量分数是( )
A.60.7%B.46.9%C.41.8%D.无法计算
19.(2分)已知:2KMnO4K2MnO4+MnO2+O2↑。将16g高锰酸钾固体放在试管中加热,反应后剩余物质的质量为14.8g,则剩余的物质是( )
A.锰酸钾
B.锰酸钾和二氧化锰
C.二氧化锰
D.高锰酸钾、二氧化锰和锰酸钾
20.(2分)已知23g纯净物X在足量的氧气中充分燃烧,生成44g二氧化碳和27g水。下列说法中错误的是( )
A.X中一定含有三种元素
B.该反应消耗氧气的质量为48g
C.X可能的化学式是CH3O
D.X中C、H两种元素的质量比为4:1
二、填空题(18分)
21.(4分)用化学用语填空:
(1)金刚石的化学式 ;
(2)3个铁离子 ;
(3)地壳中含量最多的金属元素 ;
(4)氯化钠是由 构成。
22.(8分)配平或写出下列化学方程式:
(1) C+ Fe2O3 Fe+ CO2↑
(2) Al2O3+ HCl═ AlCl3+ H2O
(3)汽车尾气中的一氧化氮与一氧化碳在催化剂的作用下,反应生成二氧化碳和一种无污染的单质气体。写出该反应的化学方程式: 。
(4)氧化铁固体高温时会分解成四氧化三铁和一种气体,写出该反应的化学方程式: 。
23.(6分)理解、掌握质量守恒定律是学好化学的基础。
(1)由质量守恒定律可知,在化学反应前后,一定不变的是 (填序号)。
①分子种类
②原子种类
③分子数目
④原子数目
⑤物质质量
⑥元素种类
(2)某过氧化氢溶液中氢元素与氧元素的质量比为2:17,向38g该溶液中加入1g二氧化锰,充分反应后生成氧气的质量是 g。
(3)某气体由C2H4、C2H2、CH4中的一种或几种组成。取该气体样品在空气中完全燃烧,测得生成的二氧化碳和水的质量比为22:9。下列对该气体组成的判断正确的是 。
A.该气体中一定含有C2H4
B.该气体中一定没有CH4
C.该气体中可能含有C2H2
D.该气体可能同时含有C2H4、C2H2、CH4
三.实验题(共3小题)
24.(7分)根据如图装置,结合所学化学实验知识,请你参与回答问题:
(1)写出编号仪器的名称:① ;② 。
(2)若用过氧化氢溶液和二氧化锰制取并收集较纯净的氧气是 (填装置字母编号),反应的化学方程式为 。
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取,则制取甲烷的发生装置和收集装置的组合是 (填装置字母编号),若用F装置收集较为干燥的甲烷,则气体应从 端进(填“a”或“b”)。
25.(6分)物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙、丙三位同学按下面的步骤进行探究:
(1)提出假设:物质发生化学变化前后总质量不变。
(2)设计并进行实验,甲设计的实验装置和选用的药品如图中A所示,发生反应化学方程式为 。乙设计的实验装置和选用的药品如B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。丙进行了图C所示的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平。然后,用酒精灯给a端铜丝加热数分钟。停止加热后冷却,他观察到的现象是 。
(3)实验结论:
甲认为在化学反应中,反应后生成的生成物的总质量与参加反应的反应物的总质量相等;乙、丙认为在化学反应中,反应后生成的生成物的总质量与参加反应的反应物的总质量不相等。
(4)大家一致认为甲的结论正确,如果用乙丙实验证明质量守恒定律应如何改进 。
26.(8分)为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如图所示的实验。实验步骤如下:先分别称量装置Ⅰ中蜡烛、装置Ⅱ、装置Ⅲ的质量,按如图图示连接好仪器装置,点燃蜡烛,同时从a导管抽气,一段时间后熄灭蜡烛,再分别称量装置Ⅰ中蜡烛、装置Ⅱ、装置Ⅲ的质量。(提示:浓硫酸只吸收水,氢氧化钠和氯化钙固体既可以吸收水分也可以吸收二氧化碳)实验数据如表。
(1)该实验中测得水的质量为 g,二氧化碳的质量为 g。
(2)由该实验数据计算,蜡烛中碳、氢元素的质量之比为 。
(3)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是 。
四、计算题(共21分)
27.(6分)实验室用电解水的方法制取氧气,若需要制得1.6克氧气,最少需要电解多少克水?
28.(7分)小华同学用16g氯酸钾和二氧化锰混合物在大试管中加热,并对试管中固体的质量在不同时刻作了记录,记录数据绘制成了如图,纵坐标表示试管中固体的质量,横坐标表示加热所用的时间,求:
(1)小华同学共制得氧气 g。
(2)他所用的混合物中氯酸钾质量是多少g(写出计算过程)?
29.(8分)实验室有一瓶含杂质的高锰酸钾,兴趣小组同学取10g该药品放入大试管中加热(杂质不参加反应),并在不同时刻测定试管内剩余固体物质的质量,实验数据记录如表,请回答:
(1)加热t5min时剩余固体质量为 g。
(2)计算该样品中高锰酸钾的质量分数?
参考答案与试题解析
一.选择题(共20小题共40分)
1.(2分)下列变化属于化学变化的是( )
A.冰融化成水
B.防毒面具中充填活性炭以吸附毒气
C.一定条件下将石墨制成金刚石
D.工业上通过分离液态空气制氧气
【解答】解:A、冰融化成水过程中只是形状发生改变,没有新物质生成,属于物理变化,故错误。
B、用木炭吸附冰箱内的异味是利用了木炭的吸附性,此过程中没有新物质生成,属于物理变化,故错误。
C、一定条件下将石墨制成金刚石过程中有新物质金刚石生成,属于化学变化,故正确。
D、工业上通过分离液态空气制过程中只是状态发生改变,没有新物质生成,属于物理变化,故错误。
故选:C。
2.(2分)如图所示实验操作正确的是( )
A.倾倒液体B.称量固体
C.用滴管取液体D.量取液体读数
【解答】解:A、取液体药品时,瓶塞倒放,标签向着手心,试管要倾斜,试管口与试剂瓶口紧挨着,故错误;
B、托盘天平称量物体的质量时,应左物右码,故错误;
C、吸取液体药品时应该在外面把胶头滴管内的空气赶净,再把胶头滴管伸入试剂瓶内吸取液体,图中有气泡说明是在试剂瓶里赶净空气,故错误;
D、用量筒量取液体读数时,视线要与凹液面的最低处保持水平,故正确;
故选:D。
3.(2分)对于化学方程式4P+5O22P2O5表示的意义,叙述正确的是( )
A.在点燃的条件下,磷和氧气反应生成了五氧化二磷
B.磷加氧气反应生成五氧化二磷
C.每4份质量的磷和5份质量的氧气完全反应能生成2份质量的五氧化二磷
D.31克的磷和32克的氧气完全反应能生成63克的五氧化二磷
【解答】解:A、该反应可表示在点燃的条件下,磷和氧气反应生成了五氧化二磷,故选项正确。
B、在反应中“+”读作“和”,故选项错误。
C、从质量角度看,每124份质量的磷和160份质量的氧气在点燃的条件下反应生成284份质量的五氧化二磷,故选项错误。
D、从质量角度看,每124份质量的磷和160份质量的氧气在点燃的条件下反应生成284份质量的五氧化二磷,则31克的磷和40克的氧气完全反应能生成71克的五氧化二磷,即31克的磷和32克的氧气反应,磷有剩余,生成的五氧化二磷的质量一定小于63克,故选项错误。
故选:A。
4.(2分)炉甘石始载于《外丹本草》,主要成分中含有碱式碳酸锌[Zn2(OH)2CO3],碱式碳酸锌受热分解不可能生成( )
A.ZnOB.H2OC.CO2D.SO2
【解答】解:碱式碳酸锌【Zn(OH)2CO3】中含有锌、氧、氢、碳四种元素,没有硫元素,因此碱式碳酸锌受热分解不可能生成SO2。
故选:D。
5.(2分)镁在氧气中燃烧生成氧化镁,在这个反应中,镁、氧气、氧化镁的质量比是( )
A.24:32:80B.48:32:40C.48:32:80D.24:32:40
【解答】解:镁在氧气中燃烧生成氧化镁的化学方程式为:2Mg+O22MgO
48:32:80
该反应中镁、氧气、氧化镁的质量比是48:32:80。
故选:C。
6.(2分)2023年6月7日,力箭一号遥二运载火箭成功发射升空。发射火箭所用的燃料液态偏二肼(C2H8N2)与N2O4发射的反应为C2H8N2+2N2O43N2↑+2X↑+4H2O,则X为( )
A.CB.COC.CO2D.H2CO3
【解答】解:反应前碳原子是2个,反应后应该是2个,包含在2X中,反应前后氢原子都是8个,反应前后氮原子都是6个,反应前氧原子是8个,反应后应该是8个,其中4个包含在2X中,X的化学式为CO2。
故选:C。
7.(2分)“微观﹣宏观﹣符号”三重表征是化学独特的表示物质及其变化的方法。如图是液化石油气成分之一燃烧前后分子种类变化的微观示意图,下列说法正确的是( )
A.生成丙与丁物质的质量比为11:6
B.反应前后各元素的化合价均不变
C.参加反应甲与乙的分子个数比为1:1
D.甲中碳、氢元素质量比为3:8
【解答】解:由微观反应示意图可知,该反应是由C3H8和氧气在点燃的条件下反应生成二氧化碳和水,化学方程式为C3H8+5O23CO2+4H2O。
A.由化学方程式可知,生成丙与丁物质的质量比为(44×3):(18×4)=11:6,选项说法正确;
B.在该反应中,有单质参与反应,所以一定存在元素的化合价的改变,选项说法错误;
C.由化学方程式可知,参加反应甲(C3H8)与乙(O2)的分子个数比为1:5,选项说法错误;
D.甲物质的化学式为C3H8,其中碳、氢元素质量比为(12×3):(1×8)=9:2,选项说法错误。
故选:A。
8.(2分)C60是1985年科学家发现的一种物质,下列关于它的叙述中,错误的是( )
①每个C60分子由60个碳原子构成 ②每个C60分子由60个碳元素组成 ③C60是一种单质 ④C60是一种化合物。
A.①③B.②④C.②③D.①④
【解答】解:①由C60的化学式可知,每个C60分子由60个碳原子构成,故说法正确;
②由C60的化学式可知,每个C60分子由60个碳原子构成,元素不论个数,故选项说法错误;
③C60是由一种元素组成的纯净物,属于单质,故选项说法正确。
④C60是由一种元素组成的纯净物,属于单质,故选项说法错误。
故选:B。
9.(2分)在化学反应A+2B═C+D中,11.2gA和14.6gB恰好完全反应,生成25.4gC,同时得到D的质量是( )
A.11.2gB.0.4gC.0.8gD.14.6g
【解答】解:根据质量守恒定律,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,则生成D的质量为11.2g+14.6g﹣25.4g=0.4g;
故选:B。
10.(2分)经测定某物质中只含有碳元素,关于该物质的说法正确的是( )
A.一定是金刚石B.一定是混合物
C.一定是一种碳单质D.一定不是化合物
【解答】解:A、某物质中只含有碳元素,该物质不一定是金刚石,也可能是石墨,A错误;
B、某物质中只含有碳元素,该物质不一定是混合物,也可能是单质,B错误;
C、某物质中只含有碳元素,该物质不一定是一种碳单质,C错误;
D、某物质中只含有碳元素,该物质一定不会是化合物,因为化合物至少含有两种元素,D正确;
故选:D。
11.(2分)下列关于化学反应2X+Y═2Z的叙述,错误的是( )
A.Z一定是化合物
B.若X和Y的相对分子质量分别为M和N,则Z的相对分子质量为(M+N)
C.在反应中X、Y、Z三种物质的粒子数目比为2:1:2
D.若agX完全反应生成bgZ,则同时消耗(b﹣a)gY
【解答】解:A、2X+Y═2Z属于化合反应,因此Z一定是化合物,故选项正确;
B、若X和Y的相对分子质量分别为M和N,则Z的相对分子质量为,故选项错误;
C、反应中X、Y、Z三种物质的粒子数目比为2:1:2,故选项正确;
D、根据质量守恒定律:agX完全反应生成bgZ,则同时消耗(b﹣a)gY,故选项正确;
故选:B。
12.(2分)学会识图能发展科学思维。下列图像与反应过程的变化趋势对应正确的是( )
A.AB.BC.CD.D
【解答】解:A、依据质量守恒定律,在密闭容器中燃烧一定量的镁条,物质的总质量不变,故选项图像错误;
B、二氧化锰在反应中作催化剂,反应前后质量不变,故选项图像正确;
C、高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,随着反应的进行,氧气逸出,剩余固体的质量减少,至完全反应不再发生改变,但不可能减少至0,故选项图像错误;
D、一定质量的过氧化氢制氧气,催化剂只能影响反应速率,不影响产生氧气的质量,有催化剂的反应速率快,至完全反应所需时间短,故选项图像错误;
故选:B。
13.(2分)在反应A+3B═2C+3D中,A、B的相对分子质量之比为5:6,若2.5gA与一定量的B恰好完全反应后,生成3.8gD。则生成C的质量为( )
A.9.6gB.7.7gC.6.8gD.8.8g
【解答】解:设A的相对分子质量为5a,则B的相对分子质量为6a;
设参加反应的B的质量为x。
A+3B═2C+3D
5a 18a
2.5g x
=
x=9g
根据质量守恒定律,生成C的质量为:2.5g+9g﹣3.8g=7.7g
故选:B。
14.(2分)在密闭容器中点燃H2和O2的混合气体10克,完全反应后生成水9克,则原混合气体中H2和O2的质量可能是( )
A.H24克,O26克B.H25克,O25克
C.H22克,O28克D.H23克,O27克
【解答】解:氢气和氧气在点燃的条件下生成水,反应的化学方程式及其质量关系如下:
2H2+O22H2O
4 32 36
1g 8g 9g
则1g氢气和8g氧气恰好完全反应生成9g水,而混合气体的质量是10g,则剩下的1g可能是氢气或氧气;当氢气剩余时,则氧气质量为8g,氢气质量为10g﹣8g=2g;当氧气剩余时,则氢气质量为1g,氧气质量为10g﹣1g=9g。
故选:C。
15.(2分)下列关于碳单质用途的叙述中,错误的是( )
①橡胶里添加炭黑能增加耐磨性
②干电池里的碳棒是石墨制成的
③电冰箱除味剂是活性炭
④防毒面具用焦炭吸收有毒气体
⑤制糖工业用炭黑来吸附有色物质
⑥金刚石不仅能刻画玻璃,还能装在钻头上钻凿坚硬的岩层.
A.②①③B.②③④C.③④D.④⑤
【解答】解:①橡胶里添加炭黑能增加耐磨性,故①正确;
②石墨具有导电性,可以用于制作干电池的碳棒,故②正确;
③活性炭具有吸附性,可用于电冰箱除味剂,故④正确;
④活性炭具有吸附性,防毒面具用活性炭吸收有毒气体,不是焦炭,故④错误;
⑤活性炭具有吸附性,能吸附色素,制糖工业用活性炭来吸附有色物质,不是炭黑,故⑤错误;
⑥由于金刚石的硬度大,金刚石不仅能刻画玻璃,还能装在钻头上钻凿坚硬的岩层。故⑥正确。
由以上分析可知,D正确。
故选:D。
16.(2分)在一个密闭容器中放入A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得密闭容器内仍然是A、B、C、D四种物质,测得有关数据如下表:关于此反应的认识不正确的是( )
A.X值为13
B.C可能是该反应的催化剂
C.B一定是化合物
D.该反应中D、B的相对分子质量之比一定为4:5
【解答】解:A、根据质量守恒定律,化学反应前后,物质的总质量不变,故18+1+2+32=X+26+2+12,X=13,故A正确;
B、C反应前后的质量不变,可能是该反应的催化剂,也可能不参加反应,故B正确;
C、反应后,A、D的质量减小,A、D是反应物,B的质量增加,B是生成物,该反应是A和D反应生成B,则B一定是化合物,故C正确;
D、无法确定相对分子质量之比,故D错误;
故选:D。
17.(2分)应用质量守恒定律进行判断:取A、B、C三种物质各20g,在一定条件下充分化合只能生成42g新物质D。若增加5gA,充分反应后原反应物中只有C剩余。下列说法错误的是( )
A.该反应是化合反应
B.第一次反应停止后,C剩余15g
C.反应中A和B的质量比是5:4
D.两次反应后,生成D的总质量为52.5g
【解答】解:A、该反应中反应物是三种,生成物是一种,符合多变一的特点,所以该反应属于化合反应,故选项说法正确。
B、设第一次反应消耗B物质质量为x,则有20g:x=5:4,解得x=16g,即第一次反应消耗B物质16g,那么第一次反应消耗C物质的质量为:42g﹣20g﹣16g=6g,所以第一次反应停止后C剩余:20g﹣6g=14g,故选项说法错误。
C、反应中A和B的质量比是25g:20g=5:4,故选项说法正确。
D、设两次反应后,生成D的总质量为y,则有20g:42g=25g:y,解得y=52.5g,故选项说法正确。
故选:B。
18.(2分)现有碳酸钠和氯化钠的固体混合物17g,其中含氧元素2.4g,则原固体混合物中氯元素的质量分数是( )
A.60.7%B.46.9%C.41.8%D.无法计算
【解答】解:由于只要碳酸钠中含有氧元素,所以根据含氧元素2.4g,可求碳酸钠的质量为2.4g÷=5.3g,则氯化钠的质量为17g﹣5.3g=11.7g。则原固体混合物中氯元素的质量分数是×100%≈41.8%
故选:C。
19.(2分)已知:2KMnO4K2MnO4+MnO2+O2↑。将16g高锰酸钾固体放在试管中加热,反应后剩余物质的质量为14.8g,则剩余的物质是( )
A.锰酸钾
B.锰酸钾和二氧化锰
C.二氧化锰
D.高锰酸钾、二氧化锰和锰酸钾
【解答】解:高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,根据质量守恒定律,反应前后物质的总质量不变,则生成氧气的质量为:16g﹣14.8g=1.2g,
设生成1.2g氧气,反应的高锰酸钾质量为x。
2KMnO4K2MnO4+MnO2+O2↑
316 32
x 1.2g
x=11.85g
则剩余的高锰酸钾的质量为:16g﹣11.85g=4.15g,所以剩余固体物质是:高锰酸钾、二氧化锰和锰酸钾。
故选:D。
20.(2分)已知23g纯净物X在足量的氧气中充分燃烧,生成44g二氧化碳和27g水。下列说法中错误的是( )
A.X中一定含有三种元素
B.该反应消耗氧气的质量为48g
C.X可能的化学式是CH3O
D.X中C、H两种元素的质量比为4:1
【解答】解:44gCO2中含有碳元素的质量为:44g××100%=12g,27g水中含有氢元素的质量为:27g××100%=3g,生成物44g二氧化碳和27g水中所含碳、氢元素的质量和=12g+3g=15g,15g<23g,该物质中含氧元素的质量为:23g﹣15g=8g,则X中一定含有碳、氢、氧三种元素。
A、由上述分析,X中一定含有碳、氢、氧三种元素,故选项说法正确。
B、由质量守恒定律,该反应消耗氧气的质量为44g+27g﹣23g=48,故选项说法正确。
C、X中C、H两种元素的质量比为12g:3g=4:1,X不可能的化学式是CH3O,故选项说法错误。
D、由上述计算可知,X中C、H两种元素的质量比为4:1,故选项说法正确。
故选:C。
二、填空题(18分)
21.(4分)用化学用语填空:
(1)金刚石的化学式 C ;
(2)3个铁离子 3Fe3+ ;
(3)地壳中含量最多的金属元素 Al ;
(4)氯化钠是由 Na+、Cl﹣ 构成。
【解答】解:(1)金刚石是碳的单质,表示为C;故答案为:C;
(2)符号前面的数字,表示原子、分子或离子的个数;3个铁离子表示为3Fe3+;故答案为:3Fe3+;
(3)书写元素符号时,第一个字母要大写,第二个字母要小写;地壳中含量最多的金属元素是铝元素,表示为Al;故答案为:Al;
(4)氯化钠是由钠离子和氯离子构成的,表示为Na+、Cl﹣;故答案为:Na+、Cl﹣。
22.(8分)配平或写出下列化学方程式:
(1) 3 C+ 2 Fe2O3 4 Fe+ 3 CO2↑
(2) 1 Al2O3+ 6 HCl═ 2 AlCl3+ 3 H2O
(3)汽车尾气中的一氧化氮与一氧化碳在催化剂的作用下,反应生成二氧化碳和一种无污染的单质气体。写出该反应的化学方程式: 2CO+2NON2+2CO2 。
(4)氧化铁固体高温时会分解成四氧化三铁和一种气体,写出该反应的化学方程式: 6Fe2O34Fe3O4+O2↑ 。
【解答】解:(1)利用最小公倍数法进行配平,以氧原子作为配平的起点,Fe2O3、CO2前面的化学计量数分别为:2、3,最后调整碳、铁前面的化学计量数为3、4。
(2)本题可利用“定一法”进行配平,把Al2O3的化学计量数定为1,则HCl、AlCl3、H2O前面的化学计量数分别为:6、2、3。
(3)汽车尾气中的一氧化氮与一氧化碳在催化剂的作用下,反应生成二氧化碳和一种无污染的单质气体,由质量守恒定律,反应前后元素种类不变,生成的单质气体是氮气,反应的化学方程式为2CO+2NON2+2CO2。
(4)氧化铁固体高温时会分解成四氧化三铁和一种气体,由质量守恒定律,反应前后元素种类不变,生成的气体是氧气,反应的化学方程式为6Fe2O34Fe3O4+O2↑。
故答案为:
(1)3;2;4;3;
(2)1;6;2;3;
(3)2CO+2NON2+2CO2;
(4)6Fe2O34Fe3O4+O2↑。
23.(6分)理解、掌握质量守恒定律是学好化学的基础。
(1)由质量守恒定律可知,在化学反应前后,一定不变的是 ②④⑥ (填序号)。
①分子种类
②原子种类
③分子数目
④原子数目
⑤物质质量
⑥元素种类
(2)某过氧化氢溶液中氢元素与氧元素的质量比为2:17,向38g该溶液中加入1g二氧化锰,充分反应后生成氧气的质量是 2 g。
(3)某气体由C2H4、C2H2、CH4中的一种或几种组成。取该气体样品在空气中完全燃烧,测得生成的二氧化碳和水的质量比为22:9。下列对该气体组成的判断正确的是 C 。
A.该气体中一定含有C2H4
B.该气体中一定没有CH4
C.该气体中可能含有C2H2
D.该气体可能同时含有C2H4、C2H2、CH4
【解答】解:(1)由质量守恒定律可知,在化学反应前后,一定不变的是原子种类、原子数目、元素种类;故选:②④⑥;
(2)某过氧化氢溶液中氢元素与氧元素的质量比为2:17,则38g双氧水溶液中氢元素质量为:38g×=4g。过氧化氢完全反应后生成水和氧气,该过程中氢元素的质量没有改变,所以反应后水的质量为:4g÷(×100%)=36g。根据质量守恒定律,生成氧气的质量为:38g﹣36g=2g;
(3)生成的二氧化碳和水的质量比为22:9,则碳元素和氢元素的质量比为:(22×):(9×)=6:1,故碳氢原子的个数比为:=1:2,
A.C2H4分子中碳氢原子的个数比为1:2,符合条件,但该气体可以是混合物,不一定只含有C2H4,故错误;
B.若是含一个CH4和一个C2H2,则能达到碳氢原子个数比是1:2,故该气体中可以含有CH4,故错误;
C.该气体中可能含有C2H2,故正确;
D.该气体可能同时含有CH4、C2H2、C2H4,故错误;
故选:C。
故答案为:(1)②④⑥;
(2)2;
(3)C。
三.实验题(共3小题)
24.(7分)根据如图装置,结合所学化学实验知识,请你参与回答问题:
(1)写出编号仪器的名称:① 酒精灯 ;② 锥形瓶 。
(2)若用过氧化氢溶液和二氧化锰制取并收集较纯净的氧气是 BE (填装置字母编号),反应的化学方程式为 2H2O22H2O+O2↑ 。
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取,则制取甲烷的发生装置和收集装置的组合是 AD或AE或AF (填装置字母编号),若用F装置收集较为干燥的甲烷,则气体应从 b 端进(填“a”或“b”)。
【解答】解:(1)由图可知,仪器①的名称是:酒精灯;仪器②的名称是:锥形瓶。
(2)若用过氧化氢溶液和二氧化锰制取氧气,需要固液常温型发生装置,用排水法收集的氧气较纯净,所以需要的装置是:BE;过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O22H2O+O2↑。
(3)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,需要固体加热型发生装置,甲烷是密度小于空气、难溶于水的气体,可以用向下排空气法或排水法来收集,所以制取甲烷的发生装置和收集装置的组合是:AD或AE或AF;甲烷的密度比空气小,若用F装置收集较为干燥的甲烷,则气体应从b端进。
故答案为:
(1)酒精灯;锥形瓶;
(2)BE;2H2O22H2O+O2↑;
(3)AD或AE或AF;b。
25.(6分)物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙、丙三位同学按下面的步骤进行探究:
(1)提出假设:物质发生化学变化前后总质量不变。
(2)设计并进行实验,甲设计的实验装置和选用的药品如图中A所示,发生反应化学方程式为 4P+5O22P2O5 。乙设计的实验装置和选用的药品如B所示,他们在反应前后都进行了规范的操作,准确的称量和细致的观察。丙进行了图C所示的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平。然后,用酒精灯给a端铜丝加热数分钟。停止加热后冷却,他观察到的现象是 a端上铜丝变黑,玻璃棒a端下沉 。
(3)实验结论:
甲认为在化学反应中,反应后生成的生成物的总质量与参加反应的反应物的总质量相等;乙、丙认为在化学反应中,反应后生成的生成物的总质量与参加反应的反应物的总质量不相等。
(4)大家一致认为甲的结论正确,如果用乙丙实验证明质量守恒定律应如何改进 使反应在密闭装置中进行 。
【解答】解:(2)红磷燃烧生成五氧化二磷,由此书写化学方程式为:4P+5O22P2O5。铜在加热的条件下会与氧气反应生成黑色的氧化铜,会使铜丝质量增加,会使左端下沉。故答案为:4P+5O22P2O5; a端上铜丝变黑,玻璃棒a端下沉;
(4)B实验反应后生成的气体逸散到空气中去了,C实验a端铜丝增加了氧元素的质量,在验证质量守恒定律时,若有气体参加或生成的实验必须在密闭的环境中进行,生成物的质量等于参加的反应物的质量之和。故答案为:使反应在密闭装置中进行。
26.(8分)为了测定蜡烛中碳、氢两种元素的质量比,某化学兴趣小组设计了如图所示的实验。实验步骤如下:先分别称量装置Ⅰ中蜡烛、装置Ⅱ、装置Ⅲ的质量,按如图图示连接好仪器装置,点燃蜡烛,同时从a导管抽气,一段时间后熄灭蜡烛,再分别称量装置Ⅰ中蜡烛、装置Ⅱ、装置Ⅲ的质量。(提示:浓硫酸只吸收水,氢氧化钠和氯化钙固体既可以吸收水分也可以吸收二氧化碳)实验数据如表。
(1)该实验中测得水的质量为 1.8 g,二氧化碳的质量为 4.4 g。
(2)由该实验数据计算,蜡烛中碳、氢元素的质量之比为 6:1 。
(3)理论上,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛失去的质量,其原因是 装置Ⅱ和Ⅲ增加的质量等于消耗的蜡烛和氧气的总质量 。
【解答】解:(1)蜡烛和氧气点燃生成水和二氧化碳,浓硫酸只吸收水,氢氧化钠和氯化钙固体既可以吸收水分也可以吸收二氧化碳;由表中数据可知,反应后生成水的质量为:184.1﹣182.3=1.8g;反应后生成二氧化碳的质量为:216.6﹣212.2=4.4g。
(2)1.8g水中氢元素的质量为:1.8g××100%=0.2g,4.4g二氧化碳中碳元素的质量为:4.4g××100%=1.2g,所以蜡烛中碳、氢元素的质量之比为1.2g:0.2g=6:1。
(3)蜡烛燃烧需要氧气,氧气来自空气中,根据质量守恒定律,参加反应的各物质的质量总和等于生成的各物质的质量总和,即消耗的蜡烛和氧气质量总和等于生成的水和二氧化碳的质量总和,装置Ⅱ和装置Ⅲ增加的总质量大于蜡烛减少的质量,是因为氧气参与了反应,装置Ⅱ和Ⅲ增加的质量等于消耗的蜡烛和氧气的总质量。
故答案为:
(1)1.8;4.4;
(2)6:1;
(3)装置Ⅱ和Ⅲ增加的质量等于消耗的蜡烛和氧气的总质量。
四、计算题(共21分)
27.(6分)实验室用电解水的方法制取氧气,若需要制得1.6克氧气,最少需要电解多少克水?
【解答】解:设需要消耗水的质量为x。
2H2O2H2↑+O2↑
36 32
x 1.6g
=
x=1.8g
答:需要电解水1.8g。
28.(7分)小华同学用16g氯酸钾和二氧化锰混合物在大试管中加热,并对试管中固体的质量在不同时刻作了记录,记录数据绘制成了如图,纵坐标表示试管中固体的质量,横坐标表示加热所用的时间,求:
(1)小华同学共制得氧气 4.8 g。
(2)他所用的混合物中氯酸钾质量是多少g(写出计算过程)?
【解答】解:(1)共制得氧气的质量为16g﹣11.2g=4.8g;故答案为:4.8;
(2)设样品中氯酸钾的质量为x。
2KClO32KCl+3O2↑
245 96
x 4.8g
=
x=12.25g
答:所用的混合物中氯酸钾质量是12.25g。
29.(8分)实验室有一瓶含杂质的高锰酸钾,兴趣小组同学取10g该药品放入大试管中加热(杂质不参加反应),并在不同时刻测定试管内剩余固体物质的质量,实验数据记录如表,请回答:
(1)加热t5min时剩余固体质量为 9.04 g。
(2)计算该样品中高锰酸钾的质量分数?
【解答】解:(1)从表中数据可知,前几次剩余固体不断减少,t4时剩余固体质量9.04g,t6时剩余固体质量9.04g,说明t4时间后,固体不再减少,则加热t5min时剩余固体质量为9.04g;
(2)反应前固体的总质量为10g,反应结束后固体的质量为9.04g,根据质量守恒定律可知,减少的质量就是生成氧气的质量,则生成氧气的质量为10g﹣9.04g=0.96g,
设该样品中高锰酸钾的质量为x,
2KMnO4K2MnO4+MnO2+O2↑
316 32
x 0.96g
=
x=9.48g
则该样品中高锰酸钾的质量分数为×100%=94.8%;
答:该样品中高锰酸钾的质量分数94.8%。
A.在密闭容器中燃烧一定量的镁条
B.加热氯酸钾和二氧化锰的固体混合物
C.加热一定质量的高锰酸钾固体
D.一定质量的过氧化氢制氧气
物质
A
B
C
D
反应前质量/g
18
1
2
32
反应后质量/g
X
26
2
12
蜡烛
装置Ⅱ
装置Ⅲ
反应前的质量/g
15.8
182.3
212.2
反应后的质量/g
14.4
184.1
216.6
加热时间/min
t0
t1
t2
t3
t4
t5
t6
剩余固体质量/g
10
10
9.24
9.16
9.04
9.04
A.在密闭容器中燃烧一定量的镁条
B.加热氯酸钾和二氧化锰的固体混合物
C.加热一定质量的高锰酸钾固体
D.一定质量的过氧化氢制氧气
物质
A
B
C
D
反应前质量/g
18
1
2
32
反应后质量/g
X
26
2
12
蜡烛
装置Ⅱ
装置Ⅲ
反应前的质量/g
15.8
182.3
212.2
反应后的质量/g
14.4
184.1
216.6
加热时间/min
t0
t1
t2
t3
t4
t5
t6
剩余固体质量/g
10
10
9.24
9.16
9.04
9.04
2024年黑龙江省大庆市第五十五中学九年级下学期一模化学试题: 这是一份2024年黑龙江省大庆市第五十五中学九年级下学期一模化学试题,共8页。
2024年黑龙江省大庆市高新区学校中考一模化学试题: 这是一份2024年黑龙江省大庆市高新区学校中考一模化学试题,文件包含2024年大庆市高新区学校第一次初中升学模拟考试化学学科试题docx、2024年大庆市高新区学校第一次初中升学模拟考试化学学科试题答案docx等2份试卷配套教学资源,其中试卷共6页, 欢迎下载使用。
2023年陕西省西安市第五十五中学中考五模化学试题(含解析): 这是一份2023年陕西省西安市第五十五中学中考五模化学试题(含解析),共15页。试卷主要包含了单选题,填空题,实验题,科学探究题,计算题等内容,欢迎下载使用。












