

66,河南省安阳市部分学校2023-2024学年九年级上学期期末化学试题
展开1.下列变化中,属于化学变化的是( )
A.冰雪融化B.矿石粉碎C.蜡烛燃烧D.干冰升华
2.下列说法正确的是( )
A.石油和煤综合利用后能得到塑料、化肥、医药、染料等产品
B.进入煤矿井,用火把照明
C.将二氧化碳通入紫色石蕊试液中,紫色石蕊试液变蓝色
D.涤纶和羊毛燃烧都可闻到一股烧毛发的焦煳味
3.学习化学我们经常做实验。下列实验操作正确的是( )
A.闻气体气味B.往试管里加锌粒
C.加热液体D.量取液体
4.化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数和质子数之和。
例如用表示核内有6个质子和7个中子的碳原子。下列关于和的说法正确的是( )
A.不属于同种元素B.原子中核外电子数不同
C.原子中含有相同数目的中子D.前者的质量大于后者的质量
5.用浓盐酸配制一定溶质质量分数的稀盐酸,实验时必不可少的一组仪器是( )
A.量筒、烧杯、漏斗、玻璃棒B.托盘天平、玻璃棒、药匙、烧杯
C.托盘天平、玻璃棒、量筒、烧杯D.玻璃棒、量筒、烧杯、胶头滴管
6.某化学小组的同学讨论辨析以下说法,正确的是( )
①汽油能清洗油污,利用的是乳化原理;②红磷在氧气中燃烧,产生大量的白雾
③凡是pH<7的降雨,都可称为酸雨④合金是具有金属特性的混合物
⑤升高温度或减小压强,气体的溶解度均会减小
A.④⑤B.③④⑤C.①②③D.①②③④⑤
7.实验现象的观察主要是指用眼看、鼻闻、耳听、手感等方式得到的实验现象,下列实验现象不合理的是( )
A.硫在氧气中燃烧:发出明亮的蓝紫色火焰,生成一种有刺激性气味的气体
B.向盛有少量碳酸钠固体的烧杯中滴加稀盐酸:有气泡冒出您看到的资料都源自我们平台,家威杏 MXSJ663 低至0.3元/份C.在硫酸铜溶液中滴加氢氧化钠溶液:有蓝色沉淀生成
D.铁丝在空气中燃烧:剧烈燃烧,火星四射,放出热量,生成黑色固体
8.2020年初防疫“新冠肺炎”期间,84消毒液[有效成分为次氯酸钠(NaClO)]对新型冠状病毒有明显的消灭作用,下列有关次氯酸钠的说法正确的是( )
A.NaClO的相对分子质量为74.5B.NaClO中钠元素和氯元素质量比为1:1
C.NaClO由四种元素组成D.NaClO中元素质量分数最大的是钠元素
9.在一密闭容器内有氧气,二氧化碳,水蒸气和一种未知物质M,在一定条件下充分反应,测知反应前后各物质的质量如下:
下列说法正确的是( )
A.X应为64B.该反应是分解反应
C.M的化学式可能是CH4D.该反应中氧气和二氧化碳的化学计量数之比是3:1
10.硅材料是太阳能电池及电脑芯片不可缺少的材料,随着一批多晶硅生产企业在乐山建成投产,乐山将成为我国重要的硅材料产业基地。下面是多晶硅生产过程中的一个重要反应:,该反应的基本类型是( )
A.化合反应B.分解反应C.置换反应D.复分解反应
11.除去下列物质中的少量杂质,实验方案能达到除杂目的的是( )
A.AB.BC.CD.D
12.下述物质在氧气中燃烧的主要现象和所属反应类型完全正确的是( )
A.硫-微弱的淡蓝色火焰-氧化反应B.红磷-黄白色火焰-分解反应
C.铁-剧烈燃烧,火星四射-化合反应D.木炭-发出淡蓝色火焰-化合反应
13.下列探究实验能达到目的的是( )
A.探究温度对分子运动速率的影响,只将少量品红加入到热水中
B.探究吸入空气和呼出气体中CO2含量不同,将燃着的木条分别伸入等体积两种气体中
C.探究MnO2是否是H2O2分解的催化剂,比较MnO2加到H2O2溶液前后产生气泡快慢
D.探究吸入空气和呼出气体中O2含量不同,将燃着的木条分别伸入等体积两种气体中
14.在100g含碳酸钙90%的石灰石中,加入过量的稀盐酸(杂质不参加反应)。有关说法正确的是( )
A.参加反应的碳酸钙与生成的二氧化碳的质量比为1:1
B.盐酸过量越多,生成的二氧化碳也越多
C.参加反应的碳酸钙的物质的量为0.1ml
D.生成的氯化钙中,钙元素的质量为36g
二、填空与简答(每空1分,共47分)
15.“宏观—微观—符号”三重表征是化学学科的重要思想,请用化学用语填空。
(1)2个铁原子______。
(2)构成硫酸铜的阴离子______。
(3)氢氧化铝______。
(4)2个亚铁离子______。
16.化学来源于生活,又服务于生活。请用所学的化学知识回答下列问题:
(1)石膏的主要成分为硫酸钙,构成该物质的粒子是______(填粒子符号)。其中硫元素的原子结构示意图为______。
(2)发生森林火灾时,在大火蔓延路线前砍掉一片树木,形成隔离带,其灭火原理是______。
(3)在新冠疫情期间,采用喷洒次氯酸钠(NaClO)对环境进行消毒,其原因是次氯酸钠与空气中的CO2和H2O反应生成了有强氧化性的次氯酸(HCIO)和碳酸氢钠,则该反应的化学方程式为______。
17.奥运会是世界规模最大的综合性运动会。
(1)2008年奥运会“祥云”火炬主要的燃料是丙烷(C3H8),丙烷中碳元素与氢元素的质量比为______。
(2)2022年冬季奥运会“飞扬”火炬的燃料是氢气,写出氢气在空气中燃烧的化学方程式______。
(3)速滑场馆“冰丝带”采用CO2跨临界直接制冰。从微粒的角度分析,CO2由气态变为固态时,变化的是______。
(4)张家口冬奥村采暖设备使用的是风能发电,使用新能源的优点是______。
18.水和溶液在生产、生活中有着重要的作用。
(1)生活中常用______的方法降低水的硬度。
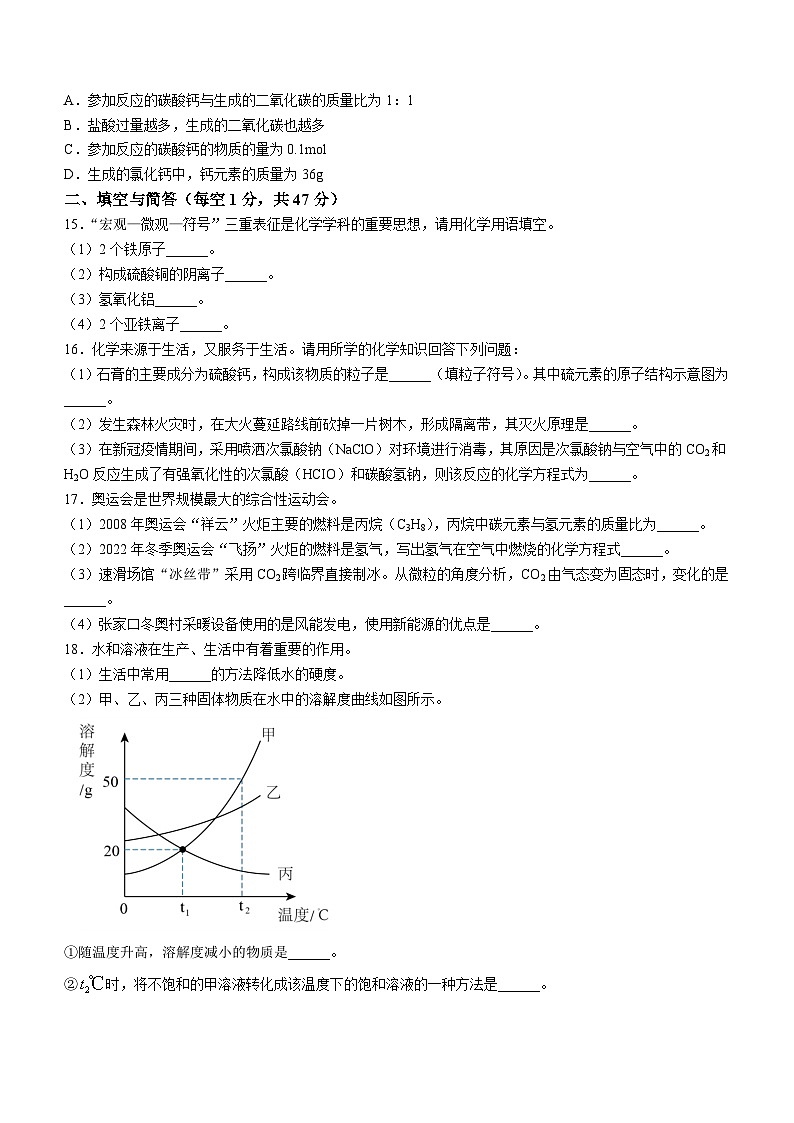
(2)甲、乙、丙三种固体物质在水中的溶解度曲线如图所示。
①随温度升高,溶解度减小的物质是______。
②时,将不饱和的甲溶液转化成该温度下的饱和溶液的一种方法是______。
③时,分别将50g甲、乙、丙固体溶于水配成饱和溶液,则甲、乙、丙三种物质需要水的质量关系为______。
④若甲中混有少量乙,提纯甲的方法是______。
(3)下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答。
①在时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为______g。
②由表中数据分析可知,氯化钠和硝酸钾在某一温度时具有相同的溶解度s,则s的取值范围是______。
19.A、B、C、D、E、F几种物质在一定的条件下存在如下图所示的转化关系。A、B为无色液体,D、F为黑色固体,C是一种常见的气体,E在C中剧烈燃烧,火星四射。
(1)物质D在反应①中起______作用。
(2)写出反应①的文字(或符号)表达式______,该反应的类型属于______反应。
(3)写出反应②的文字(或符号)表达式______,该反应的类型属于______反应。
20.在一个密闭的容器中有A、B、C、D四种物质,在一定条件充分反应,测得反应前后各物质的质量如表:
(1)试写出该反应的化学方程式______。
(2)此反应的基本反应类型为______。
(3)参加反应的物质的总质量为______。
(4)X的值为______。
21.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
图1 图2 图3
图4
(1)如图1,X是氢气、汞、氯化钠三种物质,由原子直接构成的物质是______(填化学符号,下同):由分子构成的物质是______,Y是______(填微粒名称)。
(2)如图2所示,可观察到的现象是______,此现象说明分子具有的性质是______。
(3)如图3所示,该反应的化学方程式为______。
(4)如图4所示为气体分子的示意图,图中“●”和“○”分别表示质子数不同的两种原子,其中表示化合物的是______(填字母序号)。
22.在人类社会的发展进程中,金属起着重要的作用,结合所学知识回答下列问题:
(1)铝合金与铝片相互刻画,在铝片表面会留下划痕,说明铝合金比铝硬度______(选填“大”或“小”)。
(2)汽车表面的烤漆,不仅美观还能防锈,其防锈的原理是______。
(3)高炉炼铁得到的产品是生铁,生铁和钢都是铁的合金,性能不同是因为______。
(4)在含有硝酸银、硝酸亚铁和硝酸铝的混合溶液中,加入一定量的锌,充分反应后,过滤,滤液仍为浅绿
色,则此时滤液中一定含有的溶质是______,滤渣可能含有的物质______。
23.海洋是人类千万年来取之不尽、用之不竭的巨大资源宝库。
(1)海底蕴着丰富的矿产资源。我国在南海可燃冰试采成功,“中国方案”实现历史性跨越:请你写出可燃
冰(主要成分CH4)完全燃烧的化学方程式______。
(2)海水“晒盐”得到的粗盐。含有氯化镁,氯化钙、硫酸钠等可溶性杂质,必须对其进行分离和提纯,才能用于工业生产和人们的日常生活。某实验小组设计如图所示流程除去粗盐中的可溶性杂质。得到氯化钠晶体。
步骤II加入的物质有①过量的碳酸钠溶液、②过量的氢氧化钠溶液、③过量的氯化钡溶液。正确的加入顺序为______(填序号)。
(3)精制的氯化钠具有广泛的工业用途。可以采用电解饱和氯化钠溶液的方法制得烧碱,同时还有氯气和氢气生成。写出该反应的化学方程式______。
三、实验题(共6分)
24.图是实验室制取气体的常用装置。
(1)写出一个用A装置制取O2的化学方程式______。
(2)B和C装置均可制取CO2,与B相比较,C的主要优点是什么?______。
(3)若用D装置采用排水法收集氧气,请简述操作步骤______。
四、综合应用题(共9分)
25.学习化学知识后,观察物质世界就要从化学视角看。水是一种重要的化学物质,在日常生活和实验室中有着不可替代的作用。请按要求回答下列问题:
(1)从物质元素组成角度看:水是由______组成的;
(2)从物质微粒构成角度看:水是由水分子构成,一个水分子是由______构成;
(3)从物质分类角度看:水属于化合物中的______;
(4)从物质变化角度看:如图实验中检验试管b内气体时的方法是______(步骤、现象、结论);
(5)从资源的利用与保护角度看;
①自来水厂生产流程可用下图表示:
结合上述过程写出两种净水方法______;
②海水淡化可缓解淡水资源匮乏的问题。下图为太阳能海水淡化装置示意图。利用该装置得到的淡水是______(填“硬水”或“软水”)。
③下图铁丝在氧气中燃烧实验中,集气瓶中水的作用是______。
(6)利用化学方程式计算:要生成48g氧气,需电解水多少g?
参考答案:
一、选择题(14小题,每小题2分,共28分)
1.C 2.A 3.D 4.D 5.D 6.A 7.D 8.A 9.C 10.C 11.C 12.C 13.D 14.D
二、填空与简答(每空1分,共47分)
15.(1)2Fe (2) (3) (4)
16.(1)
(2)清除可燃物
(3)
17.(1)9:2 (2) (3)分子之间的间隔 (4)环保,无污染
18.(1)煮沸 (2)丙 加溶质甲,或降温 甲<乙<丙 降温结晶 (3)145.8 36.0g
(2)过氧化氢水+氧气() 分解
(3)铁+氧气四氧化三铁(或) 化合
20.(1) (2)分解反应 (3)25g (4)20
21.(1)Hg H2 离子 (2)无色酚酞变红 分子在不断地运动
(3) (4)B
22.(1)大 (2)隔绝氧气和水 (3)含碳量不同 (4)硝酸铝、硝酸锌、硝酸亚铁 银/Ag
23. ③②①(或②③①或③①②)
三、实验题(共6分)
24.(1)
(2)控制反应速率
(3)先将装置装满水,再将氧气从a口通入
四、综合应用题(共9分)
25.(1)氢元素、氧元素
(2)两个氢原子和一个氧原子
(3)氧化物
(4)打开活塞,把一根带火星的木条放在玻璃尖嘴口,若木条复燃,说明是氧气
(5)沉淀、过滤、吸附、消毒(任两个即可) 软水 防止高温熔融物溅落瓶底,炸裂集气瓶
(6)解:设需电解水的质量为x,
解得:x=54g
答:需电解54g水。物质
氧气
二氧化碳
水
M
反应前质量/g
132
2
2
32
反应后质量/g
4
90
74
X
物质(括号内为杂质)
实验方案
A
氮气(氧气)
通过足量灼热氧化铜
B
氧化铜(木炭粉)
隔绝空气充分灼烧
C
硫酸亚铁溶液(硫酸铜)
加入过量铁粉、过滤
D
二氧化碳(一氧化碳)
通入氧气点燃
温度/℃
20
30
40
50
60
溶解度/g
NaCl
36.0
36.3
36.6
37.0
37.3
KNO3
31.6
45.8
63.9
85.5
110
物质
A
B
C
D
反应前质量/g
1
27
4
9
反应后质量/g
10
2
X
9
05,河南省安阳市部分学校2023-2024学年九年级上学期期末化学试题: 这是一份05,河南省安阳市部分学校2023-2024学年九年级上学期期末化学试题,共11页。
河南省安阳市部分学校2023-2024学年九年级上学期期末化学试题: 这是一份河南省安阳市部分学校2023-2024学年九年级上学期期末化学试题,共11页。
河南省安阳市文峰区2023-2024学年九年级上学期期末化学试题: 这是一份河南省安阳市文峰区2023-2024学年九年级上学期期末化学试题,共16页。试卷主要包含了本试卷分试题卷和答题卡两部分, 重氢可应用于光导纤维制备, 下列实验现象描述正确的是, 部分蔬菜及水果中含有维生素A等内容,欢迎下载使用。












