

12,山东省烟台市2023-2024学年高三上学期期末考试化学试题(1)
展开注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:Li 7 O 16 S 32 Mn 55 Cu 64 I 127
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题意。
1.中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
A.粮食酿酒过程中碳元素仅被还原
B.“白青[Cu2(OH)2CO3]得铁化为铜”,其中白青属于盐
C.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成
D.“盖此矾色绿,味酸,烧之则赤”,“味酸”是因绿矾水解产生H+
2.实验室中下列做法正确的是
A.用铜丝代替铂丝做焰色试验
B.用剩的白磷放回盛有水的广口瓶中
C.用10 mL量筒量取8.50 mLNaOH溶液
D.浓硝酸保存在带橡胶塞的棕色细口瓶中
3.X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X的原子半径小于Y的原子半径,Z基态原子核外有3个未成对电子,Y的核外电子数与Z的价层电子数相等,Q2是氧化性最强的单质,下列说法正确的是
A.键能:Z2
A.用甲装置鉴别Br2(g)和NO2(g) B.用乙装置除去水中的苯酚
C.用丙装置收集Cl2 D.用丁装置灼烧Fe(OH)3固体制得Fe2O3 您看到的资料都源自我们平台,家威鑫 MXSJ663 低至0.3/份 5.酞菁和酞菁钴可制得光动力学中的光敏剂,分子结构如图,其中酞菁分子中所有原子共平面,下列说法正确的是
A.酞菁钴中钴的化合价为+4
B.直径为1.5×10–9 m的酞菁钴分子能透过半透膜
C.酞菁钴中元素的电负性由大到小的顺序为N>C>H>C
D.标注①②的N原子的杂化方式是sp2,③的N原子的杂化方式是sp3
6.根据下列实验操作和现象能得到相应结论的是
7.化合物M的结构如图。下列关于M的说法错误的是
A.存在顺反异构
B.1 ml M最多可与4 ml H2反应
C.其酸性水解的产物均可与溴水反应
D.可形成分子内氢键和分子间氢键
8.实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
已知:苯甲酸乙酯的沸点为212.6 ℃,“乙醚-环己烷-水共沸物”的沸点为62.1 ℃。
下列说法正确的是
A.试剂X宜选用NaOH溶液
B.“操作1”过程中有机相1从分液漏斗的上口倒出
C.“操作2”需用到球形冷凝管
D.“操作5”中洗涤苯甲酸时,用乙醇的效果比用蒸馏水好
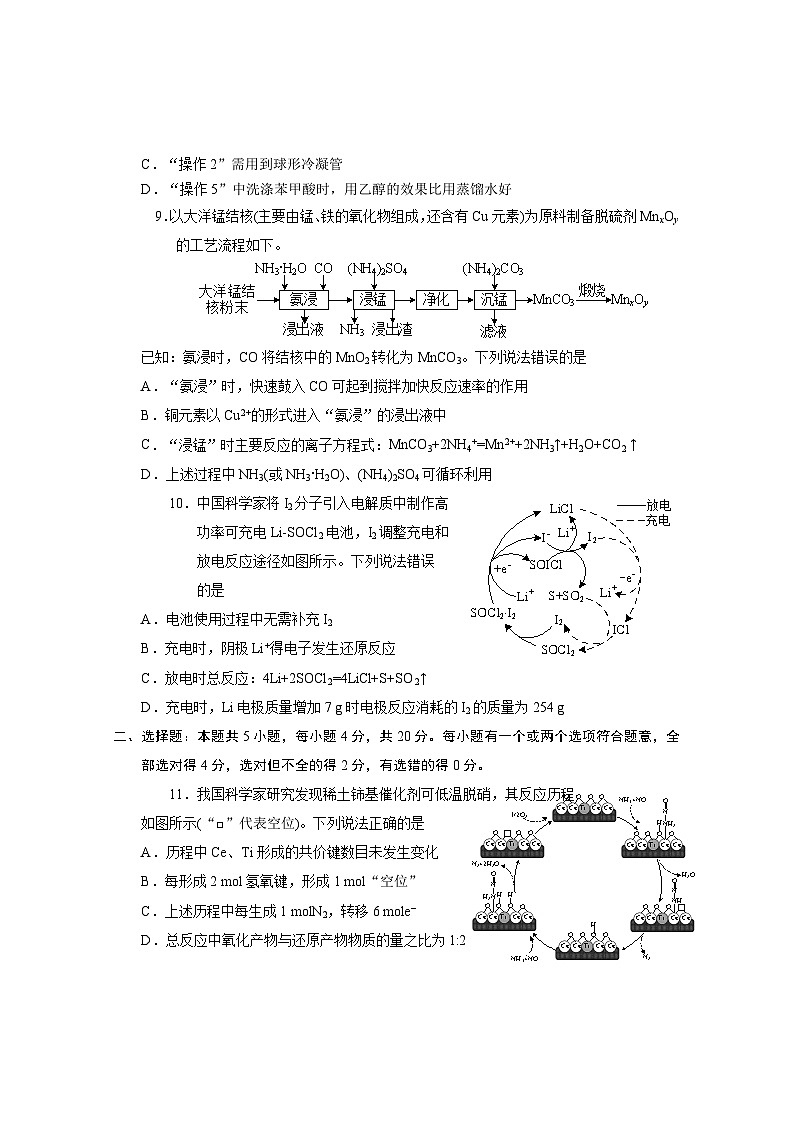
9.以大洋锰结核(主要由锰、铁的氧化物组成,还含有Cu元素)为原料制备脱硫剂MnxOy的工艺流程如下。
已知:氨浸时,CO将结核中的MnO2转化为MnCO3。下列说法错误的是
A.“氨浸”时,快速鼓入CO可起到搅拌加快反应速率的作用
B.铜元素以Cu2+的形式进入“氨浸”的浸出液中
C.“浸锰”时主要反应的离子方程式:MnCO3+2NH4+=Mn2++2NH3↑+H2O+CO2 ↑
D.上述过程中NH3(或NH3·H2O)、(NH4)2SO4可循环利用
10.中国科学家将I2分子引入电解质中制作高功率可充电Li-SOCl2电池,I2调整充电和放电反应途径如图所示。下列说法错误的是
A.电池使用过程中无需补充I2
B.充电时,阴极Li+得电子发生还原反应
C.放电时总反应:4Li+2SOCl2=4LiCl+S+SO2↑
D.充电时,Li电极质量增加7 g时电极反应消耗的I2的质量为254 g
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.我国科学家研究发现稀土铈基催化剂可低温脱硝,其反应历程
如图所示(“□”代表空位)。下列说法正确的是
A.历程中Ce、Ti形成的共价键数目未发生变化
B.每形成2 ml氢氧键,形成1 ml“空位”
C.上述历程中每生成1 mlN2,转移6 mle–
D.总反应中氧化产物与还原产物物质的量之比为1:2
12.Cpe重排反应如图所示,K()经Cpe重排反应可得到M。已知:羟基直接连在双键碳原子上不稳定会异构化成酮羰基或醛基。下列说法错误的是
A.Y中所有碳原子可能共平面
B.M的结构简式为
C.依据红外光谱可确证K、M存在不同的官能团
D.含酚羟基且有手性碳原子的M的同分异构体有9种(不考虑立体异构)
13.一种利用电化学富集锂的装置如图所示。富集锂的工作步骤如下:①接通电源1并向电极室2中通入海水,海水中的Li+进入MnO2结构而形成LixMn2O4,当电路中转移0.15 mle-时,43.5 gMnO2完全反应。②断开电源1接通电源2,停止通海水,使LixMn2O4中的Li+脱出进入电极室3。下列说法正确的是
A.x=0.6
B.惰性电极1与电源负极相连
C.离子交换膜b为阳离子交换膜
D.接通电源2后,MnO2电极的电极反应式为LixMn2O4+xe–=2MnO2+xLi+
14.将2 ml N2和6 ml H2通入2 L密闭容器中,分别在T1和T2温度下进行反应:N2(g)+3H2(g)2NH3(g) ΔH<0。下图曲线分别表示X的浓度(或Y的物质的量)随时间的变化(X、Y分别代表某一种反应物或生成物)。下列说法正确的是
A.X表示的物质是H2
B.T2温度下,该反应的平衡常数为
C.T2温度下,4~12 min的反应速率v(H2)=0.05 ml∙L–1∙min–1
D.T2温度下,反应达到平衡时容器内气体的压强较大
15.工业上常用H2S处理废水中的Ni2+和Cd2+,对其工艺条件进行研究。处理过程中始终保持H2S饱和,即c(H2S)=0.1 ml∙L–1。在一定pH范围内,溶液中HS–、S2–、Ni2+和Cd2+浓度的-lg(c/ml·L–1)随pH的变化关系如图。已知pH=2时溶液中仅有CdS沉淀生成,下列说法正确的是
A.X点:c(H+)>c(Cd2+)=c(S2–)
B.Ka2(H2S)=10–14.6 ml·L–1
C.m=9.2
D.反应Cd2+(aq)+HS–(aq)CdS(s)+H+(aq)的平衡常数K=10–11.4(ml·L–1)–1
三、非选择题:本题共5小题,共60分。
16.(12分)硫是组成生命的重要元素。回答下列问题:
(1)基态硫原子的价电子轨道表示式为 。
(2)广谱杀虫剂硫酰氟(SO2F2)常温常压下为无色气体,固态SO2F2的晶体类型为 ,S原子的轨道杂化方式为 ,其F-S-F键角 硫酰氯(SO2Cl2)中的Cl-S-Cl键角(填“>”或“<”),原因是 。
(3)硫代硫酸根(S2O32–)可看作是SO42–中的一个O原子被S原子取代的产物,S2O32–的空间结构是_____;工业上,S2O32–常作为配体与金属阳离子形成配合物,除O原子外可做配位原子的是 (填“中心”或“端基”)S原子。
(4)天然硫化铜俗称铜蓝,其晶胞结构如图。已知晶胞中含S22–,则一个晶胞中含有 个Cu2+,若阿伏伽德罗常数的值为NA,则该晶体的密度ρ=___g·cm–3(用含NA的代数式表示)。
17.(12分)工业上以富钒炉渣(主要含FeO·V2O3、V2O5和少量的SiO2、Al2O3等)为原料制备V2O5的工艺流程如下:
已知:①+ 5价钒元素在溶液中的存在形式与溶液pH的关系:
②Ksp[Fe(OH)3]=2.6×10–39;Ksp[Al(OH)3]=1.0×10–33;Ksp(NH4VO3)=1.6×10–3
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是 ;“高温氧化”过程中发生主要反应的化学方程式为 。
(2)滤渣1的主要成分为 ;“调pH”时需将Fe3+、Al3+除尽(浓度≤1×10–5 ml∙L–1时,可认为已除尽),需调节pH的范围为 。
(3)若“沉钒”前溶液中c(VO3–)=0.2 ml∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH4+)为 ml·L–1。过滤、洗涤、干燥得到NH4VO3沉淀,检验NH4VO3沉淀是否洗净的操作是 。
(4)“焙烧”时生成两种参与大气循环的无毒物质,则该反应的化学方程式为 。
18.(12分)环烷酸钴[(C5H9)(CH2)3COO]2C可作合成橡胶的催化剂,实验室以CCl2、环烷酸[C5H9(CH2)3COOH]等为原料制备环烷酸钴。回答下列问题:
= 1 \* ROMAN \* MERGEFORMAT I.CCl2的制备
实验室用如图实验装置制备纯净的CCl2(CCl2易潮解)。
(1)A中发生反应的离子方程式为 。
(2)B中盛放的试剂为__;图示装置存在一处缺陷会导致产品不纯,改进的措施是__。
(3)SOCl2遇水极易反应生成两种酸性气体,常作吸水剂。某实验小组设计用CCl2·6H2O和SOCl2反应制备无水CCl2,反应的化学方程式为______。
= 2 \* ROMAN \* MERGEFORMAT II.环烷酸钴的制备
控制温度90~95 ℃,向环烷酸中滴入一定浓度NaOH溶液,反应约2 h后,再加入一定浓度CCl2溶液,得到含有环烷酸钴的水溶液,分离提纯得环烷酸钴粗产品。
(4)实验中NaOH溶液的用量对环烷酸钴产率的影响如图所示,NaOH溶液过量导致环烷酸钴产率降低的原因是___。
= 3 \* ROMAN \* MERGEFORMAT III.环烷酸钴纯度的测定
步骤①:准确称取m g环烷酸钴产品,加入少量稀硫酸使其溶解,将溶液转移至250 mL容量瓶,定容。
步骤②:移取25.00 mL上述溶液于锥形瓶中,加入0.0500 ml∙L–1EDTA标准溶液25.00 mL。充分反应后,以铬黑T为指示剂,用0.0500 ml∙L–1锌标准溶液滴定过量的EDTA,消耗锌标准溶液5.00 mL。
已知:环烷酸钴摩尔质量为M g∙ml–1;EDTA与金属离子以1:1形成稳定配合物。
(5)产品中环烷酸钴的纯度为 (用含字母的式子表示)。下列情况会导致产品纯度测定值偏低的是 。
A.产品中存在[(C5H9)(CH2)3COO]3C B.步骤①中定容时俯视刻度线
C.步骤①中转移溶液时未洗涤烧杯 D.步骤②中滴定管未用锌标准溶液润洗
19.(12分)以麦芽酚为原料合成一种药物中间体M()的路线如下(部分反应条件或试剂略去):
已知:I.R1CHO+CH3-CR2=CHR3R1CHOHCH2CR2=CHR3
II.R1CH=CHR2R1COOH+R2COOH
(1)麦芽酚中含氧官能团的名称是 ;有机物Q是麦芽酚多一个碳原子的同系物,符合下列条件的Q的同分异构体有 种。
①遇FeCl3溶液显紫色 ②1 ml Q最多能与2 mlNa2CO3反应 ③含有六种化学环境的氢
(2)物质C可由A通过两步转化生成(A→中间产物→C),则中间产物的化学名称为 ;B的结构简式为 。
(3)D→E的反应类型为 ;K→L的化学方程式为 。
(4)根据上述信息,写出以乙二醇、2-丁烯为主要原料制备的合成路线。
20.(12分)利用1-甲基萘(1-MN)制备四氢萘类物质(MTLs,包括1-MTL和5-MTL)。反应过程中伴有生成1-甲基十氢萘(1-MD)的副反应,涉及反应如下。各反应的平衡常数K与温度T的关系如图所示。
回答下列问题:
(1)温度为T1时,反应Ⅱ的平衡常数与反应Ⅲ、Ⅳ的平衡常数之间的关系是K2= (用含K3、K4的代数式表示),曲线a、b中,表示反应Ⅳ的平衡常数随温度变化的曲线为 (填代号)。已知1-MTL比5-MTL稳定,则的数值范围是 (填标号)。
A.< -1 B.-1~0 C.0~1 D.>1
(2)以1ml 1-MN为原料,在1×103 kPa的高压H2氛围下反应(H2的压强近似等于总压),测得不同温度下达平衡时各产物的选择性Si(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数xi(xi表示物种i物质的量与除H2外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图所示。
反应温度为T2时,1-MN平衡转化率y=80%,则反应消耗H2的物质的量为 ,m= ,反应Ⅱ的分压平衡常数Kp= kPa–2。
(3)同温同压下,向温度为T2时的平衡体系中再充入H2,过程中保持H2的浓度不变,反应Ⅰ的化学平衡 (填“正向移动”“逆向移动”或“不移动”)。平衡时,1-MTL与5-MTL物质的量浓度之比c(1-MTL):c(5-MTL)=___。选项
操作和现象
结论
A
向漂白粉溶液中通入SO2,产生白色沉淀
酸性:H2SO3>HClO
B
常温下,分别测定1 ml·L–1CH3COONH4溶液和0.1 ml·L–1 CH3COONH4溶液的pH,测得pH都等于7
同温下,不同浓度CH3COONH4溶液中水的电离程度相同
C
10 mL 0.1 ml·L–1FeCl3溶液和10 mL 0.1 ml·L–1KI溶液充分反应后分成两等份,一份加入2滴KSCN溶液,溶液变红;另一份加入2滴淀粉溶液,溶液变蓝
FeCl3和KI的反应存在限度
D
向露置在空气中的Na2O2固体中加入稀盐酸,产生气泡
Na2O2固体已经变质
溶液pH
<1.0
1.0~4.0
4.0~6.0
6.0~8.5
8.5~13.0
>13.0
钒元素存在形式
VO2+
V2O5
多矾酸根
VO3–
多矾酸根
VO43–
备注
多矾酸盐在水中溶解度较小
70, 山东省烟台市2023-2024学年高二上学期期末考试化学试题: 这是一份70, 山东省烟台市2023-2024学年高二上学期期末考试化学试题,共21页。试卷主要包含了 PCl5晶体的晶胞结构如图, 某共价化合物结构如图等内容,欢迎下载使用。
14, 山东省烟台市2023-2024学年高二上学期期末考试化学试题: 这是一份14, 山东省烟台市2023-2024学年高二上学期期末考试化学试题,共2页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
14, 山东省烟台市2023-2024学年高二上学期期末考试化学试题(1): 这是一份14, 山东省烟台市2023-2024学年高二上学期期末考试化学试题(1),共9页。












