

江苏省常州市2024届高三上学期11月期中学业水平监测化学试题含答案
展开2023年11月
注意事项:
1.本试卷分为选择题和非选择题两部分,共100分。考试时间75分钟。
2.将选择题的答案填涂在答题卡的对应位置上,非选择题的答案写在答题卡的指定栏目内。
可能用到的相对原子质量:H1 C12 N14 O16 P31 K39 Fe56 Ag108 I127
一、单项选择题:共13小题,每题3分,共39分。每题只有一个选项最符合题意。
1.我国自主研发的“深地一号”为进军万米深度提供核心装备。制造钻头用的金刚石为( )
A.共价晶体B.离子晶体C.分子晶体D.金属晶体
2.易被氧化,与反应放出,需在保护下储存。下列说法正确的是( )
A.中N元素的化合价为-2B.键能大小:
C.分子的VSEPR模型为D.键角大小:
3.实验室制取的实验原理及装置均正确的是( )
A.制取B.干燥
C.收集D.吸收尾气中的
4.下列有关物质的工业制备反应不正确的是( )
A.合成氨:
B.制HCl:
C.制粗硅:
D.冶炼铝:
5.铁系超导材料Fe-Sm-As-F-O中基态Sm原子的价电子排布为。下列说法正确的是( )
A.Sm位于元素周期表中的f区B.Fe成为阳离子时先失去3d轨道电子
C.氢化物的稳定性:D.第一电离能:
阅读下列材料,完成6~8题:
碳元素及其化合物在自然界广泛存在且具有重要应用。碳元素能形成活性炭、金刚石、石墨、石墨烯等单质,也能形成、、、、葡萄糖、尿素、SiC等重要化合物;可做燃料,具有较大的燃烧热();尿素可用于消除污染。
6.下列说法正确的是( )
A.活性炭和使品红褪色的原理相同
B.1ml金刚石含C-C键数目约为
C.石墨烯是石墨的基本单元,两者互为同分异构体
D.等物质的量的和中所含σ键与π键的数目之比均为1:1
7.下列化学用语的表达正确的是( )
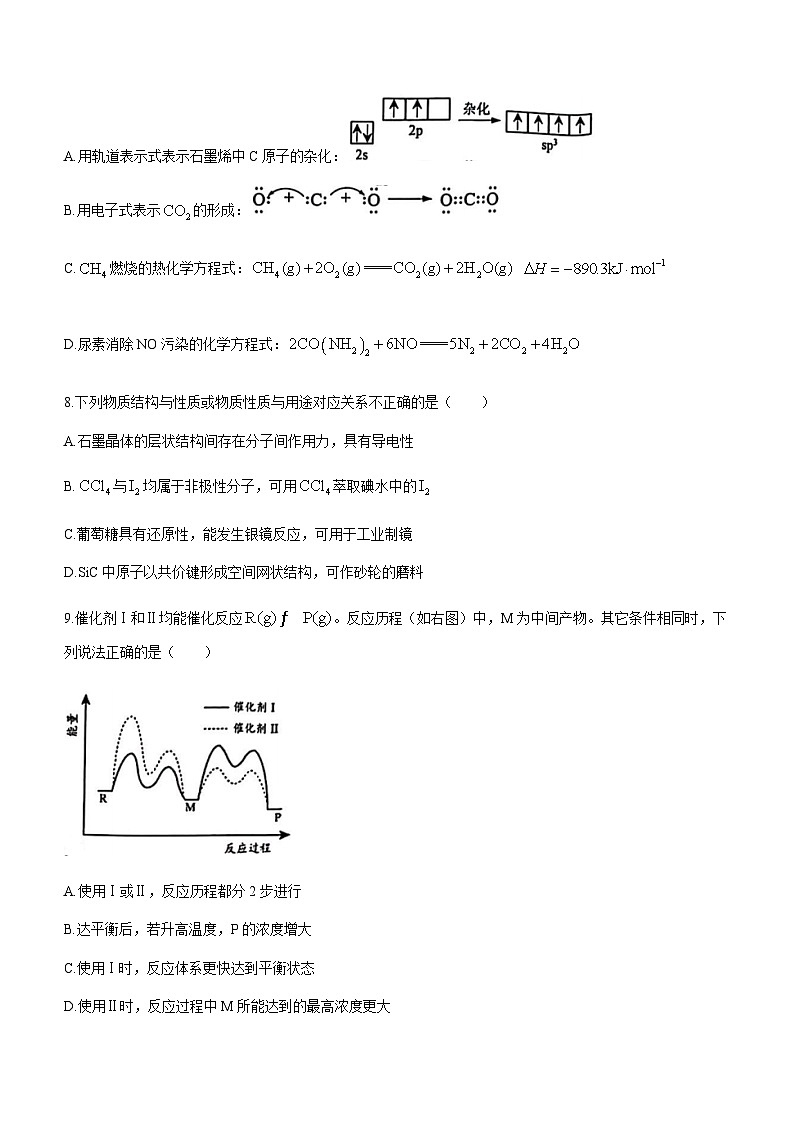
A.用轨道表示式表示石墨烯中C原子的杂化:
B.用电子式表示的形成:
C.燃烧的热化学方程式:
D.尿素消除NO污染的化学方程式:
8.下列物质结构与性质或物质性质与用途对应关系不正确的是( )
A.石墨晶体的层状结构间存在分子间作用力,具有导电性
B.与均属于非极性分子,可用萃取碘水中的
C.葡萄糖具有还原性,能发生银镜反应,可用于工业制镜
D.SiC中原子以共价键形成空间网状结构,可作砂轮的磨料
9.催化剂Ⅰ和Ⅱ均能催化反应。反应历程(如右图)中,M为中间产物。其它条件相同时,下列说法正确的是( )
A.使用Ⅰ或Ⅱ,反应历程都分2步进行
B.达平衡后,若升高温度,P的浓度增大
C.使用Ⅰ时,反应体系更快达到平衡状态
D.使用Ⅱ时,反应过程中M所能达到的最高浓度更大
10.直接无膜微流体燃料电池(结构如下图所示)利用多股流体在微通道内平行层流的特性,自然地将燃料和氧化剂隔开,无需使用传统燃料电池中的交换膜,且使用氧化剂可确保电池工作过程中无固体析出附着电极表面问题。下列有关说法不正确的是( )
A.电池工作时,电子由电极a直接经外电路流向电极b
B.电极a上发生的反应为
C.电极b上消耗时,理论上共转移3ml电子
D.上述无膜微流体技术可降低燃料电池的生产成本,提升电池工作性能
11.探究溶液的性质,下列实验方案不能达到探究目的是( )
12.室温下,通过下列实验探究溶液的性质。
实验Ⅰ:向溶液中滴加溶液。
实验Ⅱ:向溶液中滴加溶液。
已知:的电离常数,,,溶液混合后体积变化忽略不计。下列说法正确的是 ()
A.实验Ⅰ滴定达终点读数时,应双手一上一下持滴定管保证其竖直
B.实验Ⅰ滴定至溶液中时,至少大于10mL
C.实验Ⅱ初始阶段发生反应的离子方程式为
D.实验Ⅱ最后阶段发生反应(最简整数比)的化学平衡常数表达式为
13.工业上用和的高温气相反应制备苯硫酚(),其主要反应为
已知:高温下,热解形成和,与卤代苯中C-X的碳成键,首先形成中间体,反应速率较慢;中间体再迅速脱去,形成苯硫酚。
将的混合气以一定流速(反应停留时间45s)通过管式反应器,测得的转化率、与的产率随温度的变化如下图所示。
下列说法不正确的( )
A.图中曲线①表示的产率随温度的变化
B.反应中还可能存在二苯硫醚()等副产物
C.一定温度下,增大一定可提高的产率
D.保持其他条件不变,若改用作原料,可提高卤代苯的转化率
二、非选择题:共4题,共61分。
14.(15分)化学还原稳定法是当前水体污染修复领域的主要技术。废水中主要以和形式存在,化学还原稳定法去除水中主要包括铬的还原和固定两个过程。常用的化学还原剂包括硫系还原剂和铁系还原剂。
已知:,。
(1)是常用的硫系还原剂,在处理时自身转化为单质S。
①具有链状结构,其结构式可表示为________。
②经修复的水体pH明显________(填“增大”或“减小”),严重影响土壤及地下水的利用。
(2)铁系还原剂的还原效率虽不及硫化物,但有利于Cr的固定。
①在酸性溶液中,还原的离子方程式为________。
②Cr的固定途径有两个:其一是难溶性铬铁共沉淀氢氧化物或沉淀的生成;其二是________。
(3)试剂联用有望实现高效且稳定的修复效果。
①待各体系充分反应后,静置2h。实验测得分别使用单一试剂和试剂联用时,溶液中总Cr的去除率随溶液初始pH的变化关系如题14图-1所示。pH>9,随pH增大,试剂联用时溶液中总Cr的去除率上升的原因是________。
图1 图2
②在存在下,试剂联用处理溶液中,待体系充分反应,静置2h。测得浓度对溶液pH以及总Cr去除效果的影响关系如题14图-2所示。随浓度进一步增加,总Cr的去除率明显上升的原因是________。
③研究表明,试剂联用效果优于单一试剂主要是由于反应过程中生成了起催化作用的FeS。FeS的生成过程可用化学方程式表示为________。
15.(15分)银及其化合物在催化与电化学等领域中具有重要应用。
(1)一定条件下,在银催化剂表面存在反应:,该反应平衡时体系的压强()与温度(T)的关系如下表:
已知:在平衡体系中,用气体物质的分压替换浓度计算得到的平衡常数称为压强平衡常数,用表示。
气体物质X的分压。
①401K时,该反应的压强平衡常数________kPa。
②起始状态Ⅰ中有、Ag和,经下列过程达到各平衡状态:
已知状态Ⅰ和Ⅲ的固体质量相等,下列叙述正确的是________(填序号)。
A.从状态Ⅰ到状态Ⅱ的过程,
B.体系压强:
C.平衡常数:
D.若体积,则
请补全题15图-1的图像。________
图1
③某温度下,向恒容容器中加入,分解过程中反应速率与压强p的关系为,k为速率常数(一定温度下,k为常数)。当固体质量减少4%时,逆反应速率最大。
当转化率为14.5%时,________(用k表示)。
(2)固体离子导体α-AgI可通过加热γ-AgI制得。上述两种晶体的晶胞如题15图-2所示(省略了在晶胞中的位置)。
图1 图2
①测定晶体结构最常用的仪器是________。
②α-AgI与γ-AgI晶胞的体积之比为________。
③判定α-AgI中导电离子类型的实验装置如题15图-3所示。实验前,H型管内填充满a-AgI,竖管a和b(含a-AgI)的质量相同,两支Ag电极的质量也相同。通电一段时间后,可判定导电离子是而不是的实验数据是________。
16.(15分)氯化亚铁活化过一硫酸盐()可有效去除废水中的氨氮,同时回收磷资源。
(1)的结构如题16图所示。从物质结构角度分析,过一硫酸盐能在酸性溶液中直接将转化为的原因是________。
(2)活化产生三种主要的有效强氧化性自由基(、·OH和Cl·)。自由基对氨氮的去除具有一定的选择性,活化过程的主要反应机理如下:
、、
①酸性条件下,经氯化亚铁活化的过一硫酸盐可将废水中的转化为沉淀被全部回收。写出生成沉淀的离子方程式:________。
②研究表明,过一硫酸盐溶液中单独投加可将废水中的全部去除,但的去除率却很低。额外投加一定量NaCl后,和的去除率均达到100%。单独投加时,才去除率很低的可能原因是________。
(3)工业废水中浓度需达国家标准(小于)方可排放。准确量取20.00mL用氯化亚铁活化过一硫酸盐处理后的废水,依次加入缓冲溶液和溶液,使完全沉淀,过滤、洗涤。将所得沉淀完全溶解于盐酸中,用溶液滴定至终点(反应为),平行滴定三次,平均消耗溶液5.00mL。
通过计算确定此废水是否达到排放标准。________(写出计算过程)
(4)实验室用钛精矿酸浸废液(含及少量、和)制备。
已知:①经测定,废液中。有关金属离子沉淀的pH如下表:
②、、;
③当溶液中离子浓度小于,可视为该离子已沉淀完全。
为获得较高纯度的,请补充实验方案:向钛精矿酸浸废液中加入改性聚丙烯酰胺吸附溶液中的胶体杂质,静置一段时间后加入活性炭,________,冷却至15℃结晶,过滤,用乙醇洗涤晶体,低温真空烘干。
(实验中须使用的试剂有:HCl气体、NaOH溶液、NaF溶液;除常用仪器外须使用的仪器有:pH传感器、浓度传感器)
17.(16分)利用合成尿素是资源化的重要途径,可产生巨大的经济价值。
(1)20世纪初,工业上以和为原料在一定温度和压强下合成尿素,反应过程中能量变化如题17图-1所示。
图1
①反应物液氨分子间除存在范德华力外,还存在________(填作用力名称)。
②写出在该条件下由和合成尿素的热化学方程式:________。
(2)近年研究发现,电催化和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的溶液通入至饱和,经电解获得尿素,其原理如题17图-2所示。
图2
①电解过程中生成尿素的电极反应式为________。
②目前以和为原料的电化学尿素合成可达到53%的法拉第效率(FE%)。
已知:
其中,,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
则电解时阳极每产生标况下44.8L的,可获得尿素的质量为________。
(3)以尿素、甲醇和1,2-丙二醇(PG)为原料在催化精馏塔中可经“一锅法”制得碳酸二甲酯(DMC)。以Ca-Zn-Al氧化物为催化剂,先进行尿素与PG的醇解合成碳酸丙烯酯(PC)的反应,同时生成副产物;在不经产物分离和更换催化剂的情况下引入甲醇,再进行PC和甲醇的酯交换合成DMC的反应。
已知:液时空速是指每小时通过单位体积固体催化剂的液相反应物的体积;
回流比是指从精馏塔顶部返回的冷凝液流量与从顶部逸出的气态产品流量之比;产品收率=原料转化率×目标产物的选择性。
①PC合成。其他条件相同时,尿素与PG混合进料的液时空速对PC收率影响的关系如题17图-3所示。液时空速大于后,PC收率下降的原因是________。
图3 图4
②DMC合成。其他条件相同时,回流比对DMC收率影响关系如题17图-4所示。回流比大于9时,DMC收率下降的原因是________。
③请从原子经济性的角度对上述“一锅法”提出合理的优化建议:________。
常州市2024届高三上学期11月期中学业水平监测
化学参考答案
2023年11月
一、单项选择题:共13小题,每题3分,共39分。每题只有一个选项最符合题意。
1.A 2.B 3.D 4.D 5.A 6.B 7.D 8.A 9.C 10.C 11.B 12.D 13.C
二、非选择题:共4题,共61分。
14.(15分)
(1)①(2分)
②增大(2分)
(2)①(2分)
②水解产生的胶体吸附或(2分)
(3)①pH增大,使用会抑制的还原,降低总Cr去除率;但使用有利于的固定,提高总Cr去除率;试剂联用时,的用量大于,增大pH,对总Cr去除率的影响程度大于(3分)
②增大浓度,溶液pH减小,试剂联用时低pH值有利于的去除(2分)
③(2分)
15.(15分)
(1)①10(2分)
②AC(2分)
(2分)
图1
③0.75k(2分)
(2)①X射线衍射仪(2分)
②7:12(3分)
③竖管a和b的质量均不变(2分)
16.(15分)
(1)过一硫酸盐中存在O-O键,具有强氧化性(2分)
(2)①(2分)
②Cl·对去除具有最高的选择性。单独投加时,浓度较小,导致产生的Cl·量也较少,不足以将完全氧化(2分)
(3)根据题意可得关系式:
浓度
故此废水达到排放标准(3分)
(4)搅拌后静置过滤,向滤液中边搅拌边滴加NaOH溶液,至pH传感器显示pH值在4.7~6.3之间,静置过滤,向滤液中边搅拌边滴加NaF溶液,至浓度传感器显示在,过滤,将滤液在HCl气体氛围中蒸发浓缩(6分)
17.(16分)
(1)①分子间氢键(2分)
② (3分)
(2)①(2分)
②15.9g(3分)
(3)①液时空速过大,原料在催化精馏塔中停留时间短,导致反应不充分(2分)
②大量冷凝液流回精馏塔内,使DMC无法及时移出反应体系,从而抑制DMC合成反应的正向进行(2分)
③将生成的副产物与反应合成尿素,进行循环利用(2分)选项
探究目的
实验方案
A
是否水解
测定溶液的pH值
B
能否催化分解
向2mL1.5%的溶液中滴加5滴溶液,观察气泡产生情况
C
是否具有氧化性
向溶液中通入一定量的HI气体,观察实验现象
D
能否形成配位键
向溶液中,边振荡边滴加过量浓氨水,观察实验现象
T/K
401
443
463
10
51
100
氢氧化物
开始沉淀的pH
6.3
3.4
11.9
7.7
完全沉淀的pH
8.3
4.7
13.9
9.8
江苏省常州市2023-2024学年高三上学期期末学业水平监测试题 化学 Word版含答案: 这是一份江苏省常州市2023-2024学年高三上学期期末学业水平监测试题 化学 Word版含答案,共11页。试卷主要包含了下列说法不正确的是,下列有关反应原理表述正确的是,氮及其化合物的转化具有重要应用等内容,欢迎下载使用。
江苏省常州市教育学会2023-2024学年高一上学期1月学业水平监测(期末考试)化学试题(PDF版含答案): 这是一份江苏省常州市教育学会2023-2024学年高一上学期1月学业水平监测(期末考试)化学试题(PDF版含答案),共8页。
江苏省常州市2023-2024学年高三上学期1月学业水平监测(期末)化学试卷(扫描版含答案): 这是一份江苏省常州市2023-2024学年高三上学期1月学业水平监测(期末)化学试卷(扫描版含答案),文件包含江苏省常州市2023-2024学年高三上学期期末监测化学试卷pdf、20232024学年高三期末调研化学答案pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。












