

广东省六校(东莞中学、广州二中、惠州一中、深圳实验、珠海一中、中山纪念中学)2023-2024学年高三上学期第一次联考化学试题
展开2024 届高三第一次六校联考试题
化 学
(满分 100 分 考试时间 75 分钟)
注意事项:
1.答题前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名和考生号、考场号、座位号填写在答题卡上。并用 2B 铅笔将对应的信息点涂黑,不按要求填涂的,答卷无效。
2.选择题每小题选出答案后,用 2B 铅笔把答题卡上对应题目选项的答案信息点涂黑,如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案,不准使用铅笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束后,只需将答题卡交回。
可能用到的相对原子质量:H 1 C 12 O 16 Ce 140
一、单项选择题:本题共 16 小题,共 44 分。第 1~10 小题,每小题 2 分;第 11~16 小题,每 小题 4 分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.中华文明源远流长,现代科技也迅猛发展。下列有关我国文明和科技的说法中不涉及化学变化的是
2.“探索浩瀚宇宙,发展航天事业,建设航天强国,是我们不懈追求的梦。”航天科技的发展与化学密切相关。下列说法不正确的是
A.神舟十四号飞船外壳使用的氮化硅陶瓷属于新型无机非金属材料
B.航天飞船内安装盛有过氧化钠颗粒的装置,它的用途是再生氧气
C. 航天服壳体使用的铝合金材料因熔点比纯铝高而耐用
D.中国空间站存储器所用的材料石墨烯与金刚石互为同素异形体
3.已知反应:RC≡CAg+ 2CN- +H2O→RC≡CH + Ag(CN)2- + OH-,该反应可用于提纯炔烃。下列说法不正确的是( )
A.CN-的电子式为 B.O 的价电子排布图为
C. H2O 的空间充填模型为 D.[Ag(CN)2]— 中σ键与π键的个数比为 1∶1
4.药物“异博定”能有效控制血压升高、促进血液循环,其合成路线中有如下转化过程。下列说法中正确的是 更多优质滋源请 家 威杏 MXSJ663
A.X 分子最多有 15 个原子共平面
B.用酸性高锰酸钾能检验 Z 中是否含有 Y
C.等物质的量的 X、Y、Z 消耗的 NaOH 的物质的量相等
D.一定条件下,X 可与 HCHO 发生缩聚反应
5.金属腐蚀对国家经济造成的损失非常严重,了解金属的腐蚀与防护具有重要意义。下列说法正确的是
A.白铁(镀锌铁)比马口铁(镀锡铁)更耐腐蚀
B.燃气灶中心部位的铁生锈发生的主要是电化学腐蚀
C.将钢闸门连接到直流电源的负极加以保护是牺牲阳极的阴极保护法
D.把金属制成防腐的合金(如不锈钢),应用的是电化学保护法
6.树立正确的劳动观念,积极参加劳动是全面发展的重要内容。下列劳动项目涉及的化学知识正确的是
7.下列说法错误的是
A. Mg、Fe 在一定条件下都能与水反应生成 H2和相应的碱
B. 稀硫酸中加入铜粉,铜粉不溶解,若再继续加入 KNO3固体,铜粉会溶解
C. 已知 Na3N 与盐酸反应生成 NaCl 和 NH4Cl,则 Mg3N2与盐酸反应生成 MgCl2和NH4Cl
D. 25℃时,pH 为 10 的 Na2CO3溶液中水电离出的 H+的物质的量浓度为 1.0×10 -4 ml/L
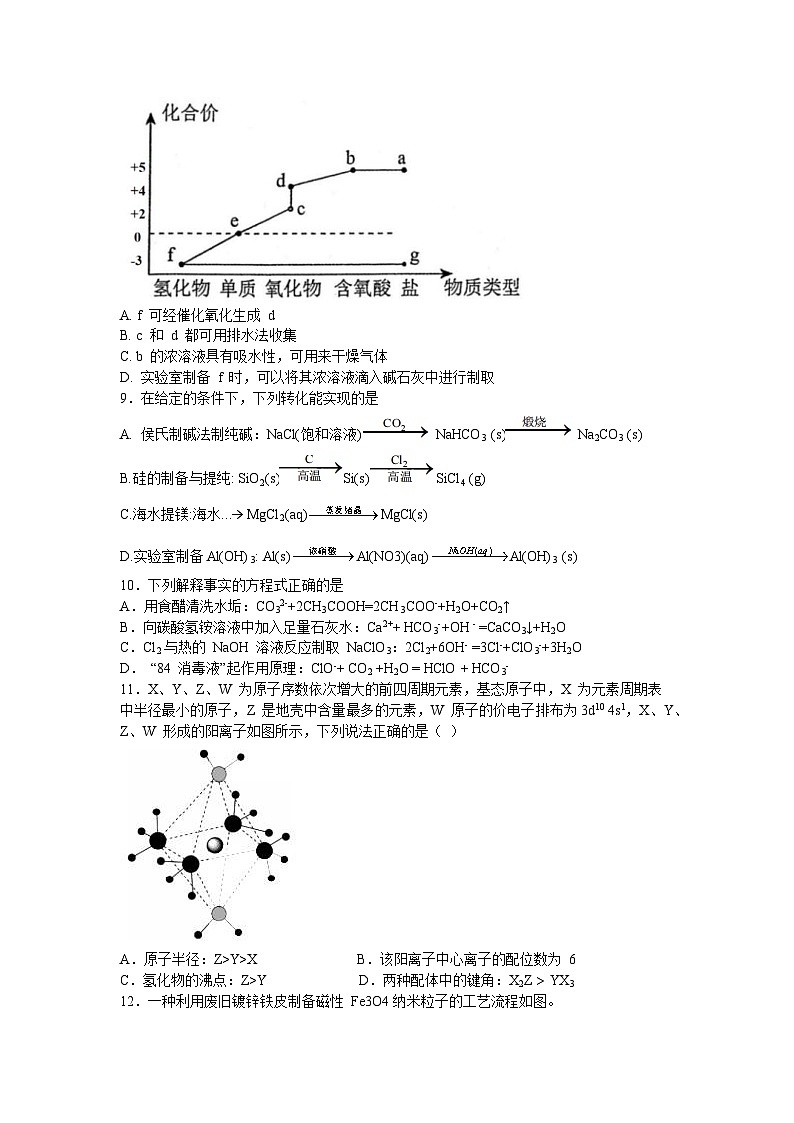
8. 如图是某元素的价—类二维图。其中正盐 g 与 NaOH 反应可生成 f,d 的相对分子质量比 c 大 16。下列说法正确的是
A. f 可经催化氧化生成 d
B. c 和 d 都可用排水法收集
C. b 的浓溶液具有吸水性,可用来干燥气体
D. 实验室制备 f 时,可以将其浓溶液滴入碱石灰中进行制取
9.在给定的条件下,下列转化能实现的是
A. 侯氏制碱法制纯碱:NaCl(饱和溶液) NaHCO3 (s) Na2CO3 (s)
B.硅的制备与提纯: SiO2(s)Si(s)SiCl4 (g)
C.海水提镁:海水...→ MgCl2(aq)MgCl(s)
D.实验室制备Al(OH)3: Al(s)Al(NO3)(aq)Al(OH)3 (s)
10.下列解释事实的方程式正确的是
A.用食醋清洗水垢:CO32-+2CH3COOH=2CH3COO-+H2O+CO2↑
B.向碳酸氢铵溶液中加入足量石灰水:Ca2++ HCO3-+OH - =CaCO3↓+H2O
C.Cl2与热的 NaOH 溶液反应制取 NaClO3:2Cl2+6OH- =3Cl-+ClO3-+3H2O
D. “84 消毒液”起作用原理:ClO-+ CO2 +H2O = HClO + HCO3-
11.X、Y、Z、W 为原子序数依次增大的前四周期元素,基态原子中,X 为元素周期表中半径最小的原子,Z 是地壳中含量最多的元素,W 原子的价电子排布为3d10 4s1,X、Y、Z、W 形成的阳离子如图所示,下列说法正确的是( )
A.原子半径:Z>Y>X B.该阳离子中心离子的配位数为 6
C.氢化物的沸点:Z>Y D.两种配体中的键角:X2Z YX3
12.一种利用废旧镀锌铁皮制备磁性 Fe3O4纳米粒子的工艺流程如图。
下列有关说法不正确的是( )
A. “氧化”时发生反应的离子方程式为 2Fe 2+ + ClO − + 2H + = 2Fe 3+ + Cl− + H2O
B. “氧化”后的溶液中金属阳离子主要有 Fe 2+、Fe 3+、Na+
C. 用激光笔照射“加热沉铁”后所得分散系,产生丁达尔效应
D. “分离”时采用的方法是过滤
13.下列实验方案合理的是
14.向 1L 刚性容器中投入 aml A (g) 与 M (s) (足量)发生反应:M (s) + 5A (g) ⇌ 5B (g) + N (s) (相对分子质量: M 大于 N)。测得不同温度下 B (g) 体积分数φ (B)随时间 t 的变化曲线如图所示。下列说法正确的是
A.0~t1min 内,v(N)=0.14at1ml·L-1·min -1
B.温度升高,容器内气体的密度减小
C.T1℃,再投入 aml A(g),平衡时 n(A)=0.7a ml
D.由图上信息可知:T2>T1
15.某课题组以纳米 Fe2O3作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图所示),下列说法不正确的是
A.充电时,Fe2O3对应电极连接充电电源的负极
B.该电池的正极的电极反应式:Fe2O3+6Li++6e −=3Li2O+2Fe
C.该电池不能使用氢氧化钠溶液作为电解液
D.该电池工作的原理:放电时,Fe2O3作为电池正极被还原为 Fe,电池被磁铁吸引
16.常温下,体积和浓度一定的 NaA 溶液中各微粒浓度的负对数(−lgc)随溶液 pH 的变化关系如图所示。下列叙述正确的是
A.曲线②表示−lgc(OH −)随溶液 pH 的变化情况
B.等物质的量浓度 NaA 和 HA 混合溶液:c(Na+) > c(A−) >c(OH−)>c(H+)
C.HA 的Ka的数量级为10 −5
D.常温下,将 M 点对应溶液加水稀释,c(A−)c(HA)不变
二、非选择题:共 56 分
17.(14 分)某小组对 Cu 和 H2O2的反应进行相关实验探究。
【实验探究】实验 i:向装有 0.5g Cu 的烧杯中加入 20mL30%H2O2溶液,一段时间内无明显现象,10 小时后,溶液中有少量蓝色浑浊,Cu 片表面附着少量蓝色固体。
(1)写出该反应的化学方程式: .
【继续探究】针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验 ii 中:溶液变蓝的原因是 (用离子反应方程式表示);经检验产生的气体为氧气,产生氧气先慢后快的原因是
(不考虑温度的影响)。
(3)对比实验 i 和 iii,为探究氨水对Cu 的还原性或H2O2 氧化性的影响,该同学利用如图装置继续实验。
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K 闭合时,电压为 x。
b.向 U 型管右侧溶液中滴加氨水后,电压不变。
c.继续向 U 型管左侧溶液中滴加氨水后,电压增大了 y。
①解释步骤 c 中电压增大的原因: 。
②若向 U 型管左侧溶液中滴加硫酸后,电压不变,继续向 U 型管右侧溶液中滴加硫酸后,电压增大了 z。则可以得出的结是: .。
(4) 基于以上实验,影响 Cu 与 H2O2反应的因素有 。(任写一条)
(5) 结合上述实验,下列说法正确的是 .
A. 电化学是研究物质氧化性、还原性的重要手段之一
B. 实验 ii 中发生的反应中,H2O2只体现氧化性
C.在还原反应(氧化反应)中,增大反应物浓度或降低生成物浓度,氧化剂(还原剂)的氧化性(还原性)增强
18.(14 分)Ce2(CO3)3可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以 CePO4形式存在,还含有 SiO2、Al2O3、Fe2O3、CaF2等物质。以独居石为原料制备 Ce2(CO3)3•nH2O 的工艺流程如图:
已知:①常温下,H2CO3的 Ka1=4.5×10﹣7,Ka2=4.7×10﹣11 , Ksp[Ce2(CO3)3]=1.0×10 -28;
②Ce 3 +易被氧化为 Ce 4+。 回答下列问题:
(1)基态Fe 2+的价层电子排布式为 ;
(2)为提高“焙烧”效率,可采取的措施有 (写一条即可);
(3)滤渣 III 的主要成分是 (填化学式) ;
(4)“沉铈”过程中,Ce 3+恰好沉淀完全[c(Ce 3+ )为 1.0×10 -5ml/L]时溶液的 pH 为 5,则溶液中c(HCO3 -)=_______ ml/L(保留两位有效数字)。
(5)滤渣Ⅱ的主要成分为 FePO4,在高温条件下,Li2CO3、草酸(H2C2O4)和 FePO4可制备电极材料 LiFePO4,同时生成 CO2和 H2O,该反应的化学方程式为
。
(6) 为测定产品中 Ce 3+的含量,取 2.00g 产品加入氧化剂将 Ce 3+完全氧化并除去多余氧化剂后,用稀硫酸酸化,配成 100.00mL 溶液,取 25.00mL 溶液用 0.10ml/L 的 FeSO4溶液滴定至终点(铈被还原成 Ce 3+),消耗 FeSO4溶液 20.00mL,则产品中 Ce 3+的质量分数为 。
(7)碳酸铈经高温煅烧可获得纯净的 CeO2,二氧化铈晶体结构类似萤石结构,其晶胞结构如图所示,设阿伏伽德罗常数的值为 NA,该立方晶胞的参数为 a nm,求该晶胞密度
g·cm-3(用含 NA的代数式表示,Ce 的相对原子质量为 140)。
氧化铈晶胞图
19.(14 分)甲烷、甲醇(CH3OH)、甲醛(HCHO)等含有一个碳原子的物质称为“一碳”化合物,广泛应用于化工、医药、能源等方面,研究“一碳”化合物的化学称为“一碳”化学。
(1)已知:①CO2 (g)+H2 (g)CO(g)+H2O(g) △H1= +41 kJ/ml
②CO(g)+2H2 (g)CH3OH(g) △H2= -90 kJ/ml
根据盖斯定律,反应CO2 (g)+3H2 (g)CH3OH(g)+H2O(g)的△H=_ kJ·ml-l,
反应能在___________(填“高温”或“低温”)自发进行。
(2)工业上合成甲醇的反应:CO(g)+2H2(g)CH3OH(g) ,在一个密闭容器中,充入 1ml CO 和 2ml H2发生反应,测得平衡时 H2的体积分数与温度、压强的关系如图所示。
压强 P1_____P2(填“大于”或“小于”),该反应达到平衡的标志是______(填标号)。
A.反应速率 v正(H2)=2v逆(CH3OH) B.容器内 CO 和 H2物质的量之比为 1:2
C.混合气体的质量不再变化 D.混合气体的平均摩尔质量不再变化
(3)我国科学家制备了一种 ZO-ZrO2催化剂,实现 CO2高选择性合成 CH3OH。气相催化合成过程中,CO2转化率(x)及 CH3OH 选择性(s)随温度的变化曲线如图。据此回答:
①生成 CH3OH 的最佳温度约为___________。
②温度升高,CO2转化率升高,但产物 CH3OH 含量降低的原因:____ 。
(4) 对于气体参与的反应如反应④[2CH3OH(g)⇌ C2H4(g)+2H2O(g),△H<0],可以用某组分的压强(Pa)变化来表示化学反应速率,在温度和体积不变的密闭容器中充入一定量的CH3OH
气体发生反应④,在 10 分钟内,容器的压强由 x kPa 升高到 y kPa,则这段时间该反应的化学反应速率v(C2H4)=______ kPa•min﹣1。该反应的速率方程式为 v正=k正•p 2(CH3OH),v逆=k逆•p 2(H2O)p(C2H4),k正、k逆表示速率常数,与温度、活化能有关。升高温度,k正的变化程度 _______(填“大于”、“小于”或“等于”)k逆的变化程度。
20. (14 分)普瑞巴林能用于治疗多种疾病,结构简式为,其合成路线如下:
(1)化合物 B 的命名为___________;F 分子中含氧官能团的名称为___________。
(2)D→E 反应的条件为___________,F→G 的反应类型为_______。
(3)在右图用“*”标出 G 化合物中的手性碳原子。
(4)在加热条件下,G 在 LiOH 水溶液中发生的化学反应方程式是___________。
(5)符合下列条件的同分异构体,共有___________种。
ⅰ、和 E 互为同系物,且比 E 相对分子质量少 14;
ⅱ、能发生银镜反应,且有机物和 Ag 的物质的量之比等于 1:4;
其中核磁共振氢谱中有三组峰且峰面积比为 3:1:1 的是___________(写结构简式)。
(6)已知:酚不容易与羧酸反应生成酚酯,可以用ⅱ反应制取酚酯。
ⅰ、
ⅱ、
参考以上合成路线及反应条件,以、和必要的无机试剂为原料,合成,写出路线流程图。
{#{QQABaYKUggAAAhAAARgCUQWACECQkAGAACgOwFAMAAASAFABAA=}#}
广东省东莞中学、广州二中、惠州一中、深圳实验、珠海一中、中山纪念中学2024届高三第四次六校联考化学试卷(PDF版附答案): 这是一份广东省东莞中学、广州二中、惠州一中、深圳实验、珠海一中、中山纪念中学2024届高三第四次六校联考化学试卷(PDF版附答案),文件包含广东省东莞中学广州二中惠州一中深圳实验珠海一中中山纪念中学2024届高三第四次六校联考化学pdf、广东省东莞中学广州二中惠州一中深圳实验珠海一中中山纪念中学2024届高三第四次六校联考化学答案pdf等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。
2024东莞中学、广州二中、惠州一中、深圳实验、珠海一中、中山纪念中学高三上学期第三次六校联考试题化学含答案: 这是一份2024东莞中学、广州二中、惠州一中、深圳实验、珠海一中、中山纪念中学高三上学期第三次六校联考试题化学含答案,文件包含广东省东莞中学广州二中惠州一中深圳实验珠海一中中山纪念中学2024届高三第三次六校联考化学docx、广东省东莞中学广州二中惠州一中深圳实验珠海一中中山纪念中学2024届高三第三次六校联考化学答案docx等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。
广东省六校(东莞中学、广州二中、惠州一中、深圳实验、珠海一中、中山纪念中学)2024届高三上学期第一次联考化学: 这是一份广东省六校(东莞中学、广州二中、惠州一中、深圳实验、珠海一中、中山纪念中学)2024届高三上学期第一次联考化学,共19页。












