
山东省潍坊市2023-2024学年高三上学期12月月考化学模拟试题(含答案)
展开可能用到原子量:H 1 C 12 N 14 Zn 65 Mn 55 As75
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1. 下列实验中, 物质的颜色变化与氧化还原反应无关的是
A. 苯酚露置在空气中,无色晶体变成粉红色
B. 向酸性K2Cr2O7溶液中加入NaOH 溶液, 溶液由橙色变为黄色
C. 用 FeCl3溶液浸泡腐蚀铜电路板,溶液由黄色变为蓝绿色
D. 向新制的Cu(OH)2中加入乙醛溶液,加热,有砖红色沉淀生成
2. 化学与生产、生活密切相关。下列说法中正确的个数有( )
①CuSO₄溶液用于除去乙炔中的 H2S,是因为 CuS 难溶;②ClO₂既可用于自来水的消毒杀菌,又可除去水中的悬浮杂质;③废旧电池必须回收处理,防止造成汞、镉及铅等重金属污染;④CaF₂与浓H2SO4糊状混合物可用于刻蚀玻璃; ⑤NaOH 是强碱, 因此钠盐的水溶液不会呈酸性;⑥溶洞的形成主要源于溶解CO2的水对岩石的溶蚀作用;⑦面包师用小苏打作发泡剂烘焙面包是依据碳酸钠与酸反应的原理
A.2项 B.3 项 C.4项 D.5 项
3. 叠氮化钠与氢气在催化剂作用下发生反应:。生成的氮化钠(Na3N)不稳定、易水解,下列说法错误的是( )
A. Na3N 与盐酸反应可生成两种盐
B. 题干方程式所列四种物质中属于电解质的有Na3N 与NaN3
C.Na3N 与NaN3中阴离子和阳离子个数比分别为1∶3和3∶1
D. 当生成NH3的体积为89.6L(标准状况下)时,反应转移了12ml e-
4. NA代表阿伏加德罗常数的值,下列说法正确的是( )
A. 25℃,101KPa下,11.2LSO2中所含氧原子个数小于NA
B. 常温下,1L pH=l的H2SO4溶液中的H+数目为0.2NA
C. 0.05ml·L-1 NaHSO4溶液中,阳离子的数目之和为0.1NA
D. 含0.2ml HCl的浓盐酸与足量MnO2反应,生成Cl2的个数为0.1NA
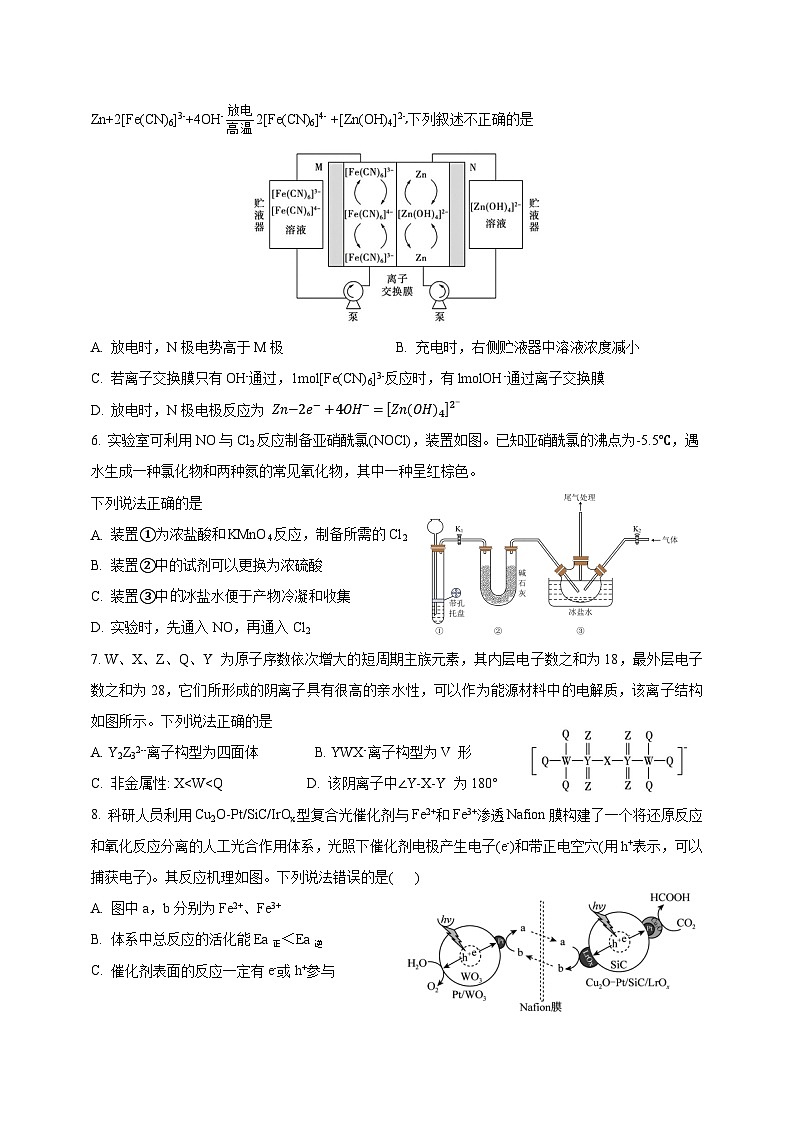
碱性锌铁液流电池具有电压高、成本低的优点。该电池的总反应为
Zn+2[Fe(CN)6]3-+4OH-2[Fe(CN)6]4- +[Zn(OH)4]2-,下列叙述不正确的是
A. 放电时,N极电势高于M极 B. 充电时,右侧贮液器中溶液浓度减小
C. 若离子交换膜只有OH-通过,1ml[Fe(CN)6]3-反应时,有lmlOH-通过离子交换膜
D. 放电时,N极电极反应为 Zn−2e−+4OH−=ZnOH42−
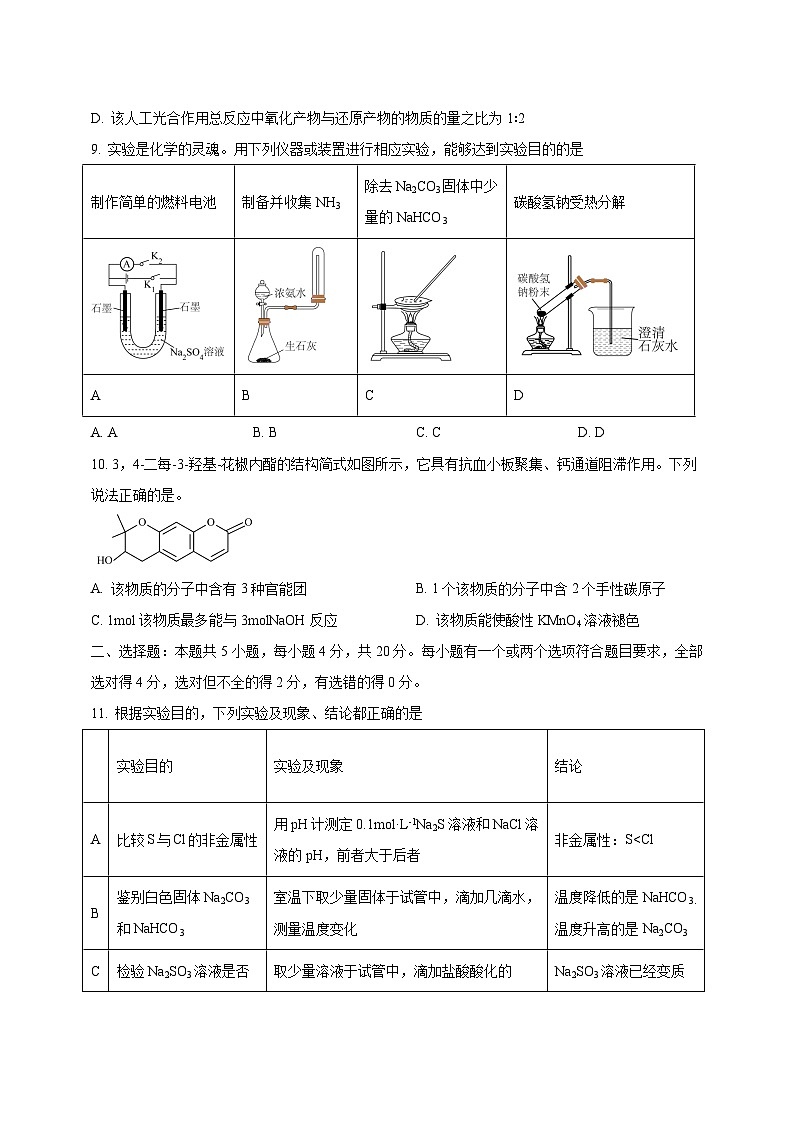
6. 实验室可利用NO与Cl2反应制备亚硝酰氯(NOCl),装置如图。已知亚硝酰氯的沸点为-5.5℃,遇水生成一种氯化物和两种氮的常见氧化物,其中一种呈红棕色。
下列说法正确的是
装置①为浓盐酸和KMnO4反应,制备所需的Cl2
B. 装置②中的试剂可以更换为浓硫酸
C. 装置③中冰盐水便于产物冷凝和收集 D. 实验时,先通入NO,再通入Cl2
7. W、X、Z、Q、Y 为原子序数依次增大的短周期主族元素,其内层电子数之和为18,最外层电子数之和为28,它们所形成的阴离子具有很高的亲水性,可以作为能源材料中的电解质,该离子结构如图所示。下列说法正确的是
A. Y2Z32--离子构型为四面体 B. YWX-离子构型为V 形
C. 非金属性: X
A. 图中a,b分别为Fe2+、Fe3+
B. 体系中总反应的活化能Ea正<Ea逆
C. 催化剂表面的反应一定有e-或h+参与
D. 该人工光合作用总反应中氧化产物与还原产物的物质的量之比为1∶2
9. 实验是化学的灵魂。用下列仪器或装置进行相应实验,能够达到实验目的的是
A. AB. BC. CD. D
10. 3,4-二每-3-羟基-花椒内酯的结构简式如图所示,它具有抗血小板聚集、钙通道阻滞作用。下列说法正确的是。
A. 该物质的分子中含有3种官能团B. 1个该物质的分子中含2个手性碳原子
C. 1ml该物质最多能与3mlNaOH反应D. 该物质能使酸性KMnO4溶液褪色
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11. 根据实验目的,下列实验及现象、结论都正确的是
12. 利用工业废气NO生产NH4NO3的流程如图所示。已知装置I和装置II反应后溶液中n(NO):n(NO)都为1:1。下列说法错误的是
A. 装置I中反应为2NO+4Ce4++3H2O=4Ce3++NO+NO+6H+
B. 装置I中若有5.6L(标准状况)NO参与反应,则转移1ml电子
C. 装置III中氧化剂和还原剂的物质的量之比为1:2
D. 装置III中NH3和O2的体积比3:1时,可实现原子利用率最大化
13. 有关物质A可发生如图所示转化过程。下列说法不正确的是
A. A→C的反应类型属于氧化反应 B. A 与H2完全加成的产物有9种不同化学环境的氢原子
C. B的结构简式为: D. 1ml D与溴水反应,消耗 3mlBr₂
14. B2O3的气态分子结构如图1所示,硼酸( H3BO3)晶体结构为层状,其二维平面结构如图2所示。下列说法错误的是
两分子中B原子分别采用 sp杂化、sp²杂化
B.1mlH3BO3晶体中含有6ml氢键
C. 硼酸晶体中层与层之间存在范德华力
D. 硼原子可提供空轨道,硼酸电离的方程式为:H3BO3+H2O=[B(OH)4]-+H+
15.马来酸(用H2B表示)是一种二元弱酸,25°C时,某混合溶液中c(H2B)+c(HB﹣)+c(B2﹣)=0.1ml•L﹣1,测得H2B、HB﹣、B2﹣及OH﹣等离子的pC(pC=﹣lgc)随溶液pH的变化关系如图所示。,下列说法正确的是( )
A.该温度下,马来酸的电离平衡常数Ka1=10﹣1.92
B.当溶液中lg=2时,pH=3.15
C.pH=7时,溶液中c(B2﹣)>c(H2B)>c(HB﹣)>c(OH﹣)
D.混合溶液中c(HB﹣)=
三、非选择题:本题共5小题,共60分。
16.硼、砷、铁等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。 回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是 (填标号,下同),用光谱仪可捕捉到发射光谱的是 。
同周期中第一电离能大于砷的元素有 种。CH3As(OH)2与CH3AsOH两种含砷有机酸中沸点较高的是 (填化学式), 原因为 。
(3)LiZnAs 晶体的立方晶胞结构如图1 所示,N 点原子分数坐标为 341414; LiZnAs 晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体LiZnmMnnAs, 其立方晶胞结构如图2所示。
①M 点原子分数坐标为 。
②m=
③已知 NA为阿伏加德罗常数的值, LiZnmMnnAs的摩尔质量为M g·ml-1, 晶体密度为d g·cm-3。晶胞中 As原子与 Mn 原子之间的最短距离为 nm(列出计算式)。
4FeSO4·7H2O的结构如图所示。
图示FeSO4·7H2O结构中键角1、2、3由大到小的顺序是 (填序号)。
17. 分析化学滴定法有酸碱中和滴定、沉淀滴定、络合滴定、氧化还原滴定等。沉淀滴定法可用于 NaCl溶液中 c(Cl⁻)的测定。实验过程包括准备标准溶液和滴定待测溶液。
已知: ①Ag2CrO₄是一种砖红色沉淀;
②已知: Ksp(AgCl)=1.56x10-10(ml·L-1)2 , Ksp(Ag2CrO4)=1.1x10-12(ml·L-1)3
③AgCl + 2NH3 = [Ag(NH3)2]+ + Cl-
Ⅰ. 准备标准溶液: 准确称取 AgNO₃基准物4.2468g(0.0250ml)后, 配制成250mL 标准溶液,放在棕色试剂瓶中避光保存,备用。
Ⅱ. 滴定待测溶液。其主要步骤如下:
a. 取待测 NaCl溶液25.00 mL于锥形瓶中; b. 加入 1mL5%K2CrO4溶液;
c. 在不断摇动下用AgNO3标准溶液滴定,当接近终点时,需逐滴加入AgNO3溶液,并用力振荡。记下终点时消耗AgNO3标准溶液的体积;
d. 重复上述操作两次。三次测定数据如下表:
e. 数据处理。 回答下列问题:
①滴定前,装有AgNO3标准液的滴定管排气泡时,应选择右图中
的 (填序号)。
②读取盛装标准AgNO3的滴定管初始读数。若液面位置如图所示,则此时读数为 mL。
(2)将称得的AgNO3配制成标准溶液。所使用的仪器除烧杯和玻璃棒外还有 。
(3)滴定终点的现象是 。
(4) 测得c(Cl⁻)= ml·L⁻¹。
(5)若用该方法测定NH4Cl溶液中的c(Cl⁻),待测液的pH不宜超过7.2,理由是 。
(6)下列关于实验的说法合理的是 (填序号)。
A. 滴定过程中可用蒸馏水将锥形瓶壁上粘附的溶液冲下
B. 为使终点现象更加明显,可改加1mL10%K2CrO4溶液
C. 滴定结束时,若未等滴定管液面稳定就读数会导致测定结果偏低
D. 若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果偏高
18、 氧化亚铜主要用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂,以及各种铜盐、分析试剂、红色玻璃,还用于镀铜及镀铜合金溶液的配制。用某铜矿(主要含CuS、FeO)制备Cu2O的一种工艺流程如下图:
已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
请回答下列问题:
(1)基态Cu原子价层电子的排布图为___ ____。
(2)滤渣的主要成分是___ ____(填化学式)。
(3)“酸浸”中加入MnO2的作用是____ _;写出其中生成单质S的化学方程式___ ___ _。
(4)“调pH”范围是___ ____。
(5)“还原”前Cu元素以[Cu(NH3)4](OH)2的形式存在,水合肼被氧化的化学方程式为____ ;一定体积下,保持其它条件不变,水合肼浓度对Cu2O的产率的影响如图所示。当水合肼浓度大于3.25ml·L-1时,[Cu(NH3)4]2+的转化率仍增大,但Cu2O的产率下降,其可能的原因是___ ____。
19. 化合物G 是合成左氧氟沙星的中间体, 合成路线如下, 回答下列问题:已知:
I.R₁NHR₂+R₃OCH=CCOOR₄₂→R₁R₂NCH=CCOOR₄₂+R₃OH
路线一:
(1)A的结构简式为 ;E中含氧官能团的名称为 。
(2)E→F的化学方程式为 。
已知:
III. X2C═CHNR1(R2)+R3NH2 X2C═CHNHR3+HNR1(R2)[X=RCO—或—COOR]
路线二
(3)H的化学名称为 (系统命名法);J中有 种化学环境的氢。
(4)路线二由H→K的过程中反应类型共有 种;H的同分异构体中氟原子与苯环直接相连且能发生银镜反应的种类有 种。
20. 丙烯腈是塑料、合成橡胶、合成纤维三大合成材料的重要原料,未来我国丙烯腈的出口量将进一步增加。合成丙烯腈的反应: 。
(1)该反应中涉及的C、N、O三种元素原子的第一电离能由小到大的顺序是___ ____。
(2)一定条件下,在2L恒容密闭容器中;通入2mlC3H6、2mlNH3、15ml空气(O2的体积分数为),丙烯腈的产率与温度的关系如图所示。
①图中460℃前的产率_______(填“是”或“否”)为平衡产率;
理由是____ ___。
②若该反应达到A点所需时间为t min,则理论上C3H6的平均反应速率为___ ____。
(3)工业上在催化剂作用下,合成丙烯腈时还有副反应: 。
①其它条件不变时,压缩容器体积,副反应的平衡移动方向为____ ___。
②某温度下,向密闭容器中通入1mlC3H6、1mlNH3、7.5ml空气(O2与N2的体积比为1∶4),保持压强恒为99kPa,平衡时测得C3H6的转化率为90%,生成丙烯腈的选择性为(选择性:生成丙烯腈的C3H6与共转化的C3H6之比)。则生成丙烯腈的分压为____ ___kPa,该温度下副反应的Kp=____ ___。
(4)己二腈[NC(CH2)4CN]是制造尼龙的原料。电解丙烯腈可制得己二腈,其装置如下图所示:
①阴极的电极反应式为___ ____。
②电解一段时间后,该装置产生的O2在标准状态下的体积为33.6L,生成了291.6g已二腈,则该装置的电流效率____ ___%。(假设装置中阳极上没有电子损失,×100%)
答案
1-5 BCCAA 6-10 CABAD 11-15B BD C B AD
16、(1)A CD
(2)2 CH3As(OH)2 CH3As(OH)2与(CH3)2AsOH都属于分子晶体,CH3As(OH)2含两个羟基,形成的氢键数目多,沸点高
18、(1) (2)MnCO3
(3) ①. 做氧化剂 ②. MnO2+CuS+2H2SO4=S↓+MnSO4+CuSO4+2H2O (4)3.2≤pH<4.8
①. 4Cu(NH3)4(OH)2+N2H4·H2O+9H2O=2Cu2O↓+N2↑+16NH3·H2O ②. Cu2O被N2H4·H2O进一步还原成铜单质
20、(1)C
(4) ①. ②. 90
制作简单的燃料电池
制备并收集NH3
除去Na2CO3固体中少量的NaHCO3
碳酸氢钠受热分解
A
B
C
D
实验目的
实验及现象
结论
A
比较S与Cl的非金属性
用pH计测定0.1ml·L-1Na2S溶液和NaCl溶液的pH,前者大于后者
非金属性:S
鉴别白色固体Na2CO3和NaHCO3
室温下取少量固体于试管中,滴加几滴水,测量温度变化
温度降低的是NaHCO3.温度升高的是Na2CO3
C
检验Na2SO3溶液是否变质
取少量溶液于试管中,滴加盐酸酸化的Ba(NO3)2溶液;产生自色沉淀示领
Na2SO3溶液已经变质
D
探究淀粉水解程度
向淀粉水解液中加入NaOH溶液调至碱性,加入新制Cu(OH)2加热,产生红色沉淀
淀粉完全水解
实验序号
1
2
3
消耗 AgNO3标准溶液体积/mL
20.45
20.02
19.98
氢氧化物
Cu(OH)2
Fe(OH)3
Fe(OH)2
Mn(OH)2
开始沉淀的pH
4.8
1.9
7.5
8.8
沉淀完全的pH
6.4
3.2
9.7
10.4
山东省潍坊市2023-2024学年高三上学期1月期末化学试题: 这是一份山东省潍坊市2023-2024学年高三上学期1月期末化学试题,共4页。
山东省潍坊市诸城市繁华中学2023-2024学年高三上学期12月月考化学试题含答案: 这是一份山东省潍坊市诸城市繁华中学2023-2024学年高三上学期12月月考化学试题含答案,共8页。试卷主要包含了下列说法正确的是,下列化学说法正确的是,有八种物质,下列说法中不正确的是等内容,欢迎下载使用。
山东省潍坊市昌乐二中2023-2024学年高三上学期12月月考化学试题含答案: 这是一份山东省潍坊市昌乐二中2023-2024学年高三上学期12月月考化学试题含答案,共7页。试卷主要包含了本试题分第Ⅰ卷和第Ⅱ卷两部分,下列化学用语或图示表达正确的是,下列化学用语或表述正确的是等内容,欢迎下载使用。












