

2021学年河南省叶县中考化学适应性试卷
展开一、单项选择(本题包括14个小题,每小题1分,共14分。下列各题,每小题只有一个选项符合题意。)
1. 中华传统文化博大精深。下列典故中一定涉及化学变化的是( )
A.凿壁偷光 B.悬梁刺股 C.火上浇油 D.立竿见影
2. 为预防青少年成长过程中食欲不振,生长迟缓,发育不良,需适量补充的元素是( )
A.碘 B.铁 C.钙 D.锌
3. 化学与我们的生活密切关联。下列做法正确的是( )
A.焚烧废旧塑料减少“白色污染”
B.工业废水经净化处理,达标后方能排放
C.亚硝酸钠有咸味,可以代替食盐作调味剂
D.大量使用农药会导致土壤和食品污染,因此要杜绝使用农药
4. 我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显像等多个领域。氮和镓的原子结构示意图及镓在元素周期表中的信息如图所示,下列说法正确的是( )
A.氮化镓的化学式为GaN2
B.镓原子核内有31个中子
C.镓的相对原子质量是69.72 g
D.镓元素位于第四周期,属于金属元素
5. 下列物质在氧气中燃烧,有刺激性气味气体生成的是( )
A.镁条B.铁丝C.硫粉D.红磷
6. 下列除去杂质(括号内为杂质)的方法正确的是( )
A.CaCO3(CaO)﹣﹣加热固体混合物
B.CO2(H2O)﹣﹣将气体通入盛有生石灰的干燥管
C.NaCl(KNO3)﹣﹣将固体溶解,然后降温结晶
D.Cu(CuO)﹣﹣向固体中加入足量稀盐酸,过滤
7. 下列有关反应现象记录正确的是( )
A.打开盛有浓盐酸的试剂瓶瓶盖,瓶口有白烟生成
B.向氯化铜溶液中加入铝丝,铝丝表面生成红色物质
C.向氢氧化钠溶液中加入几滴石蕊,石蕊由紫色变为红色
D.铁与盐酸反应后溶液温度无变化
8. 下列与碳和碳的氧化物有关的说法中,正确的是( )
A.煤炉上放一盆水可防止CO中毒
B.CO2能使紫色石蕊溶液变红,说明CO2显酸性
C.CO和CO2化学性质不同的原因是分子构成不同
D.用墨绘制的古画经久不变色,说明碳不与任何物质反应
9. 稀土元素镝(Dy)常用于制造硬盘驱动器。下列有关说法中不正确的是( )
A.镝属于非金属元素
B.镝原子的质子数为66
C.镝的相对原子质量为162.5
D.稀土资源需合理利用和保护
10. 下列物质的名称(或俗名)与化学式一致的是( )
A.酒精、CH4B.石灰石、Ca(OH)2
C.纯碱、NaOHD.葡萄糖、C6H12O6
11. 月壤中富含多种元素,如:硅、铝、钾、钡、锂、铷、锆、铪、钛和稀土元素,下列元素中不属于金属元素的是( )
A.Si B.Li C.Ti D.Al
12. X、Y、Z有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去),下列各组物质按照X、Y、Z的顺序不符合要求的是( )
A.C、CO2、COB.H2O2、H2O、H2
C.CaO、Ca(OH)2、CaCO3D.CuO、Cu、Cu(NO3)2
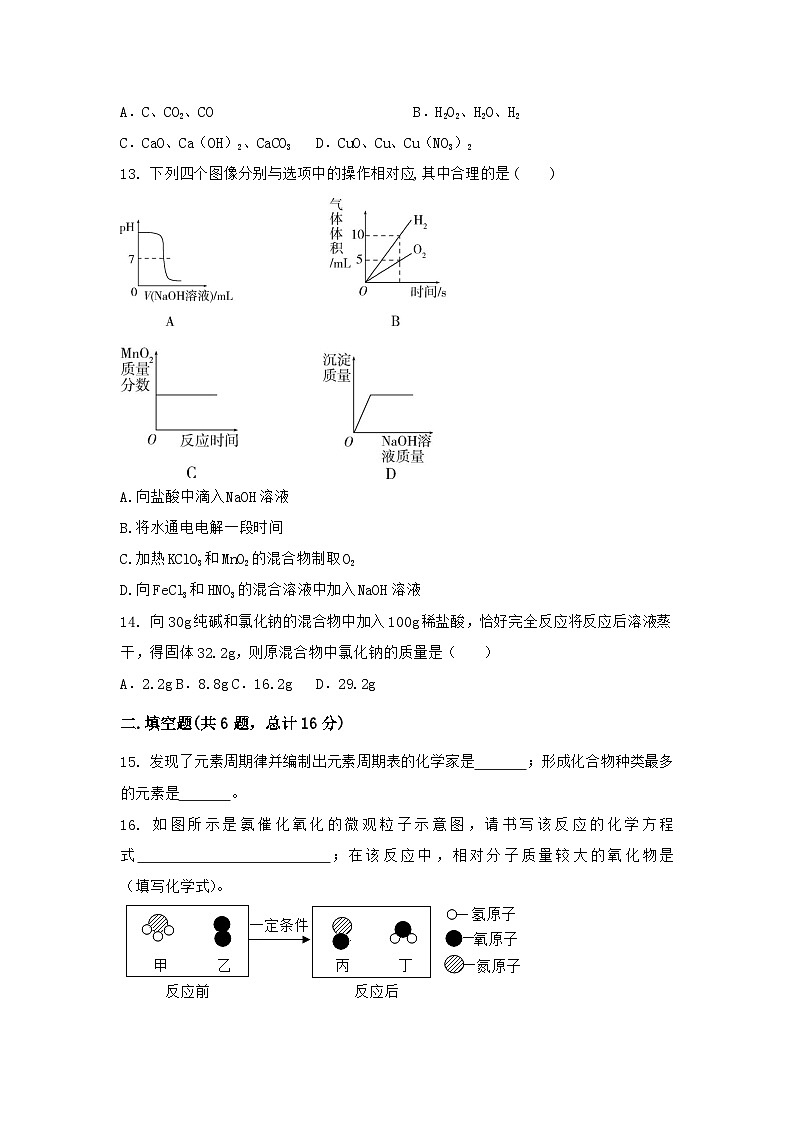
13. 下列四个图像分别与选项中的操作相对应,其中合理的是( )
A.向盐酸中滴入NaOH溶液
B.将水通电电解一段时间
C.加热KClO3和MnO2的混合物制取O2
D.向FeCl3和HNO3的混合溶液中加入NaOH溶液
14. 向30g纯碱和氯化钠的混合物中加入100g稀盐酸,恰好完全反应将反应后溶液蒸干,得固体32.2g,则原混合物中氯化钠的质量是( )
A.2.2gB.8.8gC.16.2gD.29.2g
二.填空题(共6题,总计16分)
15. 发现了元素周期律并编制出元素周期表的化学家是 ;形成化合物种类最多的元素是 。
16. 如图所示是氨催化氧化的微观粒子示意图,请书写该反应的化学方程式 ;在该反应中,相对分子质量较大的氧化物是 (填写化学式)。
17. 化石燃料的燃烧产生了大量的CO2,加剧了大气层的 效应;用医用酒精进行室内消毒时,若不慎引起小面积失火,可用湿抹布扑灭,其灭火的主要原理是 ;经测定某医用酒精中乙醇分子和水分子的个数比为1:1,则该医用酒精中乙醇的溶质质量分数为 (结果精确到0.1%)。
18. 乙醇俗称酒精,常用作燃料、溶剂和消毒剂。
(1)乙醇属于 (填“有机物”或“无机物”);
(2)将138 g酒精(C2H5OH)点燃,酒精燃烧全部转化为CO、CO2和H2O,恢复到室温,测得所得气体中碳元素质量分数为36%,则燃烧所消耗氧气的质量为 g。
19. 一定条件下,4.8 g CH4与16.0 g O2恰好完全反应,生成10.8 g H2O、4.4 g CO2和物质X。则X的质量为 g。该反应方程式中O2与X的化学计量数之比为 。
20. 如图所示,A、B、C、D分别为镁、稀盐酸、硝酸银溶液和氧气中的一种,短线相连的两物质间均能发生化学反应,且B与C反应后导致溶液质量增加。请回答,B的化式为: ,C和D反应的化学方程式为 。
三.简答题(共4题,总计10分)
21. 请用微观粒子的相关知识解释如下现象。
(1)打开盛放白酒的陶瓷瓶,闻到一股酒香 。
(2)用水银温度计测量体温,发现水银柱升高 。
22. 化学来源于生活,生活中蕴含着丰富的化学知识。请你用所学的化学知识帮助洋洋解决她的疑问。
(1)清晨,洋洋佩戴着KN95医用口罩走出了家门,这种口罩可以防止病毒吸入鼻腔,起到了与化学实验中
操作相同的作用。
(2)吃完午饭,洋洋用洗涤剂清洗饭盒上的油污,这是因为洗涤剂具有 作用。
(3)下午的化学课上,洋洋看到老师将一瓶汽水的瓶盖打开,汽水自动喷出来了,这是因为 。
(4)从课本中洋洋知道了高炉炼铁的反应原理:3CO+Fe2O3 2Fe +3CO2,在这个反应中 发生了还原反应。
(5)伴着晚霞洋洋回到了家中,妈妈准备了丰盛的晚餐,其中米饭富含的营养素是 。
23. 为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:
①溶解;
②依次加入过量的BaCl2、NaOH、Na2CO3溶液;
③过滤;
④加入适量盐酸;
⑤蒸发、结晶。
[提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀]
(1)请写出操作②中加入Na2CO3溶液后,生成沉淀的化学方程式 (写出一个即可)。
(2)操作⑤中玻璃棒的作用是什么? 。
(3)过滤后加入盐酸前溶液中含有哪些杂质? ,请设计实验检验(写出操作、现象、结论) 。
24. 某兴趣小组对“人体吸入的空气和呼出的气体有什么不同”进行探究。
(1)小明进行了实验并得出结论如下表,请补充完整。
(2)小红认为实验③的结论不正确,并查阅到相关资料。
【资料卡片】
Ⅰ.经测定,人体吸入空气和呼出气体中各成分的体积分数大约是:
Ⅱ.用氧气、二氧化碳传感器在烧杯顶部测量杯内两支蜡烛从点燃到全部熄灭后,杯内氧气和二氧化碳的浓度变化如图。
Ⅲ.将燃着的木条插入含20%氧气和80%二氧化碳的集气瓶中,木条能正常燃烧。
请结合以上资料,简述小红认为实验③结论不正确的理由。
四.综合题(共1题,总计10分)
25. 化学是以实验为基础的科学,实验是科学探究的重要手段。
(1)化学兴趣小组利用如图1所示装置制取CO2并进行相关的系列实验。
①装置A能控制反应的发生和停止,请将装置A图补画完整。
②装置C的作用是 。
③装置D中发生反应的化学方程式为 。
④装置E中观察到的现象是 。
⑤尾气CO可用装置G收集,利用了CO的性质有 。
(2)用如图2所示的微型装置进行实验。向A处注入H2O2溶液,在B处下方加热使木炭燃烧,产生的气体通入C处。
①A处发生反应的化学方程式为 。
②请设计实验证明反应结束后C中NaOH有剩余 。
(3)兴趣小组的同学将足量的大理石加入50g溶质质量分数为14.6%的稀盐酸中,充分反应(杂质不参加反应)。计算生成CO2的质量。
参考答案
一.选择题
1. C 2. D 3. B 4. D 5. C 6. D 7. B 8. C 9. A 10. D 11. A 12. C 13. B 14. B
二. 填空题
15. 门捷列夫;碳。
16. 4NH3+5O24NO+6H2O;NO。
17. 温室;隔绝氧气;71.9%。
18. (1)有机物 (2)224
19. 5.6 5∶2
20. Mg;HCl+AgNO3═AgCl↓+HNO3。
三. 简答题
21. (1)分子是不断地运动的;
(2)汞原子间的间隔变大。
22. (1)过滤
(2)乳化
(3)压强减小气体的溶解度减小(或气体的溶解度随压强的减小而减小或气体的溶解度和压强成正比)
(4)Fe2O3(或氧化铁或三氧化二铁)
(5)糖类
23. (1)BaCl2+Na2CO3=BaCO3↓+2NaCl或CaCl2+Na2CO3=CaCO3↓+2NaCl;
(2)搅拌,防止局部受热过高造成液滴飞溅;
(3)氢氧化钠和碳酸钠;取样,向其中加入足量的氯化钙溶液,有白色沉淀产生说明溶液中含有碳酸钠,然后过滤,再向滤液中加入无色酚酞试液,若变红色,说明溶液中还含有氢氧化钠。
24. (1)②浑浊 Ca(OH)2+CO2CaCO3↓+H2O
(2)由资料Ⅲ可知,二氧化碳含量为80%时木条仍能燃烧,而呼出气体中二氧化碳含量仅为4%,因此,不是呼出气体中二氧化碳含量高导致木条熄灭。[或由资料Ⅱ可知,当氧气含量低于15.65%(约16%)时蜡烛熄灭,而呼出气体中氧气含量为16%,因此木条熄灭的原因是氧气含量不足。
四.综合题
25. (1)①;
②除去CO2中混有的水蒸气;
③C+CO22CO;
④红棕色的粉末变成黑色;难溶于水、不与水反应等;
(2)①2H2O22H2O+O2↑;
②取C中的溶液适量于一支干净的试管中,加入过量的氯化钙溶液,充分反应后静置一段时间后,往上层清澈中滴加无色酚酞溶液,如果溶液变红色,说明NaOH有剩余,否则,NaOH没有剩余;
(3)设生成二氧化碳的质量为x。
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
50g×14.6% x
x=4.4g
答:生成CO2的质量为4.4g。
实验
实验操作
实验现象
解释与结论
①
收集两瓶呼出的气体
—
—
②
向其中一瓶气体中加入澄清的石灰水,振荡
澄清石灰水变
化学方程式为
③
向另一瓶气体中插入燃着的木条
燃着的木条熄灭
呼出气体中二氧化碳含量高,导致木条熄灭
气体成分
氮气
氧气
二氧
化碳
水蒸气
其他
气体
吸入的空气(%)
78
21
0.03
0.07
0.9
呼出的气体(%)
78
16
4
1.1
0.9
2021学年河南省孟州市中考化学适应性试卷: 这是一份2021学年河南省孟州市中考化学适应性试卷,共10页。试卷主要包含了单项选择等内容,欢迎下载使用。
2021学年河南省临颍县中考化学适应性试卷: 这是一份2021学年河南省临颍县中考化学适应性试卷,共11页。试卷主要包含了单项选择等内容,欢迎下载使用。
2021学年河南省辉县市中考化学适应性试卷: 这是一份2021学年河南省辉县市中考化学适应性试卷,共9页。试卷主要包含了单项选择等内容,欢迎下载使用。












