安徽省安庆市怀宁县高河中学2023-2024学年高一上学期12月第二次月考化学试题(含答案)
展开一、单选题(每题3分,共30分)
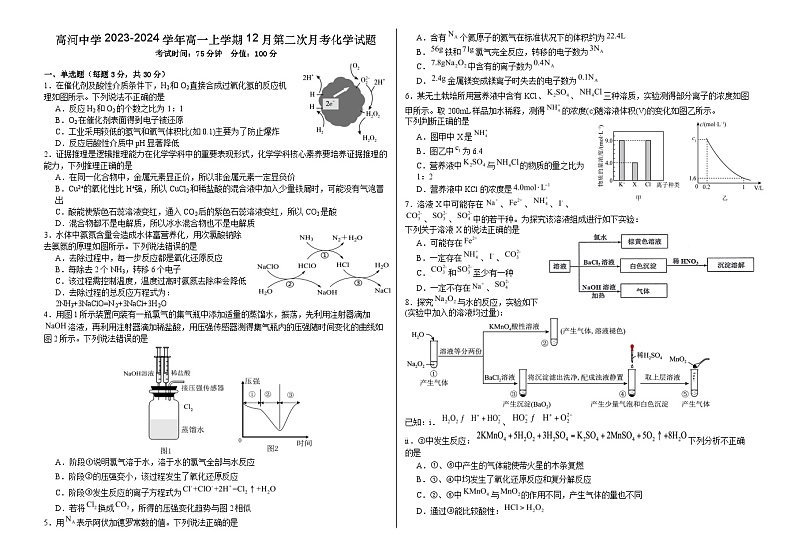
1.在催化剂及酸性介质条件下,H2和O2直接合成过氧化氢的反应机理如图所示。下列说法不正确的是
A.反应H2和O2的个数之比为1:1
B.O2在催化剂表面得到电子被还原
C.工业采用较低的氢气和氧气体积比(如0.1)主要为了防止爆炸
D.反应后酸性介质中pH显著降低
2.证据推理是逻辑推理能力在化学学科中的重要表现形式,化学学科核心素养要培养证据推理的能力,下列推理正确的是
A.在同一化合物中,金属元素显正价,所以非金属元素一定显负价
B.Cu2+的氧化性比H+强,所以CuCl2和稀盐酸的混合液中加入少量铁屑时,可能没有气泡冒出
C.酸能使紫色石蕊溶液变红,通入CO2后的紫色石蕊溶液变红,所以CO2是酸
D.混合物都不是电解质,所以冰水混合物也不是电解质
3.水体中氨氮含量会造成水体富营养化,用次氯酸钠除去氨氮的原理如图所示。下列说法错误的是
A.去除过程中,每一步反应都是氧化还原反应
B.每除去2个NH3,转移6个电子
C.该过程需控制温度,温度过高时氨氮去除率会降低
D.去除过程的总反应方程式为:2NH3+3NaClO=N2+3NaCl+3H2O
4.用图1所示装置向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法错误的是
A.阶段①说明氯气溶于水,溶于水的氯气全部与水反应
B.阶段②的压强变小,该过程发生了氧化还原反应
C.阶段③发生反应的离子方程式为
D.若将换成,所得的压强变化趋势与图2相似
5.用表示阿伏加德罗常数的值。下列说法正确的是
A.含有个氦原子的氦气在标准状况下的体积约为
B.铁和氯气完全反应,转移的电子数为
C.中含有的离子数为
D.金属镁变成镁离子时失去的电子数为
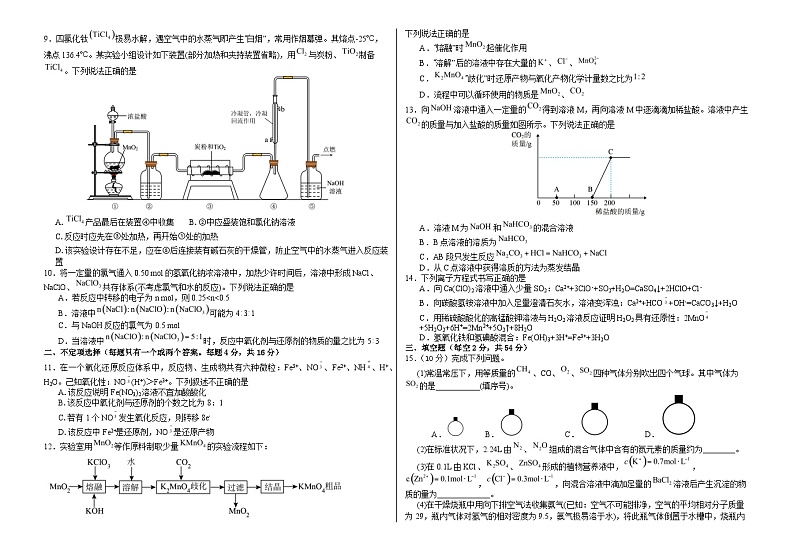
6.某无土栽培所用营养液中含有KCl、、三种溶质,实验测得部分离子的浓度如图甲所示。取200mL样品加水稀释,测得的浓度(c)随溶液体积(V)的变化如图乙所示。
下列判断正确的是
A.图甲中X是
B.图乙中为6.4
C.营养液中与的物质的量之比为1:2
D.营养液中KCl的浓度是
7.溶液X中可能存在、、、、、、中的若干种。为探究该溶液组成进行如下实验:
下列关于溶液X的说法正确的是
A.可能存在
B.一定存在、、
C.和至少有一种
D.一定不存在、
8.探究与水的反应,实验如下(实验中加入的溶液均过量):
已知:i.、
ii.②中发生反应:下列分析不正确的是
A.①、⑤中产生的气体能使带火星的木条复燃
B.①、④中均发生了氧化还原反应和复分解反应
C.②、⑤中与的作用不同,产生气体的量也不同
D.通过③能比较酸性:
9.四氯化钛极易水解,遇空气中的水蒸气即产生“白烟”,常用作烟幕弹。其熔点-25℃,沸点136.4℃。某实验小组设计如下装置(部分加热和夹持装置省略),用与炭粉、制备。下列说法正确的是
A.产品最后在装置④中收集B.②中应盛装饱和氯化钠溶液
C.反应时应先在③处加热,再开始①处的加热
D.该实验设计存在不足,应在⑤后连接装有碱石灰的干燥管,防止空气中的水蒸气进入反应装置
10.将一定量的氯气通入0.50 ml的氢氧化钠浓溶液中,加热少许时间后,溶液中形成NaCl、NaClO、共存体系(不考虑氯气和水的反应)。下列说法正确的是
A.若反应中转移的电子为n ml,则0.25
C.与NaOH反应的氯气为0.5 ml
D.当溶液中时,反应中氧化剂与还原剂的物质的量之比为5∶3
二、不定项选择(每题只有一个或两个答案。每题4分,共16分)
11.在一个氧化还原反应体系中,反应物、生成物共有六种微粒:Fe3+、NO、Fe2+、NH、H+、H2O。己知氧化性:NO(H+)>Fe3+。下列叙述不正确的是
A.该反应说明Fe(NO3)2溶液不宜加酸酸化
B.该反应中氧化剂与还原剂的个数之比为8:1
C.若有1个NO发生氧化反应,则转移8e-
D.该反应中Fe2+是还原剂,NO是还原产物
12.实验室用等作原料制取少量的实验流程如下:
下列说法正确的是
A.“熔融”时起催化作用
B.“溶解”后的溶液中存在大量的、、
C.“歧化”时还原产物与氧化产物化学计量数之比为
D.流程中可以循环使用的物质是、
13.向溶液中通入一定量的得到溶液M,再向溶液M中逐滴滴加稀盐酸。溶液中产生的质量与加入盐酸的质量如图所示。下列说法正确的是
A.溶液M为和的混合溶液
B.B点溶液的溶质为
C.AB段只发生反应
D.从C点溶液中获得溶质的方法为蒸发结晶
14.下列离子方程式书写正确的是
A.向Ca(ClO)2溶液中通入少量SO2:Ca2++3ClO-+SO2+H2O=CaSO4↓+2HClO+Cl-
B.向碳酸氢铵溶液中加入足量澄清石灰水,溶液变浑浊:Ca2++HCO+OH-=CaCO3↓+H2O
C.用稀硫酸酸化的高锰酸钾溶液与H2O2溶液反应证明H2O2具有还原性:2MnO+5H2O2+6H+=2Mn2++5O2↑+8H2O
D.氢氧化铁和氢碘酸混合:Fe(OH)3+3H+=Fe3++3H2O
三、填空题(每空2分,共54分)
15.(10分)完成下列问题。
(1)常温常压下,用等质量的、CO、、四种气体分别吹出四个气球。其中气体为的是___________(填序号)。
A.B.C.D.
(2)在标准状况下,2.24L由、组成的混合气体中含有的氮元素的质量约为________。
(3)在0.1L由KCl、、形成的植物营养液中,,,,向混合溶液中滴加足量的溶液后产生沉淀的物质的量为_____________。
(4)在干燥烧瓶中用向下排空气法收集氨气(已知:空气不可能排净,空气的平均相对分子质量为29,瓶内气体对氢气的相对密度为9.5,氨气极易溶于水),将此瓶气体倒置于水槽中,烧瓶内液面上升的体积占烧瓶总体积的___________。
(5)100mL0.3溶液(密度为,)和50mL0.2溶液(密度为)的混合,所得密度为的混合溶液中的浓度为____________(用含d1、d2、d3的式子表示)。
16.(18分)
(I)新冠肺炎疫情期间,“84消毒液”被广泛应用于物体表面杀菌消毒。绵实高一某学习小组的同学参阅“84消毒液”的配方,欲用NaClO固体配制480mL0.2ml/L的NaClO消毒液。回答下列问题:
(1)配制上述溶液需要的玻璃仪器有量筒、烧杯、玻璃棒、____________、____________;
(2)需要用托盘天平称量NaClO固体的质量为___________g;
(3)该小组的同学查阅资料得知:“84消毒液”与稀硫酸混合使用可增强消毒能力,于是他们准备用98%(密度为1.84g·cm-3)的浓硫酸配制250mL1.84ml·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①需用量筒量取浓硫酸的体积为____________mL;
②若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是_________
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,仰视溶液的凹液面
(II)有一份无色溶液,只可能有Na+、Cl﹣、H+、SO、CO、Cu2+、NO中的几种(忽略水电离产生的少量的OH﹣)。取该溶液检测,发现溶液显强酸性。
(4)不需要进一步实验,可以判断,溶液中一定存在___________,一定不存在____________。
(5)进一步测定,取100mL该溶液,发现该溶液中n(H+)=0.01ml,加入足量BaCl2,生成2.33g沉淀,过滤,滤液中加入足量AgNO3溶液,产生5.74g沉淀。100mL溶液中是否有Cl﹣_______(填“一定有”、“一定没有”或“可能有”),100mL溶液中Na+的物质的量至少为____________ml。
17.(16分)为保证家中所用器具与居住环境的洁净卫生,往往需使用各种各样的消毒剂,其中含氯消毒剂是目前广泛使用的一类消毒剂。
(1)用下列两种方法制取氯气:①用含有146 g HCl的浓盐酸与足量的反应;②用87 g 与足量的浓盐酸反应,所得氯气_______(填标号)。
A.②比①多B.①比②多C.一样多D.无法比较
(2)氯气通入淀粉-KI溶液后可观察到溶液变蓝,可得氧化性:_______(填“>”或“<”),已知氧化性,若将71g通入含1 ml 的溶液中,写出反应的离子方程式:
___________________________。
(3)是新型消毒剂,已知在酸性条件下可发生反应生成NaCl并释放出,该反应的离子方程式为____________________。NaOH溶液吸收,生成物质的量之比为1:1的两种盐,其中一种为,写出该反应的离子方程式:______________________。
(4)漂白粉的有效成分为___________(填化学式,下同),露置于空气中一段时间的漂白粉,加稀盐酸后产生的气体除了可能有和HCl外,还可能含有___________。在制备漂白粉的过程中,若温度控制不当,易生成,若向溶液中通入一定量的,制得的混合物中,则反应中被氧化和被还原的Cl的物质的量之比为_____________。
18.(12分)某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。
(1)A中发生反应的离子方程式为_______________。
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯。回答下列问题:
①在装置D中能看到的实验现象是__________________________________________________。
②在装置E的硬质玻璃管内盛有炭粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为______________________________________。
③装置F中球形干燥管的作用是________________________________________________。
(3)储气瓶b内盛放的试剂是_______________________。
(4)装置B中Fe2+被Cl2氧化为Fe3+,反应的离子方程式为_____________________________。
高一月考化学参考答案
1-10:DBAAA, CBDAD 11.BD 12.BC 13.BD 14.AC
15.(1)A (2)2.8g (3)0.03ml (4) (5)
16.(1) 500mL容量瓶 胶头滴管
(2)7.5
(3) 25.0 D
(4) H+ CO、Cu2+
(5) 可能有 0.01
17.(1)A
(2) > 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
(3) 5ClO+4H+=Cl-+4ClO2↑+2H2O 2ClO2+2OH-=ClO+ClO+H2O
(4) Ca(ClO)2 CO2 3:5
18.(1)4H++2Cl-+MnO22Mn2++Cl2↑+2H2O
(2) 溶液先变红后褪色 C+2Cl2+2H2OCO2+4HCl 防止倒吸
(3)饱和食盐水
(4)2Fe2++Cl2=2Fe3++2Cl-
安徽省安庆市怀宁县2023-2024学年高二上学期期末化学试题(含答案): 这是一份安徽省安庆市怀宁县2023-2024学年高二上学期期末化学试题(含答案),共9页。试卷主要包含了单选题,非选择题等内容,欢迎下载使用。
安徽省安庆市怀宁县高河中学2023-2024学年高二上学期第三次月考化学试题含答案: 这是一份安徽省安庆市怀宁县高河中学2023-2024学年高二上学期第三次月考化学试题含答案,共6页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
安徽省安庆市怀宁县高河中学2023-2024学年高二上学期第二次月考化学试题: 这是一份安徽省安庆市怀宁县高河中学2023-2024学年高二上学期第二次月考化学试题,共4页。试卷主要包含了5 Na-23 I-127, 下列说法中正确的是,5−10﹣9等内容,欢迎下载使用。












