

2024届高三新高考化学大一轮专题训练-盐类的水解
展开2024届高三新高考化学大一轮专题训练-盐类的水解
一、单选题
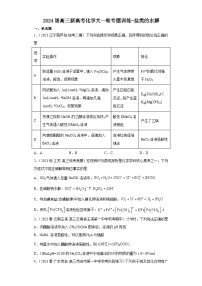
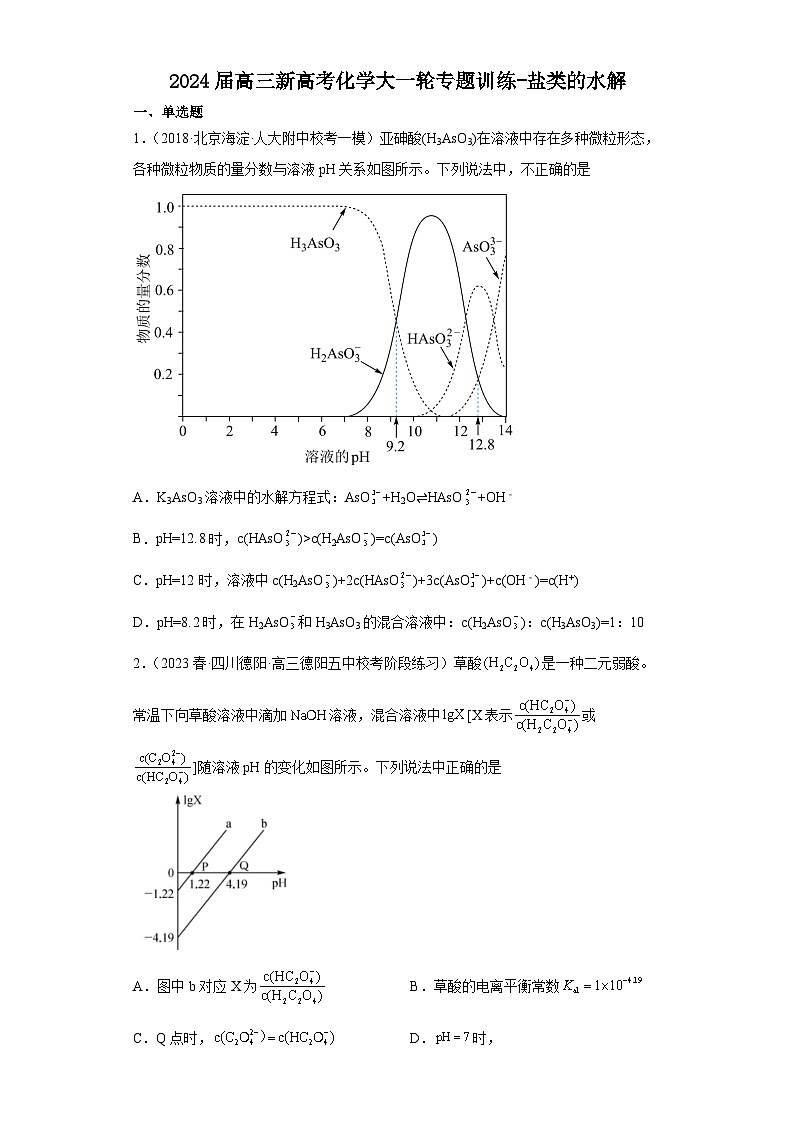
1.(2018·北京海淀·人大附中校考一模)亚砷酸(H3AsO3)在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液pH关系如图所示。下列说法中,不正确的是
A.K3AsO3溶液中的水解方程式:AsO+H2O⇌HAsO+OH﹣
B.pH=12.8时,c(HAsO)>c(H2AsO)=c(AsO)
C.pH=12时,溶液中c(H2AsO)+2c(HAsO)+3c(AsO)+c(OH﹣)=c(H+)
D.pH=8.2时,在H2AsO和H3AsO3的混合溶液中:c(H2AsO):c(H3AsO3)=1:10
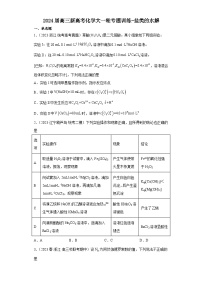
2.(2023春·四川德阳·高三德阳五中校考阶段练习)草酸是一种二元弱酸。常温下向草酸溶液中滴加溶液,混合溶液中[X表示或]随溶液pH的变化如图所示。下列说法中正确的是
A.图中b对应X为 B.草酸的电离平衡常数
C.Q点时, D.时,
3.(2023·江苏南京·统考二模)在元素周期表中,某些主族元素与右下方的主族元素的有些性质是相似的。和均为两性氢氧化物,溶于强碱形成。BeO和都具有难溶于水、高熔点等性质。和在气态时通常以二聚体的形式存在。B和Si均能溶于NaOH溶液生成盐和氢气。工业上用焦炭和石英砂(主要成分为)在高温条件下反应制得粗硅。硼酸()和硅酸都是弱酸,硼酸晶体有类似于石墨的片层状结构,常用作医用消毒剂、润滑剂等。下列化学反应表示不正确的是
A.氢氧化铍溶于强碱:
B.可溶性铝盐净水原理:
C.硅与氢氧化钠溶液反应:
D.焦炭与石英砂反应:
4.(2023春·江苏南京·高三南京市雨花台中学校考期中)生产碳酸饮料时常添加苯甲酸钠(用NaA表示),用作饮料的防腐剂。已知25℃时,苯甲酸(HA)、醋酸、碳酸的电离平衡常数分别为: Ka(HA) = 6.25×10-5,Ka(CH3COOH) = 1.75×10-5, Ka1(H2CO3)=4.17×10-7、 Ka2(H2CO3)=4.90×10-11,25°C时,不考虑饮料中其他成分的影响,下列说法错误的是
A.饮料中添加苯甲酸钠,促进了水的电离
B.向苯甲酸溶液中滴加Na2CO3溶液,有气泡产生
C.当pH为6.0时, 饮料中=0.16
D.Ka(HA)> Ka(CH3COOH)的原因是:苯环和甲基对羧基中氧氢键极性影响不同
5.(2023·安徽马鞍山·统考一模)用0.1000mol·L-1盐酸滴定0.1000mol·L-1Na2A溶液20.00mL,溶液中H2A、HA-、 A2-的分布分数 δ随pH变化曲线及滴定曲线如图。下列说法不正确的是
[如A2-分布分数: δ(A2-)=
A.a点溶液中存在c(Na+)+ c(H+)=3 c(A2-)+ c(OH-)+ c(Cl-)
B.b点溶液中存在c(H2A)< c(A2-)
C.c点溶液中存在c(HA-)>c(H2A)
D.H2A的Ka1为10-6.38
6.(2023·重庆·统考三模)25℃时,的电离常数。在10.0mL 0.10mol/L的溶液中加入5.0mL 0.10mol/L的NaOH溶液。下列说法不正确的是
A.该混合溶液呈酸性
B.该混合溶液中:
C.0.10mol/L的溶液中
D.将0.10mol/L的溶液加水稀释,增大
7.(2023春·四川内江·高三四川省内江市第六中学校考期中)下列实验操作能达到实验目的的是
实验目的
实验操作
A
制备Fe(OH)3胶体
将NaOH浓溶液滴加到饱和FeCl3溶液中
B
由MgCl2溶液制备无水MgCl2
将MgCl2溶液加热蒸干
C
测定醋酸钠溶液pH
用玻璃棒蘸取溶液,点在湿润的pH试纸上
D
制取次氯酸浓度较高的溶液
将Cl2通入碳酸氢钠溶液中
A.A B.B C.C D.D
8.(2023春·江苏常州·高三统考期中)通过下列实验探究草酸()的性质
实验
实验操作和现象
1
加热草酸晶体,将产生的气体通入澄清石灰水中,石灰水变浑浊
2
室温下,用pH计测得溶液的pH约为1.3
3
室温下,向溶液中逐滴加入溶液,得到如图所示的滴定曲线
下列有关说法正确的是
A.,溶液中存在
B.依据实验1的现象,确定气体的成分仅为
C.时的溶液中:
D.、、对应的溶液中,水的电离程度:
9.(2023春·河南·高三洛宁县第一高级中学校联考期中)室温下,向20 mL 0.05 mol/L的H2X溶液中逐滴加入0.1 mol/L的NaOH溶液,溶液pH随着NaOH溶液体积变化的关系如图所示。下列叙述错误的是
A. mL时,溶液中
B.随着NaOH溶液的不断加入,水的电离程度先增大后减小
C.室温下,的电离常数
D.时, mL,溶液中
10.(2023·浙江绍兴·统考模拟预测)已知为二元弱酸,,。室温下,下列说法不正确的是
A.0.1mol/L NaHR溶液
B.用NaOH溶液中和一定量的溶液至呈中性时,溶液中
C.0.1mol/L 溶液:
D.0.01mol/L的溶液与的NaOH溶液完全中和时,消耗酸与碱溶液的体积比为1∶2
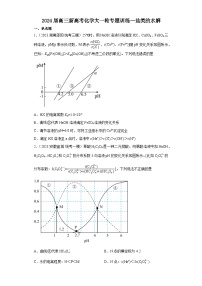
11.(2023·湖北荆州·统考模拟预测)某温度下,改变0.1溶液的pH,各种含铬元素微粒及的浓度随pH的变化如图所示,下列有关说法正确的是
A.该温度下
B.该温度下溶液呈碱性
C.的平衡常数
D.C点溶液中存在:
12.(2023春·重庆沙坪坝·高三重庆市凤鸣山中学校考阶段练习)25℃时,取两份10mL0.05mol/L的溶液,一份滴加0.05mol/L的盐酸,另一份滴加0.05mol/LNaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法不正确的是
A.的水解程度大于电离程度
B.a、c、e三点的溶液中均有分子存在
C.a→b→c过程中:逐渐增大
D.d点对应的溶液中:
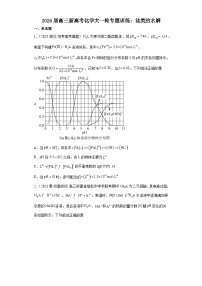
13.(2023·辽宁·校联考三模)25℃,用0.1 mol⋅L NaOH溶液滴定某二元弱酸,pH与粒子的分布分数δ[如],的关系如图所示。下列说法正确的是
A.时,应选择酚酞溶液作指示剂
B.的数量级为
C.NaHA溶液中
D.Na₂A溶液中
14.(2023·辽宁·校联考三模)常用于微电子工业,可由反应制得。为阿伏加德罗常数的值,下列说法正确的是
A.1 mol 中含有的中子数为
B.反应生成22.4 L 时,转移电子数为
C.当反应消耗1 mol 时,断裂的键数为
D.1000 mL 0.1mol·L-1 溶液中数目为
二、非选择题
15.(2023·全国·高三专题练习)Ⅰ.回答下列问题:
(1)溶液蒸干得到的固体物质是_______,原因是_______。
(2)溶液蒸干灼烧得到的固体物质是_______,原因是_______。
(3)将的溶液加热蒸干灼烧最后所得的固体是_______,原因是_______。
Ⅱ.具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比高效,且腐蚀性小。请回答下列问题:
在溶液中分三步水解:
(4)以上水解反应的平衡常数由大到小的顺序是_______。通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为。欲使平衡正向移动可采用的方法是_______(填字母)。
a.降温 b.加水稀释 c.加入 d.加入
室温下,使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是_______。
16.(2023·全国·高三专题练习)回答下列问题
(1)已知某温度时,溶液的水解常数,则当溶液中时,试求该溶液的___________。
(2)已知时,的电离常数,该温度下的溶液中___________(已知:)。
(3)时,的电离常数,则该温度下水解反应的平衡常数___________,若向溶液中加入少量的,则溶液中将___________(填“增大“减小”或“不变”)。
17.(2022秋·甘肃兰州·高三兰州一中校考期末)I.室温时,向100mL 0.1 HCl溶液中滴加0.1氨水,得到溶液pH与氨水体积的关系曲线如图所示:
(1)试分析图中a、b、c、d四个点,水的电离程度最大的是______________;
(2)在b点,溶液中各离子浓度由大到小的排列顺序是_____________________________;
(3)写出a点混合溶液中下列算式的精确结果(不能近似计算):_______________;
(4)25℃时,同浓度的下列溶液:①HCl;②;③;④,其中pH由大到小的顺序是_________________。
II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg/L。处理镉废水可采用化学沉淀法。
(5)一定温度下,的,的,该温度下______________[填“”或“”]的饱和溶液中浓度较大。
(6)向某含镉废水中加入,当浓度达到mol/L时,废水中的浓度为___________________mol/L[已知:,此时______________(填“符合”或“不符合”)《生活饮用水卫生标准》。
18.(2023春·陕西咸阳·高三校考开学考试)Ⅰ.运用化学反应原理,研究硫、磷化合物的反应具有重要意义。
(1)已知(次磷酸)的水溶液中存在分子。与足量溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为_______,该盐属于_______(填“正盐”或“酸式盐”)。易被氧化为,已知常温下的电离常数为,,请利用以上数据计算推测溶液呈_______性。
(2)常温下,用溶液吸收得到的溶液,吸收过程中水的电离平衡_______(填“向左”“向右”或“不”)移动。试计算该溶液中_______(常温下,的电离平衡常数)。
(3)化工生产中常用作沉淀剂除去工业废水中的,其反应原理为。下列有关叙述正确的是_______。
A.
B.达到平衡时
C.溶液中加入少量固体后,溶液中都减小
D.该反应平衡常数
Ⅱ.在氯化铁溶液中存在平衡:。回答下列问题:
(4)加热稀溶液,溶液颜色会不断加深,可得到一种红褐色透明液体,向这种液体中加入溶液,产生的现象为_______。
(5)不断加热溶液,蒸干水分并灼烧,最终得到的固体是_______(写化学式)。
(6)为防止配制溶液时出现浑浊,正确操作是_______。
参考答案:
1.C
【详解】A.由图示可知,溶液中存在H2AsO、HAsO、AsO、H3AsO3,说明H3AsO3为三元弱酸,AsO水解以第一步为主,其水解方程式为:AsO+H2O⇌HAsO+OH﹣,故A正确;
B.结合图示可知,pH=12.8时,H2AsO、HAsO、AsO离子浓度大小为:c(HAsO)>c(H2AsO)=c(AsO),故B正确;
C.pH=12时,c(H+)较小,溶液中c(H2AsO)+2c(HAsO)+3c(AsO)+c(OH﹣)之和远远大于c(H+),故C错误;
D.pH=9.2时c(H2AsO)=c(H3AsO3),Ka(H3AsO3)==c(H+)=10﹣9.2,pH=8.2时平衡常数不变,结合Ka(H3AsO3)=可知,c(H2AsO3﹣):c(H3AsO3)=Ka(H3AsO3):c(H+)=10﹣9.2:10﹣8.2=1:10,故D正确;
故选C。
2.C
【详解】A.相同pH时,>,则a对应X为,b对应X为,A项错误;
B.,当=,即lgX=0,c(H+)=10-1.22,所,B项错误;
C.Q点时,lg=0,则=1,,C项正确;
D.,时,=>1,即,D项错误。
答案选C。
3.B
【详解】A.由题给信息可知,氢氧化铍是两性氢氧化物,能与氢氧化钠溶液反应生成四羟基合铍离子,电极反应式为,故A正确;
B.可溶性铝盐净水原理为铝离子在溶液中水解生成氢氧化铝,氢氧化铝吸附水中悬浮杂质而达到净水的作用,反应的离子方程式为,故B错误;
C.硅与氢氧化钠溶液反应生成硅酸钠和氢气,反应的化学方程式为,故C正确;
D.焦炭与石英砂高温条件下反应生成硅和一氧化碳,反应的化学方程式为,故D正确;
故选B。
4.C
【详解】A.苯甲酸钠为强碱弱酸盐,在溶液中水解使溶液呈碱性,水解促进了水的电离,故A正确;
B.由电离常数可知,苯甲酸的电离常数大于碳酸的一级电离常数,则向苯甲酸溶液中滴加碳酸钠溶液,会有二氧化碳气体产生,故B正确;
C.由电离常数公式可知,饮料中= ,则溶液pH为6.0时,饮料中==0.016,故C错误;
D.苯环是吸电子基团,使羧基中氢氧键的极性增强,易电离出氢离子,而甲基是供电子基团,使羧基中氢氧键的极性减弱,难电离出氢离子,所以苯甲酸的电离常数大于乙酸是因为苯环和甲基对羧基中氧氢键极性影响不同,故D正确;
故选C。
5.B
【分析】各离子含量曲线如图 。
【详解】A.a点加入10mL盐酸发生反应为Na2A+HCl=NaCl+NaHA,溶液中主要有NaCl、NaHA、Na2A且物质的量之比为1:1:1。该体系中电荷守恒为c(Na+)+ c(H+)=2 c(A2-)+ c(OH-)+ c(Cl-)+c(HA-),如图c(A2-)= c(HA-),所以等式变形为c(Na+)+ c(H+)=3 c(A2-)+ c(OH-)+ c(Cl-),A项正确;
B.b点加入20mL盐酸发生的反应为Na2A+HCl=NaCl+NaHA,溶液中的物质为NaCl和NaHA,溶液呈碱性,水解大于电离即c(H2A)>c(A2-),B项错误;
C.从含量分布图可看出c(HA-)>c(H2A),C项正确;
D.利用d点pH=6.38即c(H+)=10-6.38,计算Ka1 =,D项正确;
故选B。
6.C
【分析】在10.0mL 0.10mol/L的溶液中加入5.0mL 0.10mol/L的NaOH溶液,酸过量,则该混合液中溶质是和,且浓度相同。据此回答问题。
【详解】A.该混合液中溶质是和,且浓度相同,由可知,的电离大于水解,所以该混合溶液呈酸性,故A正确;
B.由可知,的电离大于水解,所以该混合溶液呈酸性,则该混合溶液中:,故B正确;
C.醋酸的电离常数,在0.10mol/L的溶液中,则,,2<pH<3,故C错误;
D.醋酸的电离常数,温度不变不变,加水稀释时减小,故增大,故D正确;
故选C。
7.D
【详解】A.制备Fe(OH)3胶体,是将饱和氯化铁溶液滴加几滴到沸水中,继续加热至出现红褐色,停止加热,故A不符合题意;
B.由于镁离子会发生水解,因此应在HCl气流中加热MgCl2溶液制备无水MgCl2,故B不符合题意;
C.测定溶液pH时,pH试纸上不能湿润,故C不符合题意;
D.将Cl2通入碳酸氢钠溶液中,氯气和水反应生成盐酸和次氯酸,次氯酸与碳酸氢钠不反应,盐酸和碳酸氢钠反应,致使氯水与水反应平衡正向移动,因此会制取次氯酸浓度较高的溶液,故D符合题意;
综上所述,答案为D。
8.C
【详解】A.根据电荷守恒,溶液中存在,故A错误;
B.二氧化碳能使澄清石灰水变浑浊,依据实验1的现象,只能确定气体的中含有,不确定是否还有其他气体,故B错误;
C.时的溶液中溶质为NaHC2O4,,根据图像可知,此时溶液呈酸性,,故C正确;
D.、、对应的溶液中,b点溶质为Na2C2O4, Na2C2O4水解促进水电离,a点含有NaHC2O4、Na2C2O4,NaHC2O4电离出的氢离子抑制水电离,c点含有Na2C2O4、氢氧化钠,氢氧化钠抑制水电离,水的电离程度b点水电离程度最大,故D错误;
选C。
9.A
【分析】由题干图像信息可知,0.05mol/L的H2X溶液的pH=3,说明H2X为弱酸,据此分析解题。
【详解】A. mL时,加入的NaOH和H2X的物质的量相等,故此时溶液中的溶质为NaHX,溶液显酸性即HX-的电离大于水解,故有,A错误;
B.随着NaOH溶液的不断加入,溶液溶质由H2X到H2X、NaHX,Na2X,Na2X和NaOH,当溶质为Na2X时由于X2-的水解对水的电离起促进作用,此时水的电离程度最大,而后再加入的NaOH则抑制水的电离,故水的电离程度先增大后减小,B正确;
C.由题干图像信息可知,0.05mol/L的H2X溶液的pH=3,故室温下,的电离常数Ka1=≈,C正确;
D.当V0=20mL时溶液中溶质为Na2X,由于X2-水解使得溶液显碱性,故时, mL,根据电荷守恒有:,故溶液中有,D正确;
故答案为:A。
10.C
【详解】A.NaHR是弱酸的酸式盐,存在电离和水解,,电离强于水解,0.1mol/L NaHR溶液,A正确;
B.用NaOH溶液中和一定量的溶液至呈中性时,=10-7mol/L,,故溶液中,B正确;
C.0.1mol/L 溶液中根据电荷守恒和元素守恒可得c(H2R)+c(HR-)+c(R2-)=0.1mol/L,c(H+)=c(HR-)+2c(R2-)+c(OH-),故,C错误;
D.H2R+2NaOH=2H2O+Na2R,0.01mol/L的(二元酸)溶液与即0.01mol/L的NaOH溶液完全中和时,消耗酸与碱溶液的体积比为1∶2,D正确;
故选C。
11.C
【详解】A.由图可知,G点溶液pH为13、氢氧根离子浓度为0.1mol/L,则水的离子积常数KW=0.1×10—13=1×10—14,故A错误;
B.由图可知,A点溶液中H2CrO4和HCrO浓度相等时,溶液pH为0.74,由电离常数公式可知,铬酸的一级电离常数Ka1== c(H+)=10—0.74,同理由B点数据可得二级电离常数Ka2== c(H+)=10—6.5,HCrO的水解常数Kh==<Ka2,则HCrO的水解程度小于电离程度,KHCrO4溶液呈酸性,故B错误;
C.由图可知,C点溶液中CrO和Cr2O的浓度都为0.051mol/L,溶液pH为6.6,由方程式可知,反应的平衡常数K==c(CrO)c2(H+)=0.051×(10—6.6)2=5.1×10—15.2,故C正确;
D.由图可知,C点溶液中CrO和Cr2O的浓度都为0.051mol/L,溶液pH为6.6,由电荷守恒关系c(K+)+ c(H+)=2c(Cr2O)+2c(CrO)+ c(HCrO)+ c(OH—),溶液中c(K+)<2c(Cr2O)+2c(CrO)+ c(HCrO)=4c(Cr2O)+c(HCrO),故D错误;
故选C。
12.C
【详解】A.0.05mol/L的溶液的pH为8,说明0.05mol/L的溶液,水解大于电离,A正确;
B.a、c、e三点的溶液中均有分子存在,B正确;
C.由电荷守恒得,加入NaOH10mL时,不变,变小,a→b→c过程中,不是逐渐增大,C错误;
D.由电荷守恒可知,D正确。
故选C。
13.C
【分析】由图可知,bf曲线为0.1mol•L−1 NaOH溶液滴定二元弱酸H2A的滴定曲线,当时,反应生成NaHA,NaHA溶液显酸性,当时,反应生成Na2A,Na2A溶液显碱性,以此解答该题。
【详解】A.时,反应生成NaHA,NaHA溶液显酸性,应选用甲基红做指示剂,故A错误;
B.由图可知,当溶液中c(HA−)=c(H2A),pH<7,由>1×10−7,故B错误;
C.由分析可知,NaHA溶液显酸性,HA-电离程度大于水解程度;所以溶液中,故C正确;
D.Na2A溶液中存在元素质量守恒关系:c(Na+)=2c(HA−)+2c(A2−)+2c(H2A),所以,故D错误;
故答案选C。
14.C
【详解】A.中子数=质量数-质子数;所以1 mol 中含有的中子数为;故A错误;
B.未说明物质状态,无法计算,故B错误;
C.根据反应可知,消耗3 mol 时,有1molNH3的断裂;1molNH3中含有3mol;所以反应消耗1 mol 时,断裂的键数为;故C正确;
D.在溶液中水解,导致溶液中数目小于;故D错误;
故答案选C。
15.(1) 尽管水解,但由于为难挥发性酸,最后仍然得到明矾。注意温度过高,会脱去结晶水
(2) 水解生成和,在加热蒸干过程中挥发,逐渐被氧化生成,灼烧分解生成
(3) 水解的化学方程式为,,,最终得到
(4) bd 调节溶液的
【详解】(1)明矾中的铝离子可以水解,但是Al3+水解生成氢氧化铝和硫酸,硫酸是高沸点酸,不能挥发,最后氢氧化铝和硫酸又反应生成Al3+,最后蒸干得到明矾晶体,故答案为KAl(SO4)2·12H2O;尽管Al3+水解,由于硫酸是高沸点酸,不能挥发,最后仍然会得到明矾晶体;
(2)蒸发FeCl2溶液,Fe2+水解生成Fe(OH)2和HCl,在加热蒸干过程中HCl挥发,得到的是氢氧化亚铁,氢氧化亚铁被氧气氧化为氢氧化铁,灼烧后得到氧化铁,故答案为 Fe2O3;Fe2+水解生成Fe(OH)2和HCl,在加热蒸干过程中HCl挥发,Fe(OH)2逐渐被氧化生成Fe(OH)3,Fe(OH)3灼烧分解生成Fe2O3;
(3)NaClO溶液加热蒸干,NaClO发生水解生成次氯酸和氢氧化钠,次氯酸受热生成氯化氢和氧气,根据钠与氯1∶1,则最终生成的氢氧化钠与氯化氢刚好反应生成氯化钠和水,所以最终加热蒸干最后所得的固体是氯化钠,故答案为氯化钠;NaClO水解的化学方程式为NaClO+H2O=NaOH+HClO,2HClO2HCl+O2↑,HCl+NaOH=NaCl+H2O,故最终得到NaCl;
(4)水解反应若分步进行,水解的平衡常数逐渐减小,故;
离子方程式为,欲使平衡正向移动可采用的方法是:
a.水解是吸热反应,降温平衡往逆向移动,a错误;
b.越稀越水解,加水稀释平衡往正向移动,b正确;
c.加入,铵根水解呈酸性,与Fe3+的水解互相抑制,所以平衡往逆向移动,c错误;
d.加入,与H+反应,使平衡往正向移动,d正确;
故选bd;
根据方程式可知,H+浓度影响平衡移动,所以使氯化铁溶液转化为高浓度聚合氯化铁的关键条件是调节溶液的。
16.(1)9
(2)
(3) 增大
【详解】(1)Na2CO3溶液的水解常数,,当溶液中,可知,,则,pH=9,答案:9;
(2)的溶液中 ,,答案:;
(3)水解反应的平衡常数,若向溶液中加入少量的,I2+HSO+H2O=2I-+SO+3H+,增大,不变, 增大,答案:;增大。
17.(1)a
(2)
(3)
(4)③④②①
(5)
(6) 符合
【详解】(1)酸或碱抑制水电离,弱离子促进水的电离,根据图中滴加氨水的体积可知a点溶质为NH4Cl,促进水电离;b、c、d三点溶液中溶质都是NH4Cl和NH3H2O混合溶液,且NH3H2O的浓度依次增大,NH3H2O属于弱碱,抑制水的电离,且浓度越大越抑制,故水的电离程度最大的是a点;
(2)b点溶液呈中性,,盐酸和氨水完全中和后氨水过量,溶质为NH4Cl和NH3H2O,根据电荷守恒可得,故,溶液中各离子浓度由大到小的排列顺序是;
(3)室温时,a点混合溶液的pH=6,,,根据电荷守恒有,故=;
(4)①HCl是强酸,完全电离,pH<7;②溶液中的水解使溶液显酸性,pH<7,但是水解程度是微弱的,pH大于同浓度的盐酸;③溶液由于的水解使溶液显碱性,溶液pH>7;④溶液中的水解使溶液显碱性,pH>7,但是水解程度小于同浓度的Na2CO3溶液,pH小于同浓度的Na2CO3溶液,根据以上分析,可知pH由大到小的顺序是③④②①;
(5)当达到沉淀溶解平衡时有Cd2++,则该温度下饱和溶液中,当达到沉淀溶解平衡时有Cd2++2OH-,则该温度下饱和溶液中,则的饱和溶液中浓度较大;
(6)当时,=10-19×112×103mgL-1=1.12×10-14 mgL-1<0.005 mgL-1,符合《生活饮用水卫生标准》。
18.(1) 盐 碱
(2) 向右
(3)CD
(4)出现红褐色沉淀
(5)
(6)将固体溶于浓盐酸中,再加水稀释至所需浓度
【详解】(1)H3PO2(次磷酸)的水溶液中存在H3PO2分子,说明H3PO2为弱酸,H3PO2与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,说明H3PO2为一元弱酸,生成的盐为正盐,化学式为:NaH2PO2,已知常温下H3PO4的电离常数为Ka1=6.9×10-3,Ka2=6.2×10-8,Ka3=4.8×10-13,Na2HPO4溶液中,水解平衡常数≈1.6×10-7>Ka2=6.2×10-8,溶液中水解程度大,溶液显碱性,故答案为:NaH2PO2;盐;碱;
(2)氢氧化钠是碱电离产生的氢氧根离子抑制水的电离,吸收二氧化硫后,消耗氢氧根离子,碱性减弱,同时生成亚硫酸钠,是强碱弱酸盐,能够水解,对水的电离起促进的作用,所以吸收二氧化硫过程中水的电离平衡向右移动,pH=9的溶液中c(H+)=10-9mol/L,碱电离产生氢氧根离子抑制水的电离,可水解的盐促进水的电离,依据Ka2=,得溶液中,故答案为:向右;;
(3)A.沉淀的转化向溶度积更小的方向移动,可知FeS的Ksp大于CuS的Ksp,故A错误;
B.开始浓度未知,不能确定平衡浓度的关系,则c(Fe2+)、c(Cu2+)平衡时不一定相等,故B错误;
C.加入少量Na2S固体后,CuS更难溶,先Cu2+、S2-发生反应生成沉淀,c(Cu2+)、c(Fe2+)都减小,故C正确;
D.Cu2+(q)+FeS(s)⇌CuS(s)+Fe2+(aq),反应的平衡常数,故D正确;
故答案为:CD;
(4)氯化镁属于电解质,向氢氧化铁胶体中加入氯化镁溶液时易产生聚沉现象,从而生成红褐色氢氧化铁沉淀,故答案为:生成红褐色沉淀;
(5)加热蒸干FeCl3溶液时,FeCl3水解生成氢氧化铁和HCl,加热促进HCl挥发,从而促进FeCl3水解,蒸干时得到氢氧化铁固体,灼烧氢氧化铁固体,氢氧化铁分解生成氧化铁和水,所以最终得到Fe2O3固体,故答案为:Fe2O3;
(6)FeCl3水解生成氢氧化铁和HCl,为防止氯化铁水解,向溶液中滴加少量稀盐酸即可,故答案为:将固体溶于浓盐酸中,再加水稀释至所需浓度。
2024届高三新高考化学大一轮专题训练-盐类的水解: 这是一份2024届高三新高考化学大一轮专题训练-盐类的水解,共26页。试卷主要包含了单选题,多选题,非选择题等内容,欢迎下载使用。
2024届高三新高考化学大一轮专题训练 盐类的水解: 这是一份2024届高三新高考化学大一轮专题训练 盐类的水解,共21页。试卷主要包含了单选题,非选择题等内容,欢迎下载使用。
2024届高三新高考化学大一轮专题训练--盐类的水解: 这是一份2024届高三新高考化学大一轮专题训练--盐类的水解,共25页。试卷主要包含了单选题,多选题,非选择题等内容,欢迎下载使用。