

所属成套资源:全套2024届人教版高考化学一轮复习培优提升练含答案
2024届人教版高考化学一轮复习培优提升练(一)阿伏加德罗常数的应用作业含答案
展开
这是一份2024届人教版高考化学一轮复习培优提升练(一)阿伏加德罗常数的应用作业含答案,共5页。试卷主要包含了5NA,NA是阿伏加德罗常数的值,NA为阿伏加德罗常数的值等内容,欢迎下载使用。
培优提升练(一) 阿伏加德罗常数的应用1.(2022·全国甲卷,11)NA为阿伏加德罗常数的值,下列说法正确的是( C )A.25 ℃,101 kPa下,28 L氢气中质子的数目为2.5NAB.2.0 L 1.0 mol·L-1 AlCl3溶液中,Al3+的数目为2.0NAC.0.20 mol苯甲酸完全燃烧,生成CO2的数目为1.4NAD.电解熔融CuCl2,阴极增重6.4 g,外电路中通过电子的数目为0.10NA解析:25 ℃、101 kPa不是标准状况,不能用标准状况下的气体摩尔体积计算氢气的物质的量,故A错误;Al3+在溶液中会发生水解生成 Al(OH)3,因此2.0 L 1.0 mol·L-1的AlCl3溶液中Al3+数目小于2.0NA,故B错误;根据碳原子守恒,0.2 mol苯甲酸(C7H6O2)完全燃烧生成1.4 mol CO2,数目为1.4NA,故C正确;电解熔融CuCl2时,阴极反应为 Cu2++2e-![]() Cu,阴极增加的质量为Cu的质量,6.4 g Cu的物质的量为0.1 mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2 mol,数目为0.2NA,故D错误。2.(2021·广东卷,11)设NA为阿伏加德罗常数的值。下列说法正确的是( A )A.1 mol CHCl3含有C—Cl的数目为3NAB.1 L 1.0 mol·L-1的盐酸含有阴离子总数为2NAC.11.2 L NO与11.2 L O2混合后的分子数目为NAD.23 g Na与足量H2O反应生成的H2分子数目为NA解析:CHCl3的结构式为
Cu,阴极增加的质量为Cu的质量,6.4 g Cu的物质的量为0.1 mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2 mol,数目为0.2NA,故D错误。2.(2021·广东卷,11)设NA为阿伏加德罗常数的值。下列说法正确的是( A )A.1 mol CHCl3含有C—Cl的数目为3NAB.1 L 1.0 mol·L-1的盐酸含有阴离子总数为2NAC.11.2 L NO与11.2 L O2混合后的分子数目为NAD.23 g Na与足量H2O反应生成的H2分子数目为NA解析:CHCl3的结构式为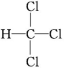 ,故 1 mol CHCl3中含有C—Cl的数目为3NA,A正确;1 L 1.0 mol·L-1的盐酸中含有Cl-的数目为NA,还有极少量的OH-,所以阴离子总数小于2NA,B错误;没有指明在标准状况下,无法进行计算,C错误;23 g Na的物质的量为1 mol,其与足量的水发生反应2Na+2H2O
,故 1 mol CHCl3中含有C—Cl的数目为3NA,A正确;1 L 1.0 mol·L-1的盐酸中含有Cl-的数目为NA,还有极少量的OH-,所以阴离子总数小于2NA,B错误;没有指明在标准状况下,无法进行计算,C错误;23 g Na的物质的量为1 mol,其与足量的水发生反应2Na+2H2O![]() 2NaOH+H2↑,生成H2的物质的量为0.5 mol,即分子数目为0.5NA,D错误。3.(2021·河北卷,7)NA是阿伏加德罗常数的值。下列说法错误的是( C )A.22.4 L(标准状况)氟气所含的质子数为18NAB.1 mol碘蒸气和1 mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NAC.电解饱和食盐水时,若阴、阳两极产生气体的总质量为73 g,则转移电子数为NAD.1 L 1 mol·L-1溴化铵水溶液中N
2NaOH+H2↑,生成H2的物质的量为0.5 mol,即分子数目为0.5NA,D错误。3.(2021·河北卷,7)NA是阿伏加德罗常数的值。下列说法错误的是( C )A.22.4 L(标准状况)氟气所含的质子数为18NAB.1 mol碘蒸气和1 mol氢气在密闭容器中充分反应,生成的碘化氢分子数小于2NAC.电解饱和食盐水时,若阴、阳两极产生气体的总质量为73 g,则转移电子数为NAD.1 L 1 mol·L-1溴化铵水溶液中N![]() 与H+离子数之和大于NA解析:22.4 L(标准状况)氟气的物质的量为1 mol,则其所含的质子数为18NA,A说法正确;反应 H2+I2
与H+离子数之和大于NA解析:22.4 L(标准状况)氟气的物质的量为1 mol,则其所含的质子数为18NA,A说法正确;反应 H2+I2![]() 2HI为可逆反应,则1 mol H2(g)和1 mol I2(g)充分反应生成的HI分子数小于2NA,B说法正确;电解饱和食盐水时,阴、阳两极产生的n(H2)∶n(Cl2)=1∶1,当H2和Cl2的总质量为 73 g 时,产生2 g H2、71 g Cl2,则H2的物质的量为1 mol,Cl2的物质的量为1 mol,转移电子数为2NA,C说法错误;溴化铵水溶液中存在电荷守恒
2HI为可逆反应,则1 mol H2(g)和1 mol I2(g)充分反应生成的HI分子数小于2NA,B说法正确;电解饱和食盐水时,阴、阳两极产生的n(H2)∶n(Cl2)=1∶1,当H2和Cl2的总质量为 73 g 时,产生2 g H2、71 g Cl2,则H2的物质的量为1 mol,Cl2的物质的量为1 mol,转移电子数为2NA,C说法错误;溴化铵水溶液中存在电荷守恒![]() )+c(H+)=c(Br-)+c(OH-),c(Br-)=1 mol·L-1,则c(N
)+c(H+)=c(Br-)+c(OH-),c(Br-)=1 mol·L-1,则c(N![]() )+c(H+)>1 mol·L-1,故1 L 1 mol·L-1溴化铵水溶液中N
)+c(H+)>1 mol·L-1,故1 L 1 mol·L-1溴化铵水溶液中N![]() 与H+离子数之和大于NA,D说法正确。4.(2021·湖南卷,5)NA为阿伏加德罗常数的值。下列说法正确的是( D )A.18 g
与H+离子数之和大于NA,D说法正确。4.(2021·湖南卷,5)NA为阿伏加德罗常数的值。下列说法正确的是( D )A.18 g ![]() O含有的中子数为10NAB.0.1 mol·L-1 HClO4溶液中含有的H+数为0.1NAC.2 mol NO与1 mol O2在密闭容器中充分反应后的分子数为2NAD.11.2 L CH4和22.4 L Cl2(均为标准状况)在光照下充分反应后的分子数为1.5NA解析:1个18O原子含有10个中子,H原子不含中子,所以每个
O含有的中子数为10NAB.0.1 mol·L-1 HClO4溶液中含有的H+数为0.1NAC.2 mol NO与1 mol O2在密闭容器中充分反应后的分子数为2NAD.11.2 L CH4和22.4 L Cl2(均为标准状况)在光照下充分反应后的分子数为1.5NA解析:1个18O原子含有10个中子,H原子不含中子,所以每个![]() O分子中含有10个中子,
O分子中含有10个中子,![]() O的相对分子质量为20,故18 g
O的相对分子质量为20,故18 g ![]() O的物质的量为0.9 mol,则18 g
O的物质的量为0.9 mol,则18 g ![]() O中含有的中子数为9NA,A错误;HClO4为强酸,在溶液中完全电离,则 0.1 mol·L-1 HClO4溶液中H+的物质的量浓度为0.1 mol·L-1,由于题中未给出溶液体积,所以无法计算H+的数目,B错误;2 mol NO与 1 mol O2恰好完全反应生成2 mol NO2,由于存在平衡2NO2
O中含有的中子数为9NA,A错误;HClO4为强酸,在溶液中完全电离,则 0.1 mol·L-1 HClO4溶液中H+的物质的量浓度为0.1 mol·L-1,由于题中未给出溶液体积,所以无法计算H+的数目,B错误;2 mol NO与 1 mol O2恰好完全反应生成2 mol NO2,由于存在平衡2NO2![]() N2O4,所以充分反应后容器中的分子数小于2NA,C错误;甲烷与氯气发生取代反应,反应前后反应物与生成物的物质的量之和不变,则反应后的分子数为
N2O4,所以充分反应后容器中的分子数小于2NA,C错误;甲烷与氯气发生取代反应,反应前后反应物与生成物的物质的量之和不变,则反应后的分子数为![]() ×NA mol-1=1.5NA,D正确。5.(不定项)若用NA表示阿伏加德罗常数的值,下列叙述错误的是( D )A.142 g Na2SO4和Na2HPO4的固体混合物中所含阴、阳离子的总数目为3NAB.锌与某浓度的浓硫酸反应,生成SO2和H2的混合气体22.4 L(标准状况),锌失去电子数目为2NAC.标准状况下,22.4 L甲烷和乙烯混合物中含碳氢共价键数目为4NAD.0.1 mol·L-1 的CH3COONH4溶液显中性,1 L该溶液中含CH3COO-数等于0.1NA解析:Na2HPO4中含有2个Na+和1个HP
×NA mol-1=1.5NA,D正确。5.(不定项)若用NA表示阿伏加德罗常数的值,下列叙述错误的是( D )A.142 g Na2SO4和Na2HPO4的固体混合物中所含阴、阳离子的总数目为3NAB.锌与某浓度的浓硫酸反应,生成SO2和H2的混合气体22.4 L(标准状况),锌失去电子数目为2NAC.标准状况下,22.4 L甲烷和乙烯混合物中含碳氢共价键数目为4NAD.0.1 mol·L-1 的CH3COONH4溶液显中性,1 L该溶液中含CH3COO-数等于0.1NA解析:Na2HPO4中含有2个Na+和1个HP![]() ,142 g固体中n(Na2HPO4)=
,142 g固体中n(Na2HPO4)=![]() =
=![]() =1 mol,则阴、阳离子总数目为3NA。Na2SO4中含有2个Na+和1个S
=1 mol,则阴、阳离子总数目为3NA。Na2SO4中含有2个Na+和1个S![]() ,142 g固体中n(Na2SO4)=
,142 g固体中n(Na2SO4)=![]() =
=![]() =1 mol,则阴、阳离子总数目为3NA,A正确;反应中关系式为SO2~2e-、H2~2e-,则电子的总物质的量为2[n(SO2)+n(H2)]=2 mol,反应中转移的电子总数目为2NA,B正确;关系式有CH4~4C-H、CH2=CH2~4C-H,则 n(C-H)=4n(CH4)+ 4n(CH2
=1 mol,则阴、阳离子总数目为3NA,A正确;反应中关系式为SO2~2e-、H2~2e-,则电子的总物质的量为2[n(SO2)+n(H2)]=2 mol,反应中转移的电子总数目为2NA,B正确;关系式有CH4~4C-H、CH2=CH2~4C-H,则 n(C-H)=4n(CH4)+ 4n(CH2![]() CH2)=4 mol,C—H的总数目为4NA,C正确;溶液中CH3COO-发生水解,得到的物料守恒式为 c(CH3COOH)+c(CH3COO-)=0.1 mol/L,1 L该溶液中含 CH3COO-数小于 0.1NA,D错误。6.(不定项)设NA为阿伏加德罗常数的值,下列说法正确的是( CD )A.1.12 L甲烷中含有的共价键数目为0.2NAB.0.5 mol熔融的NaHSO4中含有的离子数目为1.5NAC.5.6 g铁粉与足量稀硝酸充分反应,转移电子数为0.3NAD.4.6 g NO2和N2O4的混合气体中所含氮原子数目为0.1NA解析:熔融的 NaHSO4 中含有的离子为钠离子和硫酸氢根离子,所以0.5 mol熔融的NaHSO4 中含有的离子数目为NA,B错误;5.6 g铁粉的物质的量为0.1 mol,与足量稀硝酸充分反应生成硝酸铁,则转移电子数为0.3NA,C正确;NO2和N2O4的最简式均为NO2,4.6 g NO2和N2O4的混合气体可以看作是4.6 g NO2,4.6 g NO2的物质的量为 0.1 mol,则所含氮原子数目为0.1NA,D正确。
CH2)=4 mol,C—H的总数目为4NA,C正确;溶液中CH3COO-发生水解,得到的物料守恒式为 c(CH3COOH)+c(CH3COO-)=0.1 mol/L,1 L该溶液中含 CH3COO-数小于 0.1NA,D错误。6.(不定项)设NA为阿伏加德罗常数的值,下列说法正确的是( CD )A.1.12 L甲烷中含有的共价键数目为0.2NAB.0.5 mol熔融的NaHSO4中含有的离子数目为1.5NAC.5.6 g铁粉与足量稀硝酸充分反应,转移电子数为0.3NAD.4.6 g NO2和N2O4的混合气体中所含氮原子数目为0.1NA解析:熔融的 NaHSO4 中含有的离子为钠离子和硫酸氢根离子,所以0.5 mol熔融的NaHSO4 中含有的离子数目为NA,B错误;5.6 g铁粉的物质的量为0.1 mol,与足量稀硝酸充分反应生成硝酸铁,则转移电子数为0.3NA,C正确;NO2和N2O4的最简式均为NO2,4.6 g NO2和N2O4的混合气体可以看作是4.6 g NO2,4.6 g NO2的物质的量为 0.1 mol,则所含氮原子数目为0.1NA,D正确。
相关试卷
这是一份2024届高考化学一轮复习 课时跟踪检测(八) 阿伏加德罗常数的应用 (含答案),共11页。试卷主要包含了NA为阿伏加德罗常数的值,用NA表示阿伏加德罗常数的值,设NA为阿伏加德罗常数的值,雄黄与雌黄在古代均曾入药等内容,欢迎下载使用。
这是一份新高考2024版高考化学一轮复习微专题小练习专练1阿伏加德罗常数的应用,共5页。
这是一份全国通用高考化学一轮复习专练1阿伏加德罗常数的应用含答案,共7页。试卷主要包含了单项选择题,不定项选择题等内容,欢迎下载使用。









