

2023届广东省广州市高三一模考试化学试题含解析
展开广东省广州市2023届高三一模考试化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.文物记载着中华文明的灿烂成就,下列文物主要由合金材料制成的是
文物
选项
A.圆雕玉舞人
B.透雕重环玉佩
C.朱雀青铜顶饰
D.炫纹贯耳瓷壶
A.A B.B C.C D.D
【答案】C
【详解】A.玉是特殊的石头,不是合金材料, A错误;
B.玉佩不属于合金材料,B错误;
C.青铜属于铜合金,C正确;
D.瓷壶属于硅酸盐材料,D错误;
故选C。
2.中国空间站建造成功、神舟系列飞船顺利往返,均展示了我国科技发展的巨大成就。下列相关叙述正确的是
A.空间站太阳翼伸展关键部件采用碳化硅材料,属于无机非金属材料
B.核心舱太阳能电池采用砷化镓()材料,属于金属材料
C.飞船火箭使用偏二甲肼作燃料,属于烃类
D.飞船返回舱使用氮化硅耐高温结构材料,属于分子晶体
【答案】A
【详解】A.属于无机非金属材料,A正确;
B.属于半导体材料,B错误;
C.烃只含碳和氢,不属于烃类,C错误;
D.氮化硅耐高温,属于共价晶体,D错误;
故选A。
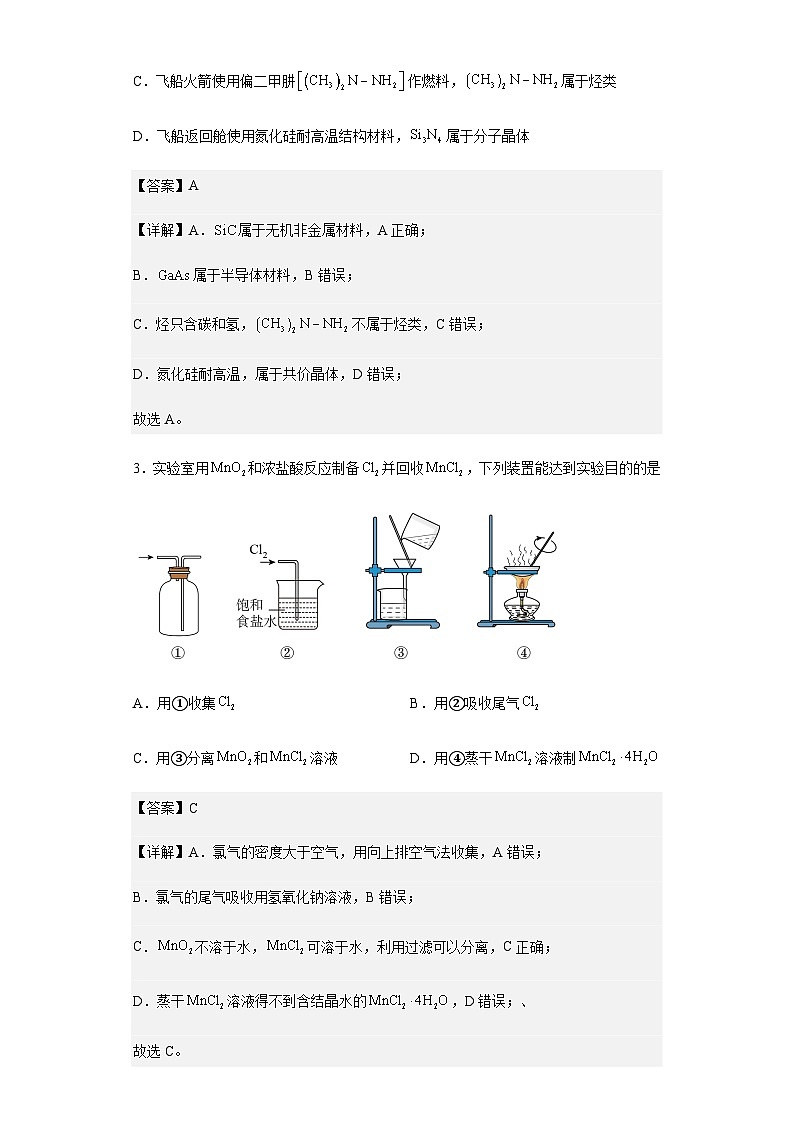
3.实验室用和浓盐酸反应制备并回收,下列装置能达到实验目的的是
A.用①收集 B.用②吸收尾气
C.用③分离和溶液 D.用④蒸干溶液制
【答案】C
【详解】A.氯气的密度大于空气,用向上排空气法收集,A错误;
B.氯气的尾气吸收用氢氧化钠溶液,B错误;
C.不溶于水,可溶于水,利用过滤可以分离,C正确;
D.蒸干溶液得不到含结晶水的,D错误;、
故选C。
4.四氯化锗()是光导纤维的常用掺杂剂,锗与硅同族。下列说法不正确的是
A.基态原子价层电子排布式为 B.的熔点比低
C.的空间构型为正四面体 D.第一电离能大小:
【答案】B
【详解】A.锗是32号元素,基态原子价层电子排布式为,A正确;
B.与晶体都属于分子晶体,的相对分子质量大,晶体内的分子间作用力大,则的熔点比高,B错误;
C.分子中原子形成了4个键,孤电子对数=,价层电子对数为4,中心原子的杂化类型为sp3,分子的空间构型为正四面体,C正确;
D.元素非金属性越强,其第一电离能越大,非金属性大小为,则第一电离能大小:,D正确;
故选B。
5.以熔融盐(、)为电解液,以石墨为阳极,电解和获取电池材料,下列说法正确的是
A.阳极上被还原 B.阴极发生的反应为
C.电解时,阳离子向阳极移动 D.理论上每生成电路中转移电子
【答案】D
【详解】A.石墨为阳极,电解池阳极发生氧化反应,A错误;
B.和为电池阴极,发生还原反应,反应方程式为++8e-=TiSi+4O2-,B错误;
C.电解时阳离子向阴极移动,阴离子向阳极移动,C错误;
D.由阴极电极反应式可知,每生成,电路中转移8mol电子,D正确;
故选D。
6.劳动开创未来。下列劳动项目与所述的化学知识没有关联的是
选项
劳动项目
化学知识
A
工人用明矾处理废水
是两性氢氧化物
B
工人用消毒自来水
具有强氧化性
C
雕刻师用氢氟酸刻蚀石英制作艺术品
可与反应
D
酿酒师在葡萄酒中添加适量的二氧化硫
可以杀菌和抗氧化
A.A B.B C.C D.D
【答案】A
【详解】A.明矾处理废水,利用胶体的吸附性,与Al(OH)3是两性氢氧化物无关,A错误;
B.具有强氧化性,可用消毒自来水,B正确;
C.可与反应,可用氢氟酸刻蚀玻璃,C正确;
D.可以杀菌和抗氧化,可在葡萄酒中添加适量的二氧化硫,D正确;
故选A。
7.苯胺()是一种有机弱碱,可与盐酸反应生成盐酸盐()。下列叙述正确的是
A.中碳原子的杂化轨道类型为
B.水溶液加水稀释,降低
C.水溶液中:
D.在水中的电离方程式为:
【答案】D
【详解】A.苯环内碳原子都采用sp2杂化,A错误;
B.盐酸盐()属于强酸弱碱盐,水解显酸性,加水稀释,水解程度增大,但由于溶液被稀释,OH-浓度减小,增大,B错误;
C.水溶液中存在电荷守恒:,C错误;
D.盐酸盐()在水中完全电离,电离方程式为:,D正确;
故选D。
8.将铜丝插入浓硝酸中进行如图所示的实验,下列说法正确的是
A.装置a中出现红棕色气体,只体现的酸性
B.一段时间后抽出铜丝,向装置b注入水,b中气体红棕色变浅
C.注入水后装置b中铜片表面产生气泡,说明与硝酸生成
D.装置c用吸收尾气,说明和均是酸性氧化物
【答案】B
【详解】A.铜与浓硝酸反应生成红棕色二氧化氮气体和硝酸铜,体现了硝酸的强氧化性和酸性,A错误;
B.一段时间后抽出铜丝,向装置b注入水,b中气体红棕色变浅,二氧化氮与水反应生成硝酸和一氧化氮,B正确;
C.注入水后装置b中铜片表面产生气泡,与稀硝酸反应生成NO气体,C错误;
D.酸性氧化物是指和水反应只能生成对应价态的酸、或和碱反应只能生成盐和水的氧化物,和均不是酸性氧化物,D错误;
故选B。
9.2022年我国科学家首次在月球上发现一种硅酸盐矿物,该物质含有X、Y、Z、W、E五种主族元素,原子序数依次增大且均不大于20,X、W为非金属元素,Y、Z、E为金属元素,Y的最高正化合价为,Z和E同族。下列说法不正确的是
A.原子半径:
B.X和Y可形成含有非极性键的离子化合物
C.Y、Z、E的最高价氧化物对应的水化物均为强碱
D.简单气态氢化物稳定性:
【答案】C
【分析】硅酸盐矿物中,X、W为非金属元素,分别为O和Si,Y、Z、E为金属元素,Y的最高正化合价为,Y可能为或者,因为原子序数逐渐增大,所以Y只能为 Na,Z为Mg,E为Ca。
【详解】A.根据原子半径大小的比较,Na、Mg、Ca的半径大小为:,A正确;
B.O和Na能形成含有非极性键的离子化合物,B正确;
C.Na、Mg、Ca的最高价氧化物的水化物中,和为强碱,为中强碱,C错误;
D.因为O的非金属性强于Si,所以氢化物的稳定性,D正确;
故C。
10.载人航天器中的物质和能量资源都十分宝贵,我国科学家进行了如图所示的氧循环研究,实现了空间站中氧气的再生。下列说法不正确的是
A.用于循环的氢原子利用率为100%
B.太阳能可作为反应①和②的能量来源
C.反应①为
D.等物质的量的和含有的电子数相同
【答案】A
【详解】A.反应①为,反应②2H2O2H2+O2,氢原子部分进入甲烷,用于循环的氢原子利用率达不到100%,A错误;
B.太阳能可作为反应①和②的能量来源,B正确;
C.根据得失电子守恒配平方程,反应①为,C正确;
D.水和甲烷都是常见的10电子微粒,等物质的量的和含有的电子数相同,D正确;
故选A。
11.下列物质性质实验对应的离子方程式书写正确的是
A.铁与稀硫酸反应:
B.溶液中通入硫化氢:
C.通入酸性溶液中:
D.溶液中加入稀硫酸:
【答案】D
【详解】A.铁与稀硫酸反应生成硫酸亚铁和氢气,其离子方程式为,A错误;
B.溶液中通入硫化氢生成CuS沉淀,硫化氢为弱酸在离子方程式中不能拆开,其离子方程式为,B错误;
C.通入酸性溶液反应生成Mn2+和SO,根据得失电子守恒配平可知,其离子方程式为,C错误;
D.溶液中加入稀硫酸反应生成S和SO2,其离子方程式为,D正确;
故选D。
12.在催化下醇的氧化氰化反应如图所示。下列叙述正确的是
A.熔点: B.键角:
C.I和II分子中键数目相同 D.II含有的元素中的电负性最大
【答案】A
【详解】A.I中含有羟基,分子之间含有氢键,熔点较高,A正确;
B.分子中有2对孤电子对,只有1对故电子对,孤电子对与成键电子对的排斥力大于成键电子对之间的排斥力,所以键角:,B错误;
C.一个单键,1个键,一个双键,1个键和1个键,一个三键,一个键个2个键,所以I中的键数为20,II中的键数为19,二者不相同,C错误;
D.O的电负性大于N的,所以II含有的元素中O的电负性最大,D错误;
故选A。
13.恒容密闭容器中,以硫()与为原料制备,受热分解成气态,发生反应 。的平衡转化率、的体积分数随温度的变化曲线如图所示。下列说法正确的是
A.
B.温度升高,分解率增大,体积分数增大
C.向平衡体系中充入惰性气体,平衡向右移动
D.其他条件相同,体积分数越大,平衡转化率越小
【答案】B
【详解】A.由图像可看出,温度升高,CH4的平衡转化率降低,S2的体积分数升高说明升温时,平衡向左移动,所以正反应方向是放热的,即<0,选项A错误;
B.因为S8分解成S2需要吸收热量,S8(g) 4S2(g) >0,所以升温时,平衡右移,S8分解率增大,S2体积分数增大,选项B正确;
C.向恒温恒容的平衡体系中,通入惰性气体,由于与反应有关的气体物质的物质的量浓度均未变化,所以Q=K,平衡不移动,选项C错误;
D.其他条件不变时,S2体积分数增大,即c(S2)越大,则平衡向右进行的程度越大,CH4的平衡转化率越大,选项D错误;
答案选B。
14.下列实验对应的现象和结论都正确的是
选项
实验
现象
结论
A
向食品脱氧剂样品(含还原铁粉)中加入硫酸后滴加酸性溶液
紫红色褪去
食品脱氧剂样品中含
B
向溶液中滴入溶液,再滴加溶液
加入后溶液变成血红色
既有氧化性又有还原性
C
向溶液加入铜片
溶液变蓝、有黑色固体出现
金属铁比铜活泼
D
向溶液中加入溶液后滴加几滴淀粉溶液
溶液变为蓝色
氧化性:
A.A B.B C.C D.D
【答案】D
【详解】A.向食品脱氧剂样品(含还原铁粉)中加入硫酸后,铁粉会与硫酸反应生成硫酸亚铁,酸性溶液为强氧化剂,会氧化亚铁离子,则滴加酸性溶液,紫红色褪去,不能说明食品脱氧剂样品中含,A错误;
B.向溶液中滴入溶液,无明显现象,再滴加溶液,会将亚铁离子氧化为铁离子,则加入后溶液变成血红色,说明有还原性,B错误;
C.向溶液加入铜片会发生反应2FeCl3+Cu=2FeCl2+CuCl2,看到溶液变蓝,无黑色固体出现,得到结论为的氧化性大于CuCl2,C错误;
D.向溶液中加入溶液后滴加几滴淀粉溶液,溶液会与溶液反应生成FeCl2和I2,则溶液变为蓝色,得到结论氧化性:,D正确;
故选D。
15.新型Li-Mg双离子可充电电池是一种高效、低成本的储能电池,其工作原理如图所示。放电时电极a的反应为:;下列说法不正确是
A.充电时,极为阴极
B.放电时,从I室向II室迁移
C.放电时,II室溶液的浓度增大
D.每消耗,电极a质量理论上增加
【答案】C
【详解】A.放电时电极a的反应为:,a为正极,为负极,所以充电时为阴极,A正确;
B.放电时I室为负极区,II室为正极区,阳离子向正极移动,所以向II室迁移,B正确;
C.放电时电极a的反应为:,消耗,所以溶液的浓度减小,C错误;
D.放电时发生反应:,当有发生反应时,转移,电极a质量理论上增加,质量为:,D正确;
故选C。
16.以酚酞为指示剂,用溶液滴定一元酸的溶液。溶液中,、分布系数(,比如的分布系数:)随的变化关系如图所示,下列叙述不正确的是
A.曲线①代表,曲线②代表
B.的数量级为
C.滴定过程中,溶液中不断减小
D.滴定终点时,
【答案】C
【详解】A.随着溶液的滴加,HA电离程度增大,溶液中减小、增大,则减小、增大,所以曲线①代表,曲线②代表,曲线③代表pH变化,A正确;
B.由图可知当溶液中时,,,,故的数量级为,B正确;
C.根据电离平衡常数:,,在滴定过程中,不变,减小,增大,C错误;
D.滴定达到终点时,生成,在溶液中发生水解,溶液显碱性,溶液中离子浓度的大小为:,D正确;
故选C。
二、实验题
17.醋酸钠是一种常用的防腐剂和缓冲剂。
(1)配制溶液,需要称量醋酸钠晶体(,)的质量为_______。实验需要的仪器有天平、药匙、玻璃棒、量筒、_______(从下列图中选择,写出名称)。
(2)某小组探究外界因素对水解程度的影响。
甲同学设计实验方案如下(表中溶液浓度均为):
i.实验_______和_______(填序号),探究加水稀释对水解程度的影响;
ii.实验1和3,探究加入对水解程度的影响;
iii.实验1和4,探究温度对水解程度的影响。
序号
温度
1
25℃
40.0
0
0
2
25℃
4.0
0
36.0
3
25℃
20.0
10.0
4
40℃
40.0
0
0
①根据甲同学的实验方案,补充数据:_______。
②实验测得,该结果不足以证明加入促进了的水解。根据_______(填一种微粒的化学式)的浓度增大可以说明加入能促进的水解。
③已知水解为吸热反应,甲同学预测,但实验结果为。实验结果与预测不一致的原因是_______。
(3)小组通过测定不同温度下的水解常数确定温度对水解程度的影响。
查阅资料:,为溶液起始浓度。
试剂:溶液、盐酸、计。
实验:测定40℃下水解常数,完成下表中序号7的实验。
序号
实验
记录的数据
5
取溶液,用盐酸滴定至终点
消耗盐酸体积为
6
测40℃纯水的
7
_______
在50℃和60℃下重复上述实验。
数据处理:40℃,_______(用含、、的计算式表示)
实验结论:,温度升高,促进水解。
【答案】(1) 3.4g 烧杯、胶头滴管、250mL容量瓶
(2) 1 2 0 升高温度促进水的电离导致溶液中氢离子浓度增大
(3) 测定40℃醋酸钠溶液的pH
或
【分析】配制一定物质的量浓度的溶液,所需的步骤有计算、称量、溶解(冷却)、转移、洗涤、定容、摇匀、装瓶贴签;
滴定实验的步骤是:滴定前的准备:滴定管:查漏→洗涤→润洗→装液→调液面→记录,锥形瓶:注液体→记体积→加指示剂;滴定:眼睛注视锥形瓶溶液颜色变化;终点判断:记录数据;数据处理:通过数据进行计算;
【详解】(1)配制溶液,需要称量醋酸钠晶体的质量为。实验需要的仪器有天平、药匙、玻璃棒、量筒、烧杯、胶头滴管、250mL容量瓶;
(2)探究加水稀释对水解程度的影响,则实验中变量为醋酸钠的浓度,故实验1和2,探究加水稀释对水解程度的影响;
①实验1和3,探究加入对水解程度的影响;不能改变醋酸根的浓度,故0;
②醋酸水解方程式为:,铵根离子水解方程式为:;铵根离子水解会导致溶液中酸性增强,实验测得,该结果不足以证明加入促进了的水解,实验中可以根据的浓度增大可以说明加入能促进的水解;
③已知水解为吸热反应,甲同学预测,但实验结果为。实验结果与预测不一致的原因是水的电离也为吸热过程,升高温度促进水的电离导致溶液中氢离子浓度增大;
(3)实验为通过测定不同温度下的水解常数确定温度对水解程度的影响,则实验7需要测定40℃醋酸钠溶液的pH;取溶液,用盐酸滴定至终点,消耗盐酸体积为,和HCl以1:1反应,此时的起始浓度=,40℃纯水的pH=b,则,;实验7所得溶液的pH=c,则,则=或。
三、工业流程题
18.铋的化合物在电催化和光催化领域都有广泛应用。一种从含铋矿渣(主要成分是、、、、等)中提取高纯的工艺如下:
已知:
①乙酰胺()有臭味、有毒,熔点为82.3℃,沸点为221℃,可溶于水。
②常温下,, 。
③该工艺条件下,相关金属离子形成氢氧化物沉淀的范围如下:
离子
开始沉淀的
1.5
3.6
4.5
沉淀完全的
3.2
4.7
6.7
回答下列问题:
(1)中的的化合价为,则的化合价是_______。
(2)“沉铋”时加入溶液,转化为沉淀的离子方程式是_______。往“沉铋”所得滤液中加入铁粉可回收其中的_______(填化学式)金属。
(3)“洗涤”时先用水洗,再用稀硫酸洗涤。用稀硫酸洗涤的目的是为了除去滤饼中的_______(填化学式)杂质。
(4)“转化”分两步进行:第一步转化为,反应的离子方程式为_______;第二步受热分解,。常温下,当恰好完全转化成时,溶液中浓度为,则此时溶液的为_______。
(5)“合成”所得乙酰胺的水溶液经_______。(填操作)可获得乙酰胺固体,以再生硫代乙酰胺()。
(6)钼酸铋()可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为,,,晶胞棱边夹角均为90°。
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。已知原子1的坐标为,则原子2的坐标为_______。
②设阿伏加德罗常数的值为,的式量为,则晶体的密度为_______ (列计算式)。
【答案】(1)+3
(2)
(3)
(4) 13
(5)蒸发浓缩,冷却结晶,过滤,洗涤,干燥
(6)
【分析】铋矿渣(主要成分是、、、、等),加入盐酸酸浸,滤渣我,溶液中含有、、、,加入调节,滤饼中含有和,再加入生成,进而转化为,用合成,最终得到产品。
【详解】(1)中的的化合价为,O的化合价为-2,根据化合物中正负化合价为0,则的化合价是+3;
(2)“沉铋”时加入溶液,转化为沉淀的离子方程式是:;“沉铋”所得滤液中含有、、、,加入铁粉,发生反应:,可回收其中的;
(3)加入溶液,调节,滤饼中含有和,用稀硫酸洗涤的目的是为了除去滤饼中的;
(4)加入溶液,转化为,反应的离子方程式为:,已知反应的,同时乘,,,当浓度为,,;
(5)乙酰胺()熔点为82.3℃,可溶于水,水溶液经蒸发浓缩,冷却结晶,过滤,洗涤,干燥,可得乙酰胺固体;
(6)根据晶胞的结构,原子1的坐标为,则原子2的坐标为:;根据晶胞的结构,Bi原子为:,Mo原子为:8,所以晶胞的相对质量的,晶胞密度为:。
四、原理综合题
19.乙醇可以通过部分氧化制氢气,涉及的相关反应方程式如下:
a)
b)
c)
d)
(1)若发生反应,可提高乙醇中氢原子的利用率,反应的_______(用代数式表示)。
(2)用平衡分压代替平衡浓度时,平衡常数可表示为,各反应的随温度的变化如图1所示。
①以上反应中,属于吸热反应的有_______(填字母)。
②平衡常数大于时可认为反应完全,则时,反应完全进行的有_______(填字母)。
(3)恒压条件下往反应容器中通入和少量,平衡时体系中各物质(、、、、)的物质的量分数随温度的变化如图2所示。
①图中表示的曲线为_______。(填“”或“”)。
②下列说法正确的是_______(填编号)。
A.当气体密度不再发生变化时,反应达到平衡状态
B.温度升高,反应的增大,减小
C.达到平衡时分离出部分,反应c的平衡常数增大
D.加入稀有气体,重新达到平衡时的物质的量增加
③下达到平衡时和均反应完全,、和的物质的量分数分别为0.20、0.32、0.12,则平衡时的物质的量为_______,反应c的平衡常数K=_____。
【答案】(1)
(2) ad ab
(3) n AD
【详解】(1)由盖斯定律可知a+b+d可得反应 ;
(2)①由图示知随着温度升高,bc反应的平衡常数减小,ad平衡常数增大,故ad反应属于吸热,升高温度平衡正向移动;
②平衡常数大于即lgKp>5时可认为反应完全,则时,反应完全进行的有ab。
(3)①ad反应属于吸热,升高温度平衡正向移动,故CO的含量增大,曲线n为CO的曲线;
②A.该体系只有气体参与反应,质量守恒,m总不变,反应体系是气体物质的量增大的反应,恒压体系容器的体积增大,故密度是个变量,当气体密度不再发生变化时,反应达到平衡状态,选项A正确;
B.温度升高,反应的、均增大,选项B错误;
C.平衡常数是个随温度变化的常数,达到平衡时分离出部分,反应c的平衡常数不变,选项C错误;
D.恒压环境中加入稀有气体,容器体积增大,反应体系的分压减小,ad平衡正向移动,重新达到平衡时的物质的量增加,选项D正确;
答案选AD;
③、和的物质的量分数分别为0.20、0.32、0.12,则一氧化碳和二氧化碳的物质的量分数之和为1-(0.2+0.32+0.12)=0.36,设平衡时各物质总的物质的量为n总,根据碳元素守恒可知(0.20+0.36)n总=4,故n总=mol,则氢气的物质的量为0.32mol=mol;由图可知,下达到平衡时CO和CO2的物质的量相等,则n(CO)= n(CO2)=0.36n总=mol,n(H2O)=0.12 n总=mol,c(CH4)=0.2 n总=mol,反应c的平衡常数K=。
五、有机推断题
20.化合物VII是一种用于缓解肌肉痉挛的药物,其合成路线如下:
回答下列问题:
(1)中官能团的名称是_______。VI→VII的反应类型是_______。
(2)中手性碳原子的个数是_______ (代表阿伏加德罗常数的值)。化合物 的分子式是_______。
(3)已知 (表示,则III的结构简式是_______。
(4)V→VI的化学方程式是_______。
(5)符合下列条件的化合物II的同分异构体有_______种。
a.含有结构单元
b.含有
c.苯环上有两个取代基
(6)参考上述信息,写出以苯甲醇和为原料制备的合成路线_____。
【答案】(1) 碳碳双键 取代反应
(2) 1
(3)
(4)2 +2
(5)3
(6)
【分析】物质I和在一定条件下生成物质II,根据物质IV的结构,和III的分子式,可以推出物质III的结构为: ,物质IV发生催化氧化生成物质V,再被氧化生成VI,最后发生酯化反应得到产物。
【详解】(1)含有的官能团为:碳碳双键,根据分析,VI→VII的反应类型是取代反应;
(2)根据物质IV的结构式 ,中手性碳原子的个数是1; 的分子式为:;
(3)根据以上分析,物质III的结构式为: ;
(4)物质V被氧化生成VI,反应的方程式为:2 +2
(5)化合物II的结构为: a.含有结构单元 ,b.含有,c.苯环上有两个取代基的结构有:3种;
(6)由 氧化生成 , 和反应,生成 ,再催化氧化,生成产品 ,流程为:。
广东省广州市2021届高三下学期二模考试化学试题(含解析): 这是一份广东省广州市2021届高三下学期二模考试化学试题(含解析),共24页。试卷主要包含了单选题,实验题,工业流程题,原理综合题,结构与性质,有机推断题等内容,欢迎下载使用。
2023届广东省湛江市高三一模考试化学试题含解析: 这是一份2023届广东省湛江市高三一模考试化学试题含解析,共25页。试卷主要包含了单选题,实验题,工业流程题,原理综合题,有机推断题等内容,欢迎下载使用。
2023届上海市黄浦区高三一模考试化学试题含解析: 这是一份2023届上海市黄浦区高三一模考试化学试题含解析,共27页。试卷主要包含了单选题,结构与性质,原理综合题,实验题,有机推断题等内容,欢迎下载使用。












