
2022-2023学年山西省运城市康杰中学高二下学期3月月考化学试题(Word版)
展开2022-2023学年高二年级第二学期第一次月考
化学试题
2023年3月
可能用到的相对原子质量 : H:1 C:12 O:16 P:31 S:32 Co:59 Cu:64
第Ⅰ卷 (选择题,共54分)
一、选择题(本题包括18小题,每小题3分,共54分,每小题只有一个选项符合题意)
1.2021年空间站“天和”号核心舱发射成功。下列有关核心舱所用材料描述正确的是
选项 | 材料 | 相关描述 |
A | 舱体钛合金外壳 | 钛合金比纯钛熔点高、硬度大 |
B | 推力器氮化硼陶瓷部件 | 耐高温、耐腐蚀 |
C | 操控台聚碳酸酯部件 | 属于无机非金属材料 |
D | 智能控制芯片 | 主要成分是二氧化硅 |
A.A B.B C.C D.D
2.下列关于物质特殊聚集状态结构的叙述中,错误的是
A.液晶具有液体的流动性,在某些物理性质方面具有类似晶体的各向异性
B.氧化镁晶体中离子键的百分数为50%,氧化镁晶体是一种过渡晶体
C.等离子体的基本构成粒子只有阴、阳离子
D.石墨晶体属于混合型晶体
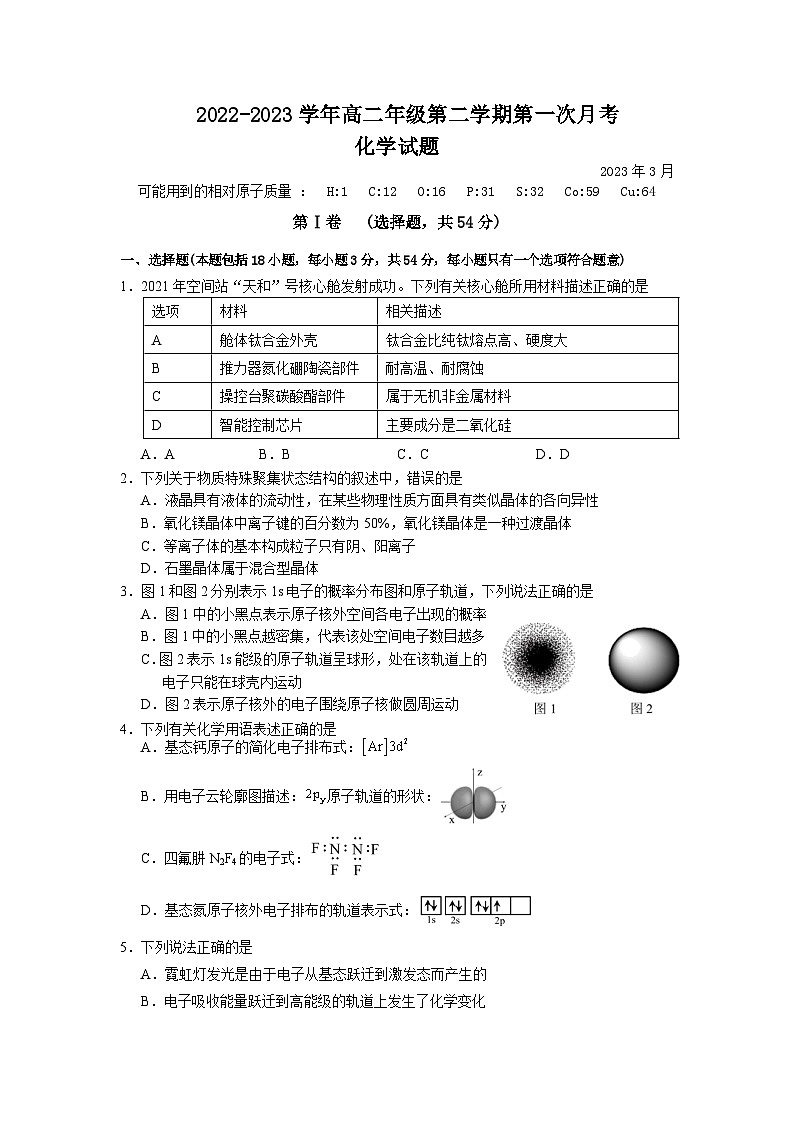
3.图1和图2分别表示1s电子的概率分布图和原子轨道,下列说法正确的是
A.图1中的小黑点表示原子核外空间各电子出现的概率
B.图1中的小黑点越密集,代表该处空间电子数目越多
C.图2表示1s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动
D.图2表示原子核外的电子围绕原子核做圆周运动
4.下列有关化学用语表述正确的是
A.基态钙原子的简化电子排布式:
B.用电子云轮廓图描述:原子轨道的形状:
C.四氟肼N2F4的电子式:
D.基态氮原子核外电子排布的轨道表示式:
5.下列说法正确的是
A.霓虹灯发光是由于电子从基态跃迁到激发态而产生的
B.电子吸收能量跃迁到高能级的轨道上发生了化学变化
C.不同种原子由激发态向基态跃迁时发出的光的颜色一定相同
D.焰色反应中颜色是金属原子电子从激发态跃迁到基态时产生的光谱谱线的颜色
6.下列有关原子轨道的说法正确的是
A.在K能层中,有自旋相反的两条轨道
B.N能层中有4s、4p、4d、4f四个能级,共16个轨道,可容纳32种运动状态的电子
C.基态原子电子能量的高低顺序为:
D.3p能级上只有一个空轨道的原子和3p能级上有两个未成对电子的原子对应为同一元素
7.轨道电子排布达到半充满的元素,其原子序数是
A.33 B.35 C.51 D.83
8.下表中关于各微粒的描述完全正确的一项是
选项 | A | B | C | D |
分子或离子的化学式 | H2F+ | PCl3 | NO | BH |
中心原子的杂化轨道类型 | sp | sp3 | sp2 | sp3 |
VSEPR模型名称 | 直线形 | 四面体形 | 平面三角形 | 正四面体形 |
分子或离子的空间结构 | 直线形 | 正四面体形 | V形 | 三角锥形 |
A.A B.B C.C D.D
9.下列现象与氢键有关的是
①NH3的熔、沸点比PH3的高 ②丙三醇的黏度大于乙醇的黏度
③冰的密度比液态水的密度小 ④戊醇在水中的溶解度比乙醇明显减小
⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
⑥HF的稳定性强于同主族其他元素的氢化物的稳定性
A.①④⑤⑥ B.①②③⑤ C.①③⑤⑥ D.①②③⑥
10.已知:Q、R、X、Y、Z五种元素的原子序数依次递增,Z的原子序数为29,其余均为短周期主族元素;Y原子价层电子排布式为msnmpn;R原子核外的L层电子数为奇数;Q、X原子p轨道的电子数分别为2和4。下列说法中正确的是
A.元素的第一电离能:X>R>Q B.电负性:X>R>Q
C.基态Z2+的电子排布式:1s22s22p63s23p63d8 D.原子半径:Y>X>R>Q
11.下列图象表示正确的是
A. B.
C. D.
12.为阿伏加德罗常数的值,下列说法正确的是
①标准状况下,2.24 L和的混合气体中含有的π键数约为
②32 g 单质(分子结构:)中,S—S数目为
③1 mol HCN中含有π键的数目为
④6.2 g白磷所含σ键的数目为
⑤0.25 mol XeF6中氙的价层电子对数为1.5NA
⑥46 g CH3OCH3中sp3杂化的原子数为2NA
⑦1 mol NH4BF4中配位键的数目为2NA
A.①③⑤⑦ B.①②④⑤ C.①④⑦ D.①②③⑥
13.下列物质的熔、沸点高低顺序正确的是
A.金刚石>晶体硅>碳化硅 B.CI4>CBr4>CCl4>CF4
C.MgO>CO2>H2O D.金刚石>生铁>钠>纯铁
14.下列关于分子的结构和性质的描述中,错误的是
A.和分子均为三角双锥结构,两者的沸点关系为:
B.乳酸()分子中含有一个手性碳原子
C.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
D.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
15.的配位化合物较稳定且运用广泛。它可与、、、等形成配离子使溶液显色。如:显浅紫色的、红色的、黄色的、无色。某同学按如下步骤完成实验:
已知与、在溶液中存在以下平衡:(红色);(无色)
下列说法不正确的是
A.Ⅰ中溶液呈黄色可能是由水解产物的颜色引起的
B.与的配位能力强于
C.为了能观察到溶液Ⅰ中的颜色,可向该溶液中加入稀盐酸
D.向溶液Ⅲ中加入足量的KSCN固体,溶液可能再次变为红色
16.“杯酚”()能够分离提纯和,其原理如图所示。下列说法错误的是
A.分离过程中“杯酚”能循环利用 B.“操作1”是过滤,“操作2”是分液
C.“杯酚”与形成了超分子 D.该过程体现了超分子的“分子识别”功能
17.氨硼烷(NH3·BH3)是一种高性能固体储氢材料在催化剂作用下可发生水解:
3NH3·BH3+6H2O=3NH+B3O+9H2↑,已知B3O的结构为,
下列说法正确的是
A.该反应过程中B原子的杂化方式均为sp3
B.水解产生的H2是氧化产物
C.共价键的键能大小与氨硼烷熔沸点的高低无直接关系
D.NH3中所有原子都满足8电子稳定结构
18.钴的某种氧化物广泛应用于硬质合金、超耐热合金、绝缘材料和磁性材料的生产,其晶胞结构如图所示。下列有关说法正确的是
A.该氧化物的化学式为
B.晶胞中的配位数为12
C.根据晶体类型推测,该物质熔点低于硫
D.若该氧化物的密度为,阿伏加德罗常数为NAmol-1,则晶胞中两个间的最短距离是
第Ⅱ卷 (非选择题,共46分)
二、非选择题(共46分)
19.(13分)锂-磷酸氧铜电池正极的活性物质是,可通过下列反应制备:回答下列问题:
(1)铜元素的基态原子价电子排布式为______。
(2)的空间结构是______。
(3)第一电离能:N______(填“>”或“<”)O,原因为______。
(4)依据的电离特点,推测分子中NH3与H2O之间的氢键可表示为______(填序号)。
①N-H…O ②H-O…H ③O-H…N
(5)Cu和S两种元素形成某种晶体的晶胞结构如图所示,假设该晶体的晶胞边长为a pm。
①Cu和S之间的最近距离为______pm。
②设为阿伏加德罗常数的值,该晶胞的密度为______(用含和a的代数式表示)。
20.(10分)(铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是,含少量、、等杂质)为原料制备铋酸钠的流程如下:
请回答下列问题:
(1)“浸渣”的主要成分是______、______(填化学式)。
(2)检验“酸浸”液中是否含,可选择的试剂是______(填标号)。
A.KSCN溶液 B.溶液 C.KSCN溶液和双氧水
(3)“除铁”的离子方程式为______________________________________。
(4)已知①,
②Cu(OH)2(s)+4NH3H2O(aq)的平衡常数K1=。
试计算“除铜”过程中Cu2+(aq)+4NH3H2O(aq)的平衡常数K2=______________。
(5)完成“氧化”环节的化学反应方程式:________________________________。
21.(10分)CuCl是一种难溶于水的白色固体,可用作有机合成的催化剂,在潮湿的空气中易被氧化。实验室常用溶液与制备CuCl,装置如图所示(夹持装置省略)。
已知:是一种无色易挥发液体,熔点℃,沸点79℃。
回答下列问题:
(1)盛装氯化铜溶液的仪器名称是___________。
(2)制备CuCl的离子方程式为_____________________________________。
(3)配制溶液所需的蒸馏水需要煮沸,目的是_________________________。
(4)遇水剧烈水解生成两种酸性物质,其中一种能使品红溶液褪色,写出该水解反应的化学方程式:______________________________________________________。
(5)冰水的作用是_____________________________________________________________。
(6)产品CuCl纯度测定。称取样品0.25g置于预先放入50粒玻璃珠和溶液的锥形瓶中,不断摇动,待样品完全溶解,加水50mL,邻菲啰啉指示剂2滴,立即用标准溶液滴定至终点,消耗标准溶液25.51mL。同时做空白实验一次,消耗标准溶液0.53mL,如此再重复操作二次。0.25g样品三次消耗标准溶液平均体积为25.52mL,空白实验三次消耗标准溶液平均体积为0.52mL。
测定过程涉及如下反应:、,产品CuCl的纯度为___________,若做空白实验时,盛装标准液的滴定管未润洗,则测得CuCl的纯度___________(填“偏大”或“偏小”)。
22.(13分)到目前为止,约90%的工业产品是借助催化剂(工业上也称为触媒)生产出来的,催化剂解决了现代人类衣食住行中的许多问题.催化剂的研发具有重大的科学意义.
I.铁触媒催化合成氨的反应可表示为,该反应历程如下图所示,其中吸附在催化剂表面的物质用“ad”表示.
(1)下列有关叙述正确的有________(填代号).
A.分子中的键强度比键高
B.反应物分子被吸附到催化剂表面是一个放热过程
C.反应在历程中速率最慢
D.反应的
II.基元反应的过渡态理论认为,基元反应在从反应物到生成物的变化过程中要经历一个中间状态,称为过渡态,示意如下:
反应物 过渡态 生成物
(2)一溴甲烷与NaOH溶液反应的历程可以表示为:
( )
反应物 过渡态 生成物
III.降低CO2浓度,维持地球大气中CO2平衡,是当前的一项重要科研工程.我国力争于2030年前做到碳达峰,2060年前实现碳中和.有科学家提出以CO2与H2为原料,在催化剂作用下生成化工原料乙烯,反应原理如下:
=
(3)已知上述反应中,,(、为速率常数,只与温度有关),反应在时达到平衡,已知,则该反应的平衡常数________;下该反应达平衡时,若,则________(填“>”或“<”).
(4)己知(4)中反应可能伴随有以下副反应:
在恒压密闭容器中,CO2与H2的起始浓度一定的条件下,催化反应在相同时间内,测得不同温度下乙烯的产率如图中实线所示(图中虚线表示相同条件下乙烯的平衡产率随温度的变化):
①一定温度下,乙烯的产率达到X点时,v(正)________v(逆)(选填“<”、“>”或“=”).
②X点后乙烯的产率变小的原因可能是________、________(写出两条即可).
③工业生产中通常采用在一定条件下增大压强的方法来提高CO2的平衡转化率,从而提高乙烯的平衡产率,却意外发现的CO的平衡产率也显著提高了,请根据平衡移动原理解释其原因__________________________。
化学参考答案
1-5 B C A B D 6-10 B C C B B 11-15 C C B C C 16-18 B C D
19.(13分)
(1)3d104s1 (2分)
(2)正四面体形(2分)
(3)>(1分);N的2p轨道呈半充满状态,比较稳定(2分)
(4)③(2分)
(5)①(2分);②(2分)
20.(10分)(1)S、(2分)
(2)B(2分)
(3)(2分)
(4)2.0×1013(2分)
(5)Bi(OH)3+Cl2+3NaOH=NaBiO3+2NaCl+3H2O(2分)
21.(10分)(1)三颈烧瓶或三口烧瓶 (1分)(2) (2分)
(3)除去水中溶解的氧气,防止CuCl被氧化 (1分)
(4) (2分)
(5)冷却、收集 (1分)
(6)99.5% (2分) 偏小 (1分)
22.(13分)
(1)B、C (2分)
(2)(2分,Br与OH位置可以互换,填也给分)
(3)0.7(2分),<(2分)
(4)①>(1分).
②温度升高,催化剂的活性降低,反应速率降低,乙烯的产率变小;
温度升高,副反应的平衡正向移动,更有利于副反应的发生,乙烯的产率变小;
温度升高,使催化剂对副反应的选择性更大,乙烯的产率变小……
(2分,其它合理答案也给分).
③压强过大,使水蒸气液化,导致副反应的平衡正向移动(2分).
山西省+运城市康杰中学2023-2024学年高三上学期9月份摸底考试化学题: 这是一份山西省+运城市康杰中学2023-2024学年高三上学期9月份摸底考试化学题,共5页。
山西省运城市康杰中学2023-2024学年高二化学上学期开学考试试题(Word版附解析): 这是一份山西省运城市康杰中学2023-2024学年高二化学上学期开学考试试题(Word版附解析),共18页。试卷主要包含了 答题时使用0, 保持卡面清洁,不折叠,不破损,73%),主要以铝士矿形式存在,7%, 羟基和碳碳三键等内容,欢迎下载使用。
2022-2023学年山西省运城市康杰中学高二下学期3月月考化学试题含答案: 这是一份2022-2023学年山西省运城市康杰中学高二下学期3月月考化学试题含答案,共6页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。












