


- 专题04 化工生产——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册) 学案 1 次下载
- 专题05 饱和烃与不饱和烃——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册) 学案 3 次下载
- 专题06 乙醇、乙酸、糖、油、蛋白质——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册) 学案 3 次下载
- 期末模拟题(一)——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册) 学案 2 次下载
- 期末模拟题(二)——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册) 学案 2 次下载
期中模拟题(一)——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册)
展开期中模拟题一
第I卷(选择题)
相对原子质量:H-1 O-16 S-32 P-31 Cl-35.5 C-12 N-14 Na-23
一、选择题(每题只有一个正确答案,每题2分,共计40分)
1.NA是阿伏加德罗常数的值。下列说法正确的是
A.1molNa2O2固体中含离子总数为4NA
B.2.4g镁在足量的氧气中燃烧,转移的电子数为0.2NA
C.1mol重水中,中子数为8NA
D.标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA
2.氨广泛应用于化工、化肥、制药等领域,一种新型合成方法如下。下列说法正确的是
A.反应①属于自然固氮
B.反应③可利用电解MgCl2溶液的方法实现
C.该转化过程总反应为2N2+6H2O=4NH3+3O2
D.反应⑤在无水环境中进行时有白雾产生
3.元素的价类二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图像。铁元素的价类二维图如图,其中箭头表示部分物质间的转化关系,下列说法正确的是
A.FeO是一种黑色的氧化物,可由Fe、水蒸气高温反应制得
B.为实现Fe2+向Fe3+的转化,可向含Fe2+的溶液中通入新制氯水
C.工业上用CO还原Fe2O3炼铁,该反应属于置换反应
D.维生素C能将Fe3+转化为Fe2+,该过程体现维生素C的氧化性
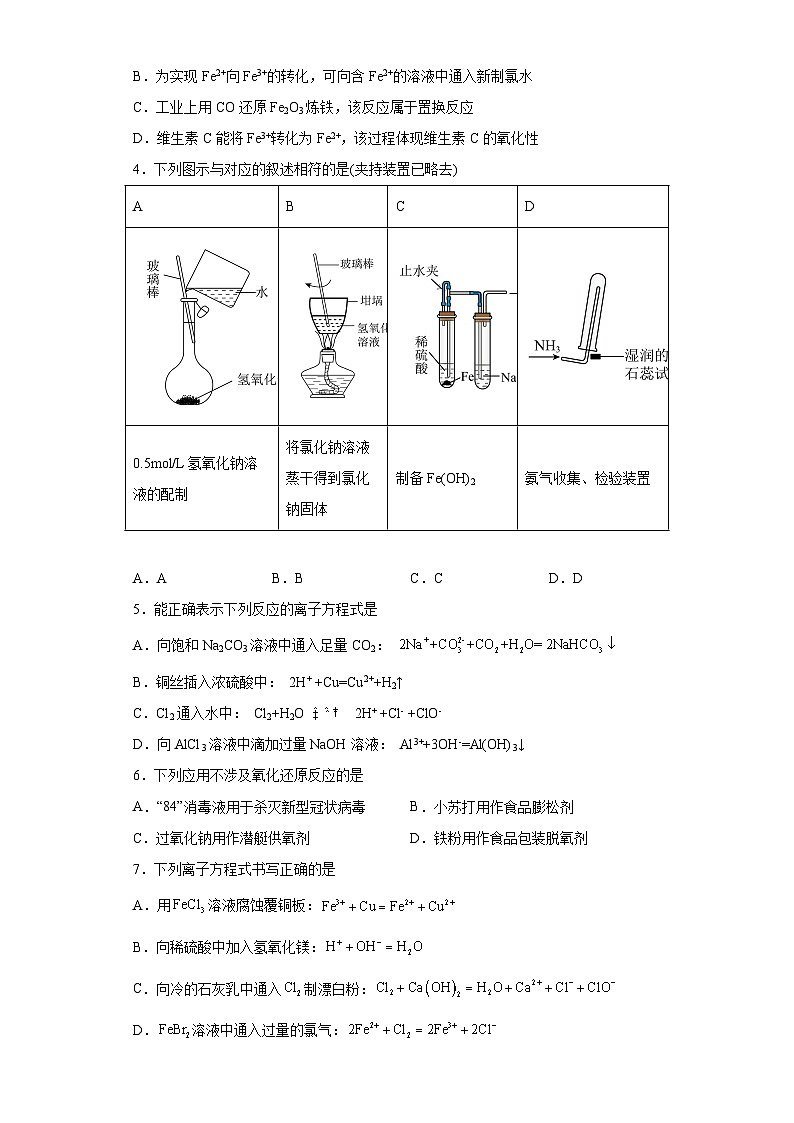
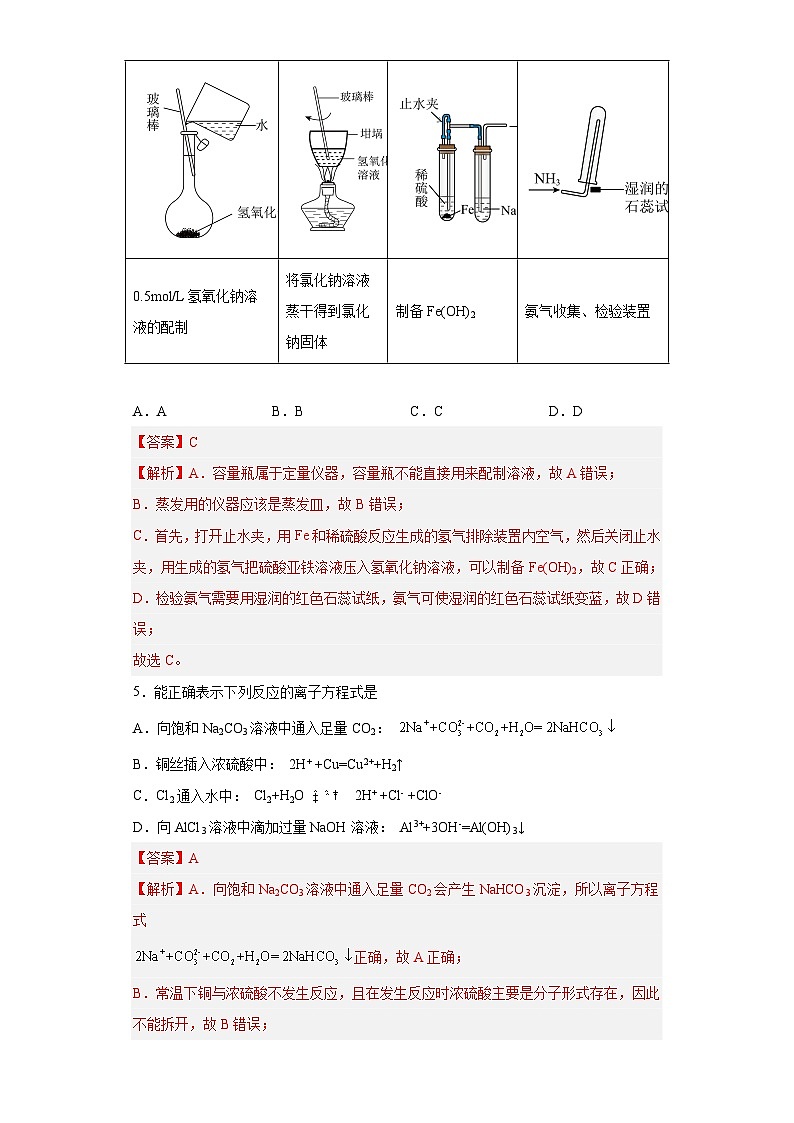
4.下列图示与对应的叙述相符的是(夹持装置已略去)
A | B | C | D |
0.5mol/L氢氧化钠溶液的配制 | 将氯化钠溶液蒸干得到氯化钠固体 | 制备Fe(OH)2 | 氨气收集、检验装置 |
A.A B.B C.C D.D
5.能正确表示下列反应的离子方程式是
A.向饱和Na2CO3溶液中通入足量CO2:
B.铜丝插入浓硫酸中: 2H+ +Cu=Cu2++H2↑
C.Cl2通入水中: Cl2+H2O 2H+ +Cl- +ClO-
D.向AlCl3溶液中滴加过量NaOH溶液: Al3++3OH-=Al(OH)3↓
6.下列应用不涉及氧化还原反应的是
A.“84”消毒液用于杀灭新型冠状病毒 B.小苏打用作食品膨松剂
C.过氧化钠用作潜艇供氧剂 D.铁粉用作食品包装脱氧剂
7.下列离子方程式书写正确的是
A.用溶液腐蚀覆铜板:
B.向稀硫酸中加入氢氧化镁:
C.向冷的石灰乳中通入制漂白粉:
D.溶液中通入过量的氯气:
8.在标准状况下将3.2g铜粉投入一定量浓中,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由和NO组成的混合气体1.344L(已转化为标况下的体积),则混合气体中NO的体积为
A.112mL B.224mL C.448mL D.1008mL
9.化学的世界,多姿多彩。下列物质颜色描述不正确的是
A.Fe2O3、黑色 B.、黄绿色
C.、淡黄色 D.Fe(OH)3、红褐色
10.某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下列分析或结果错误的是
A.OA段产生的是NO,AB段发生的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
B.第二份溶液从反应开始至结束,所得气体总体积在标况下为4.48L
C.原混合酸中的物质的量为0.1mol
D.C点浓度为2.5mol·L-1
11.下列指定反应的离子方程式正确的是
A.稀硫酸滴在铁片上:
B.少量金属铝放入氢氧化钠中:
C.醋酸溶解水垢中的碳酸钙:
D.金属钠放入冷水中:
12.下列化合物不能用相应元素的单质直接化合而成的是
①②③④⑤⑥⑦
A.②⑤⑧ B.①④⑥ C.③④⑦ D.④⑥⑦
13.常温下,下列各组离子能大量共存的是
A.、、、 B.、、、
C.、、、 D.、、、
14.下列实验操作可以达到实验目的的是
选项 | 实验操作 | 实验目的或结论 |
A | 将1mL溶液与1mLKI溶液混合,充分反应后分为两份,一份加2滴KSCN,另一份加2滴淀粉试液,观察现象 | 证明KI与能反应且具有可逆性 |
B | 向两支盛有2mL5%溶液的试管中分别加入的溶液和的溶液,比较产生气泡速率 | 催化分解效果优于 |
C | 向饱和溶液中通入某无色无味气体X,观察是否有沉淀生成 | 确定X是否为 |
D | 用pH计分别测定和的溶液的pH,记录并比较pH变化 | 随着溶液中减小,的电离程度增大 |
A.A B.B C.C D.D
15.下列有关化学反应速率的说法正确的是
A.100mL的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
B.用锌片和稀硫酸反应制取氢气时,用粗锌比纯锌反应生成氢气的速率会加快
C.反应在一容积可变的密闭容器中进行,增加的量,其反应速率增大
D.汽车尾气中的和可以反应生成和,减小压强反应速率加快
16.可逆反应,在四种不同情况下的反应速率如下,其中反应进行得最快的是
A. B.
C. D.
17.在反应:C+CO22CO中,可使反应速率增大的措施是
①压缩体积以增大压强;②升高温度;③体积不变,通入CO2;④增加碳的量;⑤移出CO
A.①②③④⑤ B.①②③⑤ C.①②③ D.①②③④
18.短周期主族元素X、Y、Z、W在周期表中的位置如图所示,其中X、W最低负化合价之和为-4,下列说法错误的是
| Y | Z |
X |
| W |
A.原子半径: X>Y
B.单质的熔点: X> W
C.X与W只能形成一种化合物
D.简单氢化物的稳定性: Z> W
19.已知短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子的最外层电子数是内层电子数的3倍,Y与X能形成两种离子化合物Q、M,Z所在周期序数与族序数相同,W与X同主族,下列说法中正确的是
A.Q、M均只含有离子键 B.氢化物的热稳定性: X>W
C.Y、Z两元素只能形成阳离子 D.简单离子半径大小: W>X>Z>Y
20.在恒温恒容下,反应,达到平衡状态的标志是
A.c(A)的浓度不再变化
B.A、B、C、D的反应速率之比为2:2:3:1
C.单位时间内生成n molB,同时消耗1.5n molC
D.容器内各气体浓度相等
第II卷(非选择题)
二、填空题(共四题,每题15分)
21.回答下列问题:
(1)如图是某同学设计的一个简易的原电池装置,请回答下列问题。
①若a电极材料为碳、b溶液为溶液,则正极的电极反应式为_______,当有1.6 g负极材料溶解时,转移的电子为_______mol。
②若a电极材料为铁、b溶液为浓硝酸,电流表的指针也会偏转,则电子的流向为_______→_______(填电极材料,下同);溶液中的向_______极移动。
(2)有人以化学反应:为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它靠人体内血液中溶有一定浓度的、进行工作。则原电池的负极材料是_______,正极反应式为_______。
22.已知反应:。某温度时,在容积恒定为2.0L的密闭容器中充入2.0mol 和2.0mol ,一段时间后反应达平衡状态,实验数据如表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~50s内的平均反应速率_______。
(2)250s时,容器中的物质的量是_______,的转化率是_______。
(3)为加快该反应速率,可以采取的措施是_______。
a.降低温度 b.使用催化剂 c.恒容时充入He气 d.恒压时充入He气
(4)已知:断开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要吸收能量为436 kJ、391 kJ、946 kJ,则生成1mol 过程中_______(填“吸收”或“放出”)的能量为_______kJ。
23.I.氮氧化物和硫氧化物是造成大气污染的主要原因之一,消除氮氧化物有多种方法。
(1)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:
①氮氧化物会带来什么污染________(回答一点),由图1可知SCR技术中的氧化剂为:_______。写出NH2与NO2反应的化学方程式___________。
②用Fe做催化剂时,在氨气足量的情况下,不同对应的脱氮率如图3所示,脱氮效果最佳的 =_______。
(2)利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如图。
①上述工艺中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是___________;滤渣可循环使用,滤渣的主要成分是___________(填化学式)。
②生产中溶液需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,其反应的离子方程式为___________。
II.氮氧化物(NO、NO2)、SO2是大气污染物。回答下列问题:
(3)如图包含气体发生装置和收集装置(部分装置的夹持仪器已省略),实验室以Cu与浓HNO3反应制备并收集NO2,应选择的装置是___________(填字母)。
(4)SCR脱硝技术已成为使用广泛和成熟的烟气净化技术,脱硝效率高达90%以上。反应机理如图所示,写出该反应发生的化学方程式:___________。
(5)目前,NaClO溶液广泛地应用于脱硫脱硝。某课外小组同学设计了如图喷淋吸收塔装置(如图)。该装置脱硫脱硝后,溶液的酸性___________(增强、减弱、不变)。
三、元素或物质推断题
24.下表列出了①~⑩十种元素在周期表中的位置。
族 周期 | IA |
|
|
|
|
|
| 0 |
二 | ① | IIA | IIIA | IVA | VA | VIA | VIIA |
|
三 |
|
|
| ② | ③ | ④ |
| ⑤ |
四 | ⑥ |
| ⑦ | ⑩ |
| ⑧ | ⑨ |
|
回答下列问题:
(1)①~⑩十种元素中,化学性质最不活泼的是_______(填元素符号)。
(2)元素②和③中原子半径较大的是_______(填元素符号)。
(3)元素③和④中气态氢化物稳定性较强的是_______(填化学式)。
(4)元素⑧和⑨的最高价氧化物对应的水化物中,酸性强的是_______(填化学式)。
(5)元素⑦的单质与⑥的最高价氧化物对应的水化物反应的离子方程式为_______。
(6)元素②的单质和⑩的最高价氧化物反应的化学方程式为_______。
(7)元素④和⑥形成的化合物中既含有离子键又含有非极性键,该化合物的电子式为_______,元素①和③组成的10电子化合物,该分子构型为_______。
期末模拟题(二)——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册): 这是一份期末模拟题(二)——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册),文件包含期末模拟题二2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷沪科版2020必修第二册解析版docx、期末模拟题二2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷沪科版2020必修第二册原卷版docx等2份学案配套教学资源,其中学案共27页, 欢迎下载使用。
期末模拟题(一)——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册): 这是一份期末模拟题(一)——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册),文件包含期末模拟题一2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷沪科版2020必修第二册解析版docx、期末模拟题一2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷沪科版2020必修第二册原卷版docx等2份学案配套教学资源,其中学案共24页, 欢迎下载使用。
专题05 饱和烃与不饱和烃——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册): 这是一份专题05 饱和烃与不饱和烃——2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷(沪科版2020必修第二册),文件包含专题05饱和烃与不饱和烃2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷沪科版2020解析版docx、专题05饱和烃与不饱和烃2022-2023学年高一化学下学期期末知识点精讲+训练学案+期末模拟卷沪科版2020原卷版docx等2份学案配套教学资源,其中学案共39页, 欢迎下载使用。