
2023届湖南省衡阳市第八中学高三下学期第七次月考化学试卷Word版含答案
展开2023届高三第七次月考化学试题
可能用到的柏对银子质亚:H~1 C~12 N~14 O~16 Cl~35.5 Ca~40 Sc~45 Fe~56 Sb~122
一、选择题:本题共14小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
1.药物本维莫德可用于局部治疗成人稳定性寻常型银屑病,其结构简式如图所示。下列关于该化合物说法正确的是
A.分子中共平面的碳原子最多有16个
B.该有机物能发生消去反应
C.1mol该有机物最多能与6mol 发生反应
D.苯环上的一氯取代物有5种
2.短周期元素X、Y、Z、M、N、W原子序数依次递增,六种元素形成的一种化合物结构如图所示,其中元素Z最外层电子数为内层电子数的3倍。下列说法正确的是
A.最高价氧化物对应水化物的酸性W>Y>N
B.元素Z与其他五种元素均可形成2种及以上化合物
C.简单离子半径Z>M>W
D.元素X与其他五种元素均可形成共价化合物
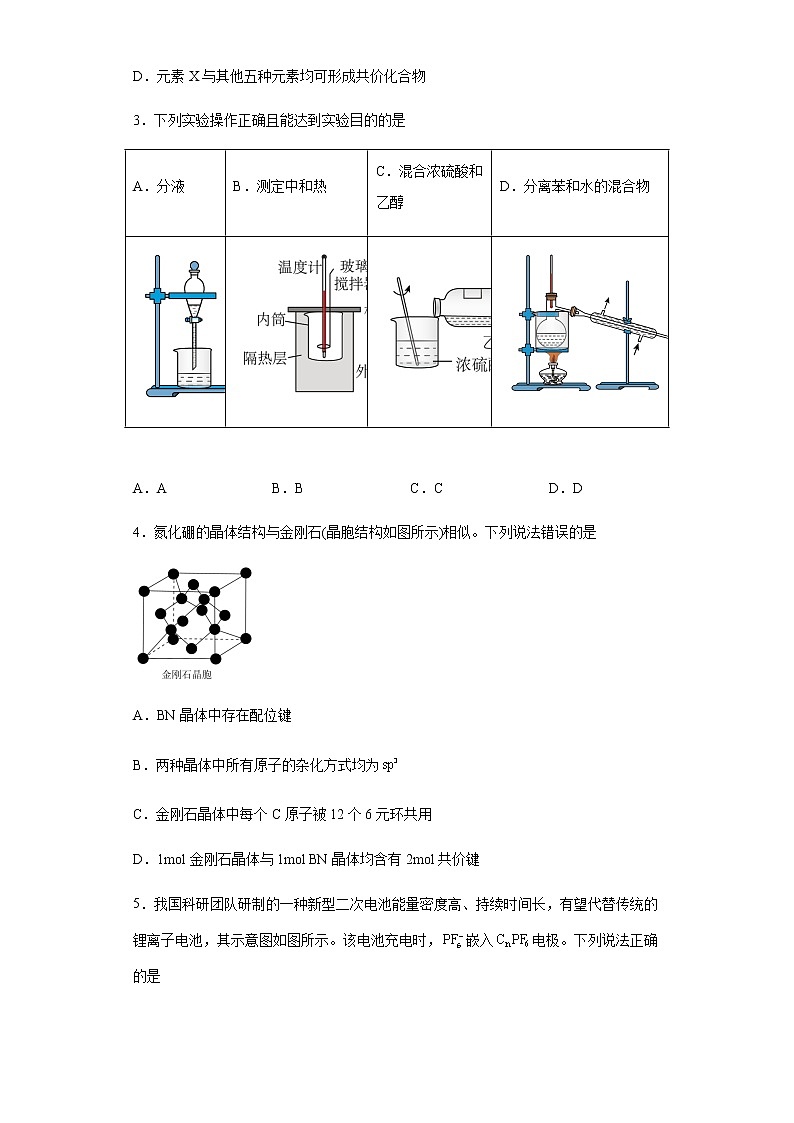
3.下列实验操作正确且能达到实验目的的是
A.分液 | B.测定中和热 | C.混合浓硫酸和乙醇 | D.分离苯和水的混合物 |
A.A B.B C.C D.D
4.氮化硼的晶体结构与金刚石(晶胞结构如图所示)相似。下列说法错误的是
A.BN晶体中存在配位键
B.两种晶体中所有原子的杂化方式均为
C.金刚石晶体中每个C原子被12个6元环共用
D.1mol金刚石晶体与1mol BN晶体均含有2mol共价键
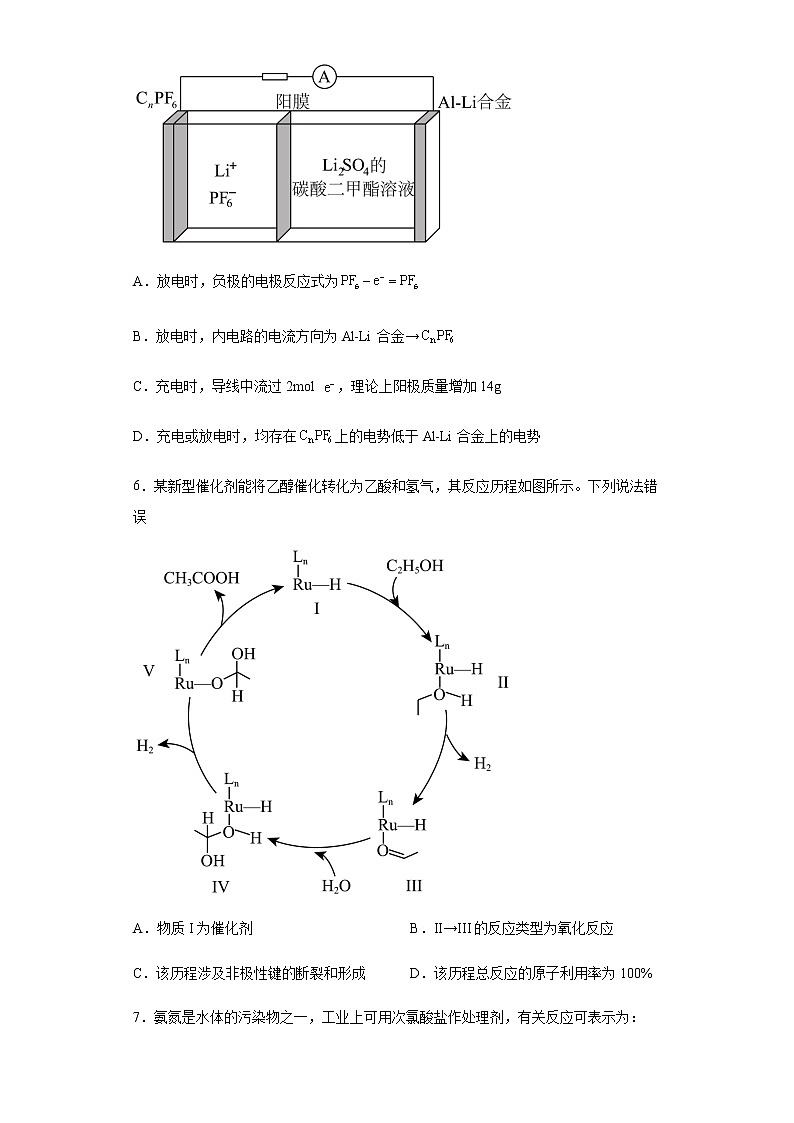
5.我国科研团队研制的一种新型二次电池能量密度高、持续时间长,有望代替传统的锂离子电池,其示意图如图所示。该电池充电时,嵌入电极。下列说法正确的是
A.放电时,负极的电极反应式为
B.放电时,内电路的电流方向为Al-Li合金→
C.充电时,导线中流过2mol ,理论上阳极质量增加14g
D.充电或放电时,均存在上的电势低于Al-Li合金上的电势
6.某新型催化剂能将乙醇催化转化为乙酸和氢气,其反应历程如图所示。下列说法错误
A.物质I为催化剂 B.II→III的反应类型为氧化反应
C.该历程涉及非极性键的断裂和形成 D.该历程总反应的原子利用率为100%
7.氨氮是水体的污染物之一,工业上可用次氯酸盐作处理剂,有关反应可表示为:
①
②
实验室将的氨水分别和不同量的混合,测得溶液中氨去除率、总氮(氨氮和硝氮的总和)残余率与投入量(用n表示)的关系如图所示。下列说法错误的是
A.的数值为 B.时,
C.时, D.时,n越大,生成的量越少
8.化学与科技、社会、生活有着密切的联系。下列有关说法正确的是
A.亚硝酸钠是一种常用食品添加剂,可用于防腐、上色
B.铁粉与氧化铝发生的铝热反应可用于焊接铁轨
C.纳米级二氧化硅可用于制计算机芯片
D.通过石油的分馏可得到乙烯等化工原料
9.设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A.含有1mol水分子的冰中,氢键的数目为4NA
B.0.25molXeF6中氙的价层电子对数为1.5NA
C.46g CH3OCH3中sp3杂化的原子数为2NA
D.1molNH4BF4中配位键的数目为2NA
10.下列有关反应的离子方程式正确的是
A.0.1mol·L-1CuSO4溶液中加入过量氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2NH
B.向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO完全沉淀:NH+Al3++2SO+2Ba2++4OH-=NH3·H2O+Al(OH)3↓+2BaSO4↓
C.溶液中通入H2S:
D.向Ca(ClO)2溶液中通入过量CO2制取次氯酸:Ca2++ClO- +H2O+CO2=2HClO+CaCO3↓
11.以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料生产Al2O3并获得Fe3O4的工艺流程如下,下列叙述中不正确的是
A.隔绝空气焙烧时反应炉中FeS2与Fe2O3的最佳质量比为3:64
B.加入CaO的目的是防止焙烧产生的SO2排放到大气中污染环境
C.加入NaOH溶液的目的是通过溶解Al2O3实现铝、铁元素的分离
D.该工艺流程能耗低,原料利用充分,符合绿色化学的思想
12.在固体M的催化下,A转化为D和E分两步进行:①;②,其反应过程能量变化如图所示,下列说法错误的是
A.该反应的速率是由步骤I决定的
B.总反应的焓变
C.反应过程中,C物质很难大量积累
D.催化剂的作用是降低反应的活化能,但活化分子百分数不变
13.根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | A、B两支试管中分别加入10 mL 5%的H2O2溶液,在A试管中加入1 mL FeCl3溶液,在B试管中加入1 mL蒸馏水 | A试管中产生气泡更快 | FeCl3是H2O2分解的催化剂 |
B | 室温下,向10 mL 0.2 mol/L NaOH溶液中滴入2滴0.1 mol/L MgCl2溶液,产生白色沉淀,再滴加2滴0.1 mol/L FeCl3溶液 | 有红褐色沉淀生成 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
C | 将5 mL 0.1mol/L FeCl3溶液与2 mL 0.1mol/L KI溶液混合于试管中充分反应后,滴加几滴KSCN溶液,振荡 | 溶液变为血红色 | Fe3+与I-的反应有一定的限度 |
D | 室温下,向2 mL 0.1 mol·L 溶液中加入2滴0.1 mol·L NaCl溶液,再滴加4滴0.1 mol·L KI溶液 | 先出现白色沉淀,后出现黄色沉淀 | 证明相同温度下: |
A.A B.B C.C D.D
14.高炉炼铁中的一个反应为 ,在1100℃下,若CO起始浓度为1.2mol/L,10min后达到平衡时的体积分数为,下列说法错误的是
A.1100℃下,此反应的平衡常数
B.达到平衡过程中,反应的平均速率为
C.达到平衡后,若增大,则达到新平衡时,增大
D.测得某时刻,则此时
二、非选择题(本题共4小题,共58分)。
15.亚硝酸钙【】是白色粉末、易潮解、易溶于水,在钢筋混凝土工程中,常用作水泥硬化促进剂和防冻阻锈剂。实验制备亚硝酸钙装置如图所示(夹持装置已略去)。
回答下列问题:
(1)加入稀硝酸之前需通入一段时间,其目的是_______。
(2)装置A中反应的化学方程式为_______。
(3)装置B中盛装试剂的名称是_______。
(4)装置E的作用是_______。
(5)利用上述装置制备亚硝酸钙,会导致产率降低,改进的方法是_______。
(6)测定所得亚硝酸钙产品中硝酸钙的含量。
实验原理:
实验步骤:
I.称量产品溶于水,加入足量的硫酸钠固体,充分搅拌后过滤;
II.将滤液配制成溶液,取溶液于锥形瓶中,加入足量饱和溶液,煮沸,冷却;
III.再向锥形瓶中加入溶液和适量硫酸;
IV.加入4滴指示剂,用标准液滴定至终点,消耗标准液。
①测定过程中未使用到的仪器是_______(填标号)。
A.漏斗 B.胶头滴管 C.直形冷凝管 D.碱式滴定管
②所得产品中硝酸钙的质量分数为_______。
16高纯碘化钠晶体是核医学、大型安防设备、暗物质探测等领域的核心材料。某研究小组在实验室制备高纯NaI的简化流程如图:
已知:①I2(s)+I-(aq)I(aq)。
②水合肼(N2H4·H2O)具有强还原性,可将各种价态的碘还原为I-,氧化产物为N2。
③NaI易被氧化,易溶于水、酒精,在酒精中的溶解度随温度的升高增加不大。
回答下列问题:
(1)①步骤Ⅰ,I2与Na2CO3溶液同时发生两个反应,生成物除NaI外,还分别生成NaIO和NaIO3,一个反应为:I2+Na2CO3=NaI+NaIO+CO2↑,另一个反应为:___________。
②I2与Na2CO3溶液的反应很慢,加入NaI固体能使开始反应时的速率明显加快,原因可能是___________。
(2)步骤Ⅱ,水合肼与IO反应的离子方程式为___________。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH时依次加入的试剂为___________、___________、___________。
A.NaOH B.HI C.NH3•H2O D.高纯水
(4)步骤Ⅳ,蒸发操作为减压蒸发。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有___________。
A.直形冷凝管 B.球形冷凝管
C.烧杯 D.抽气泵
②采用“减压蒸发”的优点有:减小压强,降低沸点,利于水的蒸发;___________。
(5)将制备的NaI•2H2O粗品以无水乙醇为溶剂进行重结晶。请选择合理的操作并排序:加热乙醇→___________→___________→___________→___________→纯品(选填序号)。
①高纯水洗涤 ②减压蒸发结晶 ③真空干燥 ④NaI•2H2O粗品溶解 ⑤趁热过滤 ⑥降温结晶
17.低碳经济是以低能耗、低污染、低排放为基础的经济模式。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)现用300mL 0.5mol•L﹣1的NaOH溶液吸收2.24L(标准状况下)CO2,完全吸收反应后,所得溶液中离子浓度由大到小的顺序为:_______。
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,紫外线照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图1所示。在0~15h内,对反应催化效果最好的催化剂是_______。(填序号)
(3)一定温度下,在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)⇌H2O(g)+CO(g)△H=+41.2kJ•mol﹣1,已知c(CO)随反应时间t的变化曲线a如图2所示,在t1时刻改变一个条件,曲线a变为b,则改变的条件是_______。
(4)如图3是利用甲烷燃料电池给C电极上镀金属铜,则乙池中选择的电解质溶液为_______,A电极的电极反应式为_______,若C电极增重0.96g,则B电极上消耗O2的物质的质量为_______。
18.有机物H是一种用于治疗帕金森病精神症状的药物,其合成路线如下图所示:
回答下列问题:
(1)A的化学名称为_______。 (2)B的结构简式为_______。
(3)C→D反应的化学方程式为_______。 (4)G→H的反应类型为_______。
(5)H中含氧官能团的名称为_______。
(6)在C的同分异构体中,同时满足下列条件的有_______种,其中核磁共振氢谱有五组峰,且峰面积之比为的结构简式为_______。
a.能使溶液发生显色反应b.能发生银镜反应,又能发生水解反应
答案:
1.A 2.B 3.B 4.D 5.B 6.C 7.C
8.A 9.D 10.B 11.D 12.D 13.A 14.C
15.(1)排除装置中的空气,防止其中的O2将生成的NO氧化为NO2
(2)
(3)蒸馏水
(4)尾气吸收,防止空气污染
(5)在装置D、E之间加装盛有浓硫酸的洗气瓶
(6) ACD %
16. 3I2+3Na2CO3=5NaI+NaIO3+3CO2↑或3I2+3CO=5I-+IO+3CO2↑ I-(aq)与I2(s)反应形成I(aq),增加固体I2的溶解性,增大反应速率或NaI对该反应具有催化作用 3N2H4·H2O+2IO= 3N2↑+2I-+9H2O A B A A D 减压环境与外界空气隔绝,避免I-被氧化; ④ ② ⑤ ③
17.(1)c(Na+)>c(HCO)>c(CO)>c(OH﹣)>c(H+)
(2)Ⅱ
(3)加入催化剂
(4) CuSO4溶液 CH4+10OH﹣﹣8e﹣=CO+7H2O 0.24g
18.(1)对羟基苯甲醛
(2)
(3)+CH3OH+H2O
(4)加成反应
(5)醚键、酰胺基
(6) 13
湖南省衡阳市第一中学2022-2023学年高三化学第七次月考试卷(Word版附解析): 这是一份湖南省衡阳市第一中学2022-2023学年高三化学第七次月考试卷(Word版附解析),共22页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
湖南省株洲市重点中学2023届高三第七次月考化学试卷(解析版): 这是一份湖南省株洲市重点中学2023届高三第七次月考化学试卷(解析版),文件包含湖南省株洲市重点中学2023届高三第七次月考化学试题解析版docx、湖南省株洲市重点中学2023届高三第七次月考化学试题原卷版docx等2份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。
湖南省宁乡市重点高级中学2023届高三第七次月考化学试卷(解析版): 这是一份湖南省宁乡市重点高级中学2023届高三第七次月考化学试卷(解析版),文件包含湖南省宁乡市重点高级中学2023届高三第七次月考化学试题解析版docx、湖南省宁乡市重点高级中学2023届高三第七次月考化学试题原卷版docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。












