
2021-2022学年黑龙江省勃利县高级中学高一上学期期末考试化学试卷含答案
展开勃利县高级中学2021-2022学年度第一学期期末考试
高一化学
(时间:90分钟 满分:100分)
相对原子质量:H-1 C-12 O-16 N-14 Na-23 S-32 Fe-56 Cl-35.5 Ba-137
一、单选题(每题2分)
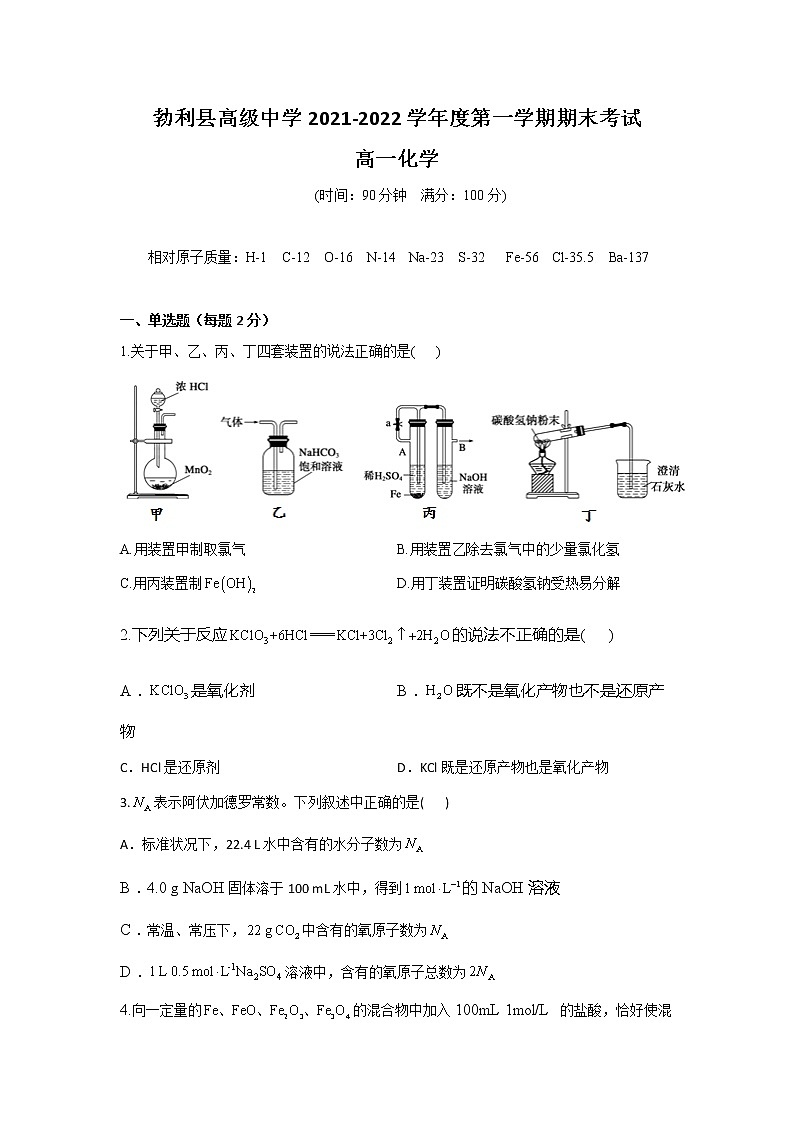
1.关于甲、乙、丙、丁四套装置的说法正确的是( )
A.用装置甲制取氯气 B.用装置乙除去氯气中的少量氯化氢
C.用丙装置制 D.用丁装置证明碳酸氢钠受热易分解
2.下列关于反应的说法不正确的是( )
A.是氧化剂 B.既不是氧化产物也不是还原产物
C.HCl是还原剂 D.KCl既是还原产物也是氧化产物
3.表示阿伏加德罗常数。下列叙述中正确的是( )
A.标准状况下,22.4 L水中含有的水分子数为
B.4.0 g NaOH固体溶于100 mL水中,得到的NaOH溶液
C.常温、常压下,中含有的氧原子数为
D.溶液中,含有的氧原子总数为
4.向一定量的的混合物中加入100mL 1mol/L 的盐酸,恰好使混合物完全反应,放出 11.2mL(标准状况)气体,所得溶液加入 KSCN 溶液不变红色。用足量的CO 在高温下还原相同质量的此混合物,所得铁的质量为( )
A.2.8g B.11.2g C.5.6g D.无法计算
5.下列实验现象的解释正确的是( )
实验现象
解释
A
KI淀粉溶液中通入Cl2,溶液变蓝
淀粉能与Cl2发生反应
B
胶体的微粒可以透过滤纸,不能透过半透膜
胶体的微粒直径介于1―100nm之间
C
用洁净铂丝蘸取溶液进行焰色反应火焰呈黄色
溶液中有Na+、无K+
D
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成
一定是由于该溶液中含有
A.A B.B C.C D.D
6.下列有关物质分类的叙述正确的是( )
A.四种物质都属于化合物
B.溶液、浊液、胶体都属于混合物
C.硫酸、纯碱、硝酸钠和生石灰分别属于酸、碱、盐和碱性氧化物
D.等非金属氧化物均属于酸性氧化物
7.诗词是中华民族的文化瑰宝,下列分析中不正确的是 ( )
A.“白云深处有人家”:“白云”是一种胶体
B.“蜡炬成灰泪始干”:该过程中只发生了物理变化
C.“爆竹声中一岁除”:燃放爆竹过程中涉及氧化还原反应
D.“烈火焚烧若等闲”:描述了碳酸钙的分解,碳酸钙是一种电解质
8.下列指定反应的离子方程式正确的是( )
A.铜片插入硝酸银溶液:
B.溶液中滴加稀盐酸: C.与水反应:
D.溶液中滴加溶液:
9.短周期主族元素W、M、X、Y、Z的原子序数依次增大。W的族序数是周期数的3倍,X原子的最外层只有一个电子,Y是地壳中含量最多的金属元素,Z在同周期中原子半径最小。下列说法错误的是( )
A.X2W2和X2W中阴、阳离子个数之比均为1:2
B.M、Z两种元素的气态氢化物的稳定性:M
D.可用M的单质与W的氢化物反应来证明非金属性:M>W
10.2019年12月以来,我国部分地区突发的新型冠状病毒肺炎威胁着人们的身体健康。以下是人们在面对“新型冠状病毒肺炎”时的一些认识,你认为符合科学道理的是( )
A.家庭消毒时,消毒液越浓越好
B.吸烟、喝酒可以预防“新型冠状病毒”
C.应经常保持室内清洁卫生和通风
D.具有还原性,可用于自来水的杀菌消毒
11.某溶液加入铝片可以产生,则在该溶液中一定能大量存在的离子组是( )
A. B.
C. D.
12.下列描述对应的离子方程式书写正确的是( )
A.用食醋清洗水垢(水垢成分之一有氢氧化镁):
B.饱和碳酸钠溶液中通入足量的二氧化碳:
C.氢氧化铝可用于治疗胃酸过多:
D.向溶液中加入溶液至刚好沉淀:
13.化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是( )
A.焰火中呈现的绚丽色彩,是金属元素焰色反应形成的
B.小苏打既是制作糕点的膨松剂,还是治疗胃酸过多的一种药剂
C.氯气、明矾是水处理过程中常用的两种化学试剂,两者的作用原理相同
D.装运乙醇的包装箱上应贴上易燃液体的危险品标志图标
14.某化学兴趣小组同学对有关物质的分类进行讨论辨析,下列说法正确的是( )
A.BaSO4、CH3COONH4都属于强电解质 B.SiO2、NO2都属于酸性氧化物
C.NaCl溶液、牛奶都属于溶液 D.CuSO4·5H2O、水玻璃都属于纯净物
15.下列有关物质的描述,不正确的是( )
A.纯碱溶液可去油污
B.干燥的Cl2可以使干燥的有色布条褪色
C.NaHCO3可作胃酸的中和剂
D.Al(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的
16.用NA表示阿伏德罗常数,下列叙述正确的是( )
A.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02NA
B.标准状况下,22.4L水含有的原子数为3NA
C.通常状况下,0.5NA个CO2分子占有的体积为11.2L
D.物质的量浓度为0.5mol·L-1的MgCl2溶液中,含有Cl-个数为NA
17.配制100mL 1.0mol·L-1的NaOH溶液,下列情况对结果没有影响的是( )
A.容量瓶使用前经蒸馏水清洗后没有干燥
B.未冷却至室温就将溶液转移至容量瓶中
C.仰视确定凹液面与刻度线相切
D.用敞口容器称量NaOH且时间过长
18.下列各组物质混合后,既有气体生成,最终又有沉淀生成的是( )
① 金属钠投入到溶液中
② 过量溶液和明矾溶液混合
③ 过量生石灰投入到少量饱和溶液中
④投入溶液中
A.只有① B.只有③ C.只有②③ D.只有①③④
19.关于反应= ,下列说法正确的是( )
A.当有2 被氧化时,2氧原子被还原
B. 是还原产物
C.若消耗2.24L ,则转移0.2电子
D.氧化剂与还原产物的物质的量之比为
20.下列叙述正确的是( )
A.固体氯化钠不导电,所以氯化钠是非电解质
B.铜丝能导电,所以铜是电解质
C.氯化氢水溶液能导电,所以氯化氢是电解质
D.溶于水能导电,所以是电解质
二、多选题(每题有一个或两个正确选项,每题两分)
21.下列说法正确的是( )
A.加热含4 mol HCl的浓盐酸与足量的混合物,使其充分反应,转移的电子数为
B.1L0.1 mol/L溶液中的质量为7.1g
C.常温常压下,32g和混合气体中氧原子的物质的量为2mol
D.用含有1 mol的溶液制得胶体,胶体中含有个胶粒
22.短周期主族元素X、Y、Z、W的原子序数和族序数均依次增大,其中只有Y、Z处于同一周期,Z是空气中含量最高的元素。下列说法正确的是( )
A.X、Z两种元素形成的化合物中可能既含极性键,又含非极性键
B.原子半径:
C.W的氧化物对应的水化物一定是强酸
D.W的简单气态氢化物与W的最高价含氧酸在任何条件下都不发生反应
23.向混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
A.溶液中一定含有
B.溶液中一定含有
C.剩余固体中一定含有Cu
D.加入KSCN溶液可能变红
24.已知常温下,在溶液中发生如下反应:
①;
②;
③。
由此推断下列说法错误的是( )
A. 反应可以进行
B.Z元素在反应①中被还原,在反应③中被氧化
C.可以置换出溶液中的X
D. 氧化性由强到弱的顺序是
25.某黄色溶液中可能含有等离子(不考虑水的电离和离子的水解)。某同学为了确定其组分,设计并完成了如下实验:
下列说法正确的是( )
A.一定为0.2 mol•L﹣1
B.一定存在
C.一定存在,一定不存在
D.可能存在,一定不存在
三、填空题
26.(每空1分,共9分)完成下列问题:
(1)个氯气分子的物质的量是_____,中含有的电子数为_____(用表示)。
(2)同温同压下,同体积的甲烷()和二氧化碳物质的量之比为_____,密度之比为_____。
(3)要使与含相同数目的氢原子,则和的质量之比为_____。
(4)含有,则的摩尔质量为_____,X的相对原子质量为_____。
(5)在标准状况下,CO和的混合气体共6.72L,质量为12g,则两种气体的物质的量之比为_________,混合气体的平均摩尔质量为_________。
27.(每空1分,共8分)为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:
(1)⑧所对应的元素名称为__________________,其在周期表中的位置__________________。
(2)在①~⑨元素中,原子半径最大的是__________________(填元素符号),其某种氧化物可用于呼吸面具中氧气来源,请写出该氧化物的电子式__________________。
(3)⑤⑥⑦三种元素所形成的最高价氧化物对应的水化物碱性最强的是__________________(填化学式)。
(4)比较④与⑨的气态氢化物的稳定性__________________>__________________(填化学式)。
(5)由下列元素形成的化合物中含有离子键的是__________________。
A.①和③ B.②和③ C.①和④ D.⑥和⑨
28.(共9分)回答下面各题。
Ⅰ现有中学化学中常见的八种物质:
①固体氢氧化钡 ②石墨碳棒 ③纯醋酸 ④液态氯化氢 ⑤硫酸氢钾固体 ⑥ 熔融氯化钠 ⑦蔗糖 ⑧碳酸钠粉末
请用序号填空:
(1)上述状态下可导电的是________,属于电解质的是_____________。
Ⅱ、现有甲、乙、丙三名同学分别进行胶体的制备实验。
①、甲同学向氯化铁溶液中加入少量的NaOH溶液;
②、乙同学直接加热饱和溶液;
③、丙同学向25 ml沸水中逐滴加入5~6滴饱和溶液,继续煮沸至溶液呈红褐色,停止加热。
(1)其中操作正确的同学是______;他的操作中涉及到的化学反应方程式为_______________________________________________________。
(2)证明有胶体生成的现象是________________________。
(3)丁同学将所制得的胶体进行下列实验:
将胶体装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明________________________________。
29.(每空2分,共16分)健康人体内含铁元素大约 2~3g,人体内铁元素以亚铁离子和三价铁离子的形式存在,Fe2+易被吸收,所以给贫血者补充铁元素时,应补充含 Fe2+的亚铁盐。“速力菲”(主要成分:琥珀酸亚铁)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
(1)试剂1的名称是__________。
(2)加入新制氯水,溶液中发生反应的离子方程式是_____________________________。
(3)加入试剂2 时溶液为淡红色说明 “速力菲”中的 Fe2+已部分氧化,一般在服用“速力菲”时,同时服用维生素C,说明维生素C具有___________性。
(4)溶液中白色沉淀更易被氧化,请写出反应的化学方程式________________
(5)实验室用下图装置制备并收集干燥纯净的。
①装置A中反应的化学方程式是___________
②装置B的作用是___________
③向干燥氯气中分别加入一块干燥的有色纸条和一块湿润的有色纸条,观察到的现象为___________
④有毒,未反应的可用NaOH溶液吸收,请写出反应的离子方程式______________
四、实验题
30.(每空2分,共8分)实验室需要配制的硫酸溶液500mL。请回答下列问题:
(1)根据计算得,需量取质量分数为98%、密度为的浓硫酸的体积为_______mL(保留三位有效数字)。
(2)在如图所示仪器中,配制上述溶液肯定不需要的有_______(填序号)。
(3)实验操作步骤包括
A.把溶液小心地转移至容量瓶中。
B.量取所需浓硫酸,沿杯壁倒入盛有适量水的烧杯中,同时用玻璃棒搅拌并冷却至室温。
C.继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切。
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液都小心注入容量瓶,并轻轻振荡。
E.将容量瓶塞塞紧,充分摇匀。
操作步骤的正确顺序为______(填序号)。
(4)下列情况中,会使所配溶液浓度偏高的是______(填序号)。
A.量取浓硫酸时,某同学仰视液面读数
B.没有进行上述的操作步骤D
C.定容加蒸馏水时,不慎超过了刻度线
D.容量瓶使用前内壁沾有水珠
E.用少量蒸馏水洗涤量取浓硫酸后的量筒,并将洗涤液注入烧杯
高一化学期末答案
1-10 CDCAB BBCBC 11-20 ABCAB AADDC 21.BC 22.AB 23.BD 24.BC 25.BD
26.答案:(1)0.5mol;
(2)1:1;4:11
(3)17:12
(4);16
(5)1:3;
27.答案:(1)硫;第三周期第ⅥA族
(2)Na;
(3)NaOH
(4)HF;HCl
(5)D
28.答案:Ⅰ(1)②⑥ ①③④⑤⑥⑧
Ⅱ (1)丙
(2)用激光笔照射,若有一条光亮的通路,则有胶体生成(或者有丁达尔现象)
(3)①胶粒带正电 ②先生成红褐色的沉淀,后溶解为黄色溶液
29.答案:(1)盐酸 ;
(3)还原性
(4)
(5);去除HCl;干燥纸条不褪色,湿润纸条褪色
30.答案:(1)13.6
(2)C
(3)BADCE
(4)AE
勃利县高级中学2022-2023学年高一下学期开学考试化学试卷(含答案): 这是一份勃利县高级中学2022-2023学年高一下学期开学考试化学试卷(含答案),共15页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。
黑龙江省牡丹江市第三高级中学2021-2022学年高一上学期期末考试化学试题(Word版含答案): 这是一份黑龙江省牡丹江市第三高级中学2021-2022学年高一上学期期末考试化学试题(Word版含答案),共7页。
勃利县高级中学2022-2023学年高二下学期期末考试化学试卷(含答案): 这是一份勃利县高级中学2022-2023学年高二下学期期末考试化学试卷(含答案),共14页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。












