

2024年江苏高考化学一轮复习 第11讲 硫及其化合物 课时练(含解析)
展开第11讲 硫及其化合物
硫 二氧化硫
1. 判断正误,正确的打“√”,错误的打“×”。
(1) 用Na2SO3溶液吸收过量Cl2,发生反应的离子方程式为3SO+Cl2+H2O===2HSO+2Cl-+SO( )
(2) 向久置的FeCl2溶液中加入几滴KSCN溶液,溶液变红色,说明FeCl2全部被氧化( )
(3) 二氧化硫可广泛用于食品的增白( )
(4) SO2气体通入Ba(NO3)2溶液可以到BaSO4( )
(5) 将SO2通入溴水中能证明SO2具有漂白性( )
(6) H2O2氧化SO2的化学方程式为H2O2+SO2===H2SO4( )
(7) (2019·江苏卷)在0.1 mol/L 硫酸溶液中,K+、NH、NO、HSO离子可以共存( )
(8) 如图1所示装置可用于 Na2SO3 和浓硫酸制取少量的 SO2 气体( )
图1 图2
(9) 如图2表示常温下酸雨在空气中放置时 pH 的变化( )
(10) (2021·广东卷)SO2通入酸性KMnO4溶液中离子方程式为5SO2 + 2H2O + 2MnO===2Mn2++5SO+ 4H+ ( )
2. (2022·常州期末)工业上利用反应S8(s)4S2(g)、CH4(g)+2S2(g)===CS2(g)+2H2S(g)制备CS2。下列说法正确的是( )
A. S8()为极性分子
B. S8与S2互为同位素
C. CS2的电子式为
D. CH4和H2S的键角相等
3. (2022·扬州期末)下列有关说法正确的是( )
A. CO的空间结构为三角锥形
B. SO2与SO3中硫原子的杂化轨道类型均是sp2
C. SO2的键角比SO3的大
D. 1 mol [Cu(H2O)4]2+中含有8 mol σ键
4. (2021·扬州一模改编)下列有关SO2的说法正确的是( )
A. SO2在大气中不能转化为SO3
B. SO2通入BaCl2溶液中生成白色沉淀
C. SO2的水溶液放置在空气中,pH增大
D. 生产SO3时SO2表现出还原性
5. (2022·江苏模拟)下列说法不正确的是( )
A. SO2通入Ba(NO3)2溶液中,产生白色沉淀BaSO4
B. SO2有还原性,所以能使溴水褪色
C. 用酸性KMnO4溶液除去CO2中含有的少量SO2
D. SO2与过量漂白粉浊液反应生成CaSO3
6. 为探究SO2与O2反应后混合气体的成分,某小组设计如下实验装置。下列说法不正确的是( )
A. Ⅰ处浓硫酸起干燥作用,可通过观察气泡产生速率来控制气体的混合比例
B. Ⅱ处V2O5作催化剂,不参与化学反应却能加快反应速率
C. Ⅲ处溶液为BaCl2溶液,若有白色沉淀产生,说明混合气体中含有SO3
D. Ⅴ处溶液是为了检验SO2存在,可盛放品红溶液或酸性高锰酸钾溶液
7. (2022·南京、盐城一模)将工业废气中的SO2吸收能有效减少对大气的污染,并实现资源化利用。下列离子方程式书写正确的是( )
A. 硫酸型酸雨露置于空气中一段时间后溶液酸性增强:H2SO3+O2===2H++SO
B. 用过量饱和Na2CO3溶液吸收废气中的SO2:
2CO+SO2+H2O===SO+2HCO
C. 用过量氨水吸收废气中的SO2:
NH3·H2O+SO2===HSO+NH
D. 用Ca(ClO)2溶液吸收废气中的SO2:
Ca2++2ClO-+SO2+H2O===2HClO+CaSO3↓
8. (2021·江苏模拟)下列反应对应的离子方程式的书写正确的是( )
A. 向溴水中通入SO2:
Br2+SO2+2H2O===2HBr+SO+2H+
B. 向酸性K2Cr2O7溶液中加入NaHSO3溶液,+6价铬元素被还原为Cr3+:3HSO+Cr2O+5H+===3SO+2Cr3++4H2O
C. 向Ba(OH)2溶液中滴入NaHSO4溶液至Ba2+恰好完全沉淀:Ba2++2OH-+2H++SO===BaSO4↓+2H2O
D. NaHSO4溶液与Ba(OH)2溶液反应至中性:
H++SO+Ba2++OH-===BaSO4↓+H2O
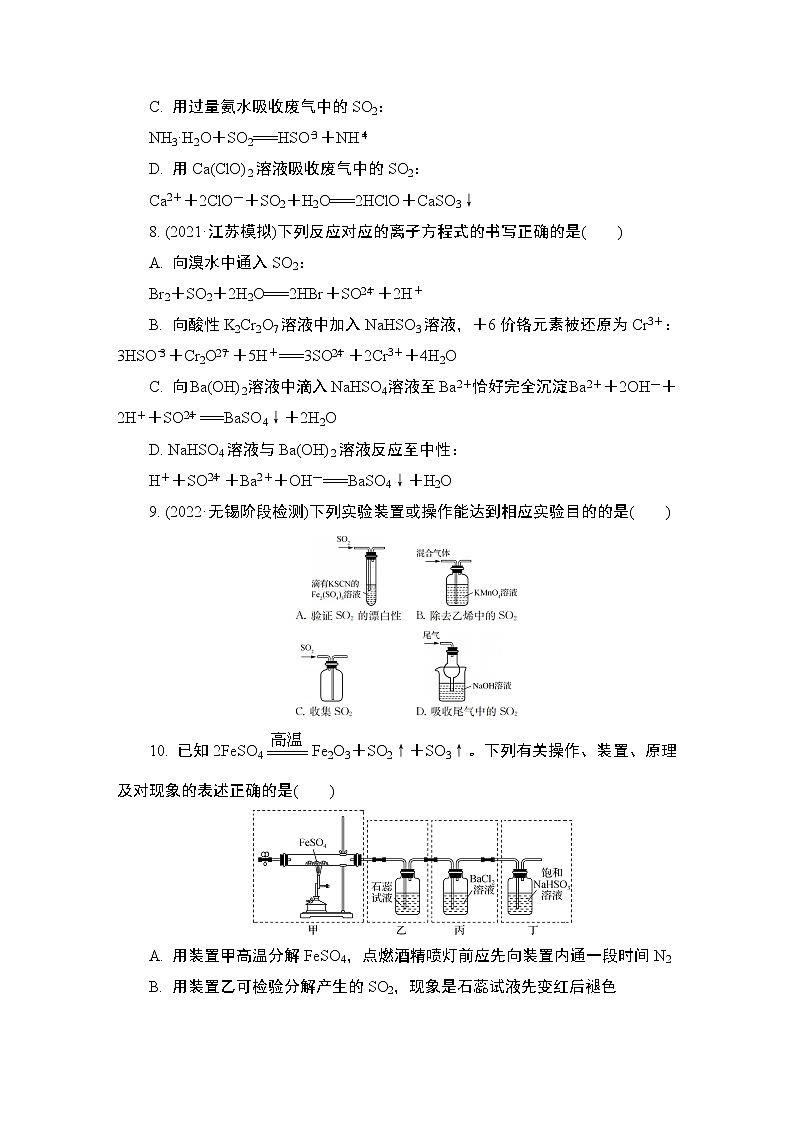
9. (2022·无锡阶段检测)下列实验装置或操作能达到相应实验目的的是( )
10. 已知2FeSO4Fe2O3+SO2↑+SO3↑。下列有关操作、装置、原理及对现象的表述正确的是( )
A. 用装置甲高温分解FeSO4,点燃酒精喷灯前应先向装置内通一段时间N2
B. 用装置乙可检验分解产生的SO2,现象是石蕊试液先变红后褪色
C. 用装置丙可检验分解产生的SO3,现象是产生白色沉淀
D. 用装置丁可吸收尾气,避免污染环境
11. (2022·广东质检)某同学用浓硫酸与亚硫酸钠制备SO2并探究其相关性质,实验装置如图所示。下列说法错误的是( )
A. 装置①中可以用Cu片代替Na2SO3
B. 装置②中溴水可以用酸性高锰酸钾溶液代替
C. 装置③中出现浑浊,说明SO2具有氧化性
D. 装置④的作用是吸收SO2,防止发生倒吸和污染环境
12. (2021·江苏模拟)根据下列实验操作和现象所得出的结论或解释正确的是( )
选项
实验操作和现象
结论或解释
A
向淀粉碘化钾溶液中通入Cl2,再通入SO2,溶液先出现蓝色,后蓝色褪去
还原性:
SO2>I->Cl-
B
检验SO2气体中是否混有SO3(g):将气体通入Ba(NO3)2溶液中,有白色沉淀生成
混有SO3(g)
C
将SO2通入Na2CO3溶液中生成的气体,先通入足量的酸性KMnO4溶液,再通入澄清石灰水中,溶液变浑浊
说明酸性:
H2SO3
将某气体通入品红溶液中,品红溶液褪色
该气体一定是SO2
硫及其化合物综合
1. (2022·佛山质检)火山喷发是硫元素在自然界中转化的重要途径,反应过程如图所示。下列说法错误的是( )
A. SO3由SO2氧化产生
B. FeS2等矿物转化为石膏时,需要暴露于地球表面
C. 火山喷发时收集的雨水,放置时pH变大
D. 火山喷发口附近可能发现硫黄
2. (2022·七市二模)下列有关H2S、SO2、SO、SO的说法正确的是( )
A. H2S的稳定性比H2O的强
B. SO2与H2S反应体现SO2的还原性
C. SO的空间结构为平面三角形
D. SO中S原子轨道杂化类型为sp3
3. (2022·南师附中)下列硫及其化合物的性质与用途具有对应关系的是( )
A. S有氧化性,可用于生产SO2
B. Na2SO3溶液显碱性,可用于吸收少量SO2
C. 硫单质呈黄色,可用作橡胶硫化剂
D. 浓硫酸有脱水性,可用作氧气干燥剂
4. 下列叙述正确的是( )
A. 浓硫酸是一种干燥剂,能够干燥气体CO2、O2、Cl2、SO2,但不能干燥气体NH3、HI、H2S
B. 浓硫酸与S反应的化学方程式为2H2SO4(浓)+S3SO2↑+2H2O,在此反应中,浓硫酸既表现了强氧化性又表现了酸性
C. 把足量的铜粉投入只含2 mol H2SO4的浓硫酸中,得到的气体体积在标准状况下为22.4 L
D. 常温下将Cu片置于浓硫酸中,无明显现象,说明Cu在冷的浓硫酸中钝化
5. (2022·江苏模拟)探究铜和浓硫酸的反应,下列装置或操作正确的是( )
甲 乙 丙 丁
A. 用装置甲能进行铜和浓硫酸的反应
B. 装置乙可用于收集SO2气体
C. 为确认甲中有CuSO4生成,将烧瓶中剩余物质倒入装置丙中稀释,观察颜色
D. 用装置丁测定余酸的浓度
6. (2022·徐州打靶卷)通过如下实验进行浓硫酸性质的探究。
步骤Ⅰ:取2 g蔗糖放入大试管中,加入2~3滴水,向试管中再加入约3 mL浓硫酸,迅速搅拌,然后塞紧带玻璃导管的橡皮塞,观察现象。
步骤Ⅱ:将玻璃导管的另一端插入盛有品红溶液的试管中,观察现象。
下列说法错误的是( )
A. 步骤Ⅰ中加入少量水的目的利用了浓硫酸遇水放热的性质
B. 步骤Ⅱ中品红溶液褪色体现了SO2的漂白性
C. 蔗糖变黑说明浓硫酸可使有机化合物炭化,有脱水性
D. 如图是一种碳单质的晶胞结构,每个C原子周围最近的C原子为12个
7. (2022·苏北七市二模改编)在指定条件下,下列选项所示的物质间的转化能实现的是( )
A. Na2SS B. SOS
C. SO2BaSO3 D. NaHSO3(aq)SO2
8. (2022·江苏模拟)室温下,下列各组离子在指定溶液中能大量共存的是( )
A. 0.1 mol/L H2SO4溶液:
Mg2+、K+、Cl-、NO
B. 0.1 mol/L Na2SO3溶液:
K+、H+、SO、NO
C. 0.1 mol/L KHSO3溶液:
Na+、NH、MnO、ClO-
D. 使pH试纸显蓝色的溶液中:
Na+、K+、Cl-、HSO
9. (2021·盐城三模)Na2SO3溶液是工业上常用的还原剂、防腐剂、去氯剂等。下列离子方程式正确的是( )
A. Na2SO3溶液在空气中易被氧化:
SO+O2===SO
B. Na2SO3溶液用作去氯剂:
Cl2+SO+H2O===2H++2Cl-+SO
C. 0.1 mol/L Na2SO3溶液pH>7:
SO+2H2OH2SO3+2OH-
D. 过量SO2与NaOH溶液反应生成Na2SO3溶液:SO2+2OH-===SO+H2O
10. (2021·江苏模拟)根据下列实验操作和现象所得出的结论或解释正确的是( )
选项
实验操作和现象
结论或解释
A
向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成
该溶液中一定含有SO
B
向某溶液中加入盐酸产生无色气体,该气体能使澄清石灰水变浑浊
该溶液中一定含有CO或SO
C
将亚硫酸钠样品溶于水,加入盐酸酸化的Ba(NO3)2溶液,有白色沉淀产生
无法判断样品是否已变质
D
向某溶液中加入盐酸,将生成的气体通入品红溶液中,品红溶液褪色
该溶液一定含有SO
11. 检验碳粉与浓硫酸反应产生气体的装置和所加药品如图所示。下列叙述不正确的是( )
A. a中品红溶液褪色,说明混合气体中有SO2
B. b中酸性KMnO4溶液的作用是除去SO2
C. b中发生反应的离子方程式为5SO2+4H++2MnO===5SO+2H2O+2Mn2+
D. c中品红溶液不褪色,d中Ca(OH)2溶液变浑浊,说明混合物中存在CO2
12. 部分含硫物质的分类与相应硫元素化合价如图所示。下列说法正确的是( )
A. 将a通入至c的水溶液中,有黄色浑浊出现
B. 将c通入紫色石蕊试液至过量,溶液先变红后褪色
C. 足量的b与56 g铁粉充分反应,转移电子的物质的量为3 mol
D. 可以向f的浓溶液和Cu反应后的试管中加入少量水,观察颜色变化以判断产物
13. 天然气是一种重要的化工原料和燃料,常含有少量H2S。一种在酸性介质中进行天然气脱硫的原理示意图如图所示。下列说法正确的是( )
A. 脱硫过程中Fe2(SO4)3溶液的pH逐渐减小
B. CH4是天然气脱硫过程的催化剂
C. 脱硫过程需不断补充FeSO4
D. 整个脱硫过程中参加反应的n(H2S)∶n(O2)=2∶1
14. 已知:2H2SO4(浓)+CCO2↑+2SO2↑+2H2O,下图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,填写下列空白:
(1) 无水硫酸铜的作用是___________________________________,
a的作用是______________________________________,
b的作用是__________________________,
c的作用是____________________________,
澄清石灰水的作用是____________________________________。
(2) 若将仪器的连接顺序变为①③②,则可以检出的物质是________;不能检出的物质是___________________________________。
第11讲 硫及其化合物
硫 二氧化硫
1. (1) × (2) × (3) × (4) √ (5) × (6) √ (7) × (8) × (9) × (10) √
【解析】 (8) Na2SO3为粉末状固体,会顺着塑料板的小孔进入溶液中,所以不能使用此装置制取SO2,错误。(9) 起初时,酸雨的pH不会大于7, 错误。
2. C 【解析】 根据S8的结构可知,其为非极性分子,A错误;S8与S2互为同素异形体,B错误;CS2的结构与CO2分子相似,C正确;CH4分子中没有孤电子对,C原子为sp3杂化,正四面体形结构,H—C—H夹角是109°28′,H2S分子中有两个孤电子对,对成键电子对排斥力较大,导致H—S—H夹角变小,D错误。
3. B 【解析】 CO的中心C原子没有孤电子对,故为平面正三角形结构,A错误;SO2分子中心S原子含有一个孤电子对,而SO3分子的中心S原子没有孤电子对,故两者中S原子均采用sp2杂化,B正确;SO2是V形结构,SO3是平面正三角形结构,由于孤电子对对成键电子对的斥力大于成键电子对之间的斥力,故SO2的键角小,C错误;Cu与H2O分子间是配位键,配位键也是σ键,每个H2O分子中含有两个σ键,故含有12 mol σ键,D错误。
4. D 【解析】 空气中的SO2可在飘尘、氮的氧化物作用下被氧化成SO3,A错误;SO2与BaCl2溶液不反应,B错误;SO2的水溶液中含有H2SO3,在空气中放置时被O2氧化生成H2SO4,故pH减小,C错误;SO2被O2氧化成SO3,SO2表现出还原性,D正确。
5. D 【解析】 SO2的水溶液显酸性,在酸性溶液中,SO2能被NO氧化成SO,故得到的白色沉淀为BaSO4,A正确;SO2能与Br2反应生成H2SO4和HBr,SO2表现出还原性,B正确;SO2能被酸性高锰酸钾溶液氧化,而CO2不能被氧化,C正确;由于漂白粉具有强氧化性,故SO2与漂白粉浊液反应后生成CaSO4而不是CaSO3,D错误。
6. B 【解析】 SO2和O2均可用浓硫酸来干燥,且同温同压下,气体的体积之比等于其物质的量之比,A正确;催化剂参与化学反应,改变反应的活化能,从而影响反应速率,B错误;由于SO2与BaCl2溶液不反应,而SO3+H2O+BaCl2===BaSO4↓+2HCl,故Ⅲ处溶液为BaCl2溶液,若有白色沉淀产生,则说明混合气体中含有SO3,C正确;SO2具有漂白性,能使品红溶液褪色,同时具有还原性,故能使酸性高锰酸钾溶液褪色,D正确。
7. B 【解析】 H2SO3被氧化的离子方程式为2H2SO3+O2===4H++2SO,A错误;过量氨水吸收SO2时生成的是(NH4)2SO3而不是NH4HSO3,C错误;Ca(ClO)2具有强氧化性,通入SO2后生成的是CaSO4,D错误。
8. B 【解析】 HBr为强电解质,在离子方程式中要拆成离子,A错误;向Ba(OH)2溶液中滴入NaHSO4溶液至Ba2+恰好完全沉淀的离子方程式为H++SO+Ba2++OH-===BaSO4↓+H2O,C错误;NaHSO4溶液与Ba(OH)2溶液反应至中性的离子方程式为2H++SO+Ba2++2OH-===BaSO4↓+2H2O,D错误。
9. D
10. A 【解析】 点燃酒精喷灯前应先向装置内通一段时间N2,排尽装置内空气,避免空气中氧气的干扰,A正确;装置乙不能检验二氧化硫的存在,产物中有三氧化硫溶于水形成硫酸溶液,遇到石蕊试液变红色,则二氧化硫遇到石蕊试液不会褪色,B错误;三氧化硫极易溶于水,通过装置乙的水溶液会被完全吸收,装置丙中无法检验三氧化硫存在,应把乙和丙位置互换才能检验三氧化硫的存在,C错误;装置丁中饱和亚硫酸氢钠溶液不能吸收二氧化硫,D错误。
11. A 【解析】 浓硫酸与铜在加热条件下才能发生反应生成硫酸铜、二氧化硫和水,该装置缺少酒精灯,A错误;二氧化硫使溴水褪色,发生反应:SO2+Br2+2H2O===2HBr+H2SO4,体现二氧化硫的还原性,二氧化硫与高锰酸钾发生氧化还原反应,二氧化硫表现还原性,装置②中溴水可以用酸性高锰酸钾溶液代替,B正确;SO2中硫元素为+4价,Na2S中硫元素为-2价,两者发生氧化还原反应生成S单质,使溶液出现浑浊,说明SO2具有氧化性,C正确;CCl4的密度大于NaOH溶液,SO2难溶于CCl4,CCl4在下层,可以起到防倒吸的作用,二氧化硫为大气污染物,装置④用氢氧化钠溶液吸收SO2,可防止污染环境,D正确。
12. A 【解析】 由于SO2、SO3溶于水中都生成相应的酸,提供H+,而Ba(NO3)2能提供NO,相当于溶液中含有HNO3,故能将SO2氧化成SO,B错误;用酸性KMnO4溶液除去SO2,澄清石灰水变浑浊,说明有CO2生成,则H2SO3的酸性强于H2CO3,C错误;该气体也可能是Cl2、O3等,D错误。
硫及其化合物综合
1. C 【解析】 由SO2转化为SO3的过程中,S元素的化合价升高被氧化,故SO3由SO2氧化产生,A正确;FeS2等矿物转化为石膏(主要成分为CaSO4)时,需要被氧气氧化,故需要暴露于地球表面,B正确;火山喷发时收集的雨水,放置时由于发生反应:2H2SO3+O2===2H2SO4,故溶液酸性增强,pH变小,C错误;火山喷发的气体中含有硫化氢和二氧化硫,二者相遇后可发生反应,生成硫黄,所以火山喷发口附近可能发现硫黄,D正确。
2. D 【解析】 由于电负性:O>S,故稳定性:H2O>H2S,A错误;SO2与H2S反应时,SO2中的硫元素转变为硫单质,体现了SO2的氧化性,B错误;SO的中心硫原子中有一个孤电子对,空间结构为三角锥形,C错误。
3. B 【解析】 由S得到SO2,硫元素化合价升高,表现还原性,A错误;硫原子能把橡胶分子连接起来使线型结构变成网状结构,提高强度,与硫单质为黄色无关,C错误;浓硫酸有吸水性,可用作氧气干燥剂,D错误。
4. A 【解析】 浓硫酸与单质硫反应时,只表现强氧化性,B错误;随着反应的进行当浓硫酸变为稀硫酸,稀硫酸不再与铜粉反应,故得到的气体体积在标准状况下小于22.4 L,C错误;常温下Cu与浓硫酸无法生成致密的氧化膜,不能发生钝化,D错误。
5. C 【解析】 铜和浓硫酸反应需要酒精灯加热,A错误;二氧化硫的密度比空气的大,因此用装置乙收集二氧化硫时,应长进短出,B错误;将烧瓶中的剩余物质倒入装置丙中,若变蓝,则有硫酸铜生成,C正确;NaOH溶液不应该放在酸式滴定管中,应该放在碱式滴定管中,D错误。
6. D 【解析】 浓硫酸加水稀释会放出大量热量,步骤Ⅰ中加入少量水的目的利用了浓硫酸遇水放热的性质,可为浓硫酸与蔗糖反应提供热量,A正确;浓硫酸具有脱水性,碳和浓硫酸发生氧化还原反应生成二氧化碳和SO2气体,步骤Ⅱ中品红溶液褪色,体现了SO2的漂白性,B正确;浓硫酸具有脱水性,蔗糖变黑说明浓硫酸可使有机化合物炭化,C正确;由晶胞可知,每个C原子周围最近的C原子为4个,D错误。
7. A 【解析】 S2-具有强还原性,能被Cl2氧化为S单质,A正确;根据氧化还原反应中价态转化规律可知,SO与SO2中硫元素处于相邻价态,两者不能反应,B错误;由于酸性:HCl>H2SO3,故反应不能发生,C错误;由于酸性:H2SO3>H2CO3,故NaHSO3溶液与CO2不反应,D错误。
8. A 【解析】 NO在有H+的条件下,能氧化SO,B错误;MnO、ClO-具有强氧化性,能够氧化HSO,C错误;使pH试纸显蓝色的溶液为碱性溶液,OH-与HSO不能大量共存,D错误。
9. B 【解析】 O原子不守恒,A错误;SO一级水解得到HSO,C错误;过量SO2与NaOH溶液反应生成NaHSO3,D错误。
10. C 【解析】 该溶液中还可能含有Ag+或SO,A错误;使澄清石灰水变浑浊的气体可能为CO2、SO2,溶液中可能存在CO、HCO、SO或HSO,B错误;盐酸酸化的Ba(NO3)2溶液,相当于含有HNO3,能将亚硫酸钠氧化成硫酸钠,C正确;该溶液也可能含HSO,D错误。
11. C 【解析】 O原子和电荷均不守恒,b中发生反应的离子方程式为5SO2+2H2O+2MnO===5SO+4H++2Mn2+,C错误。
12. A 【解析】 a为H2S,b为S,c为SO2,发生的反应为2H2S+SO2===3S↓+2H2O,A正确;将SO2通入紫色石蕊试液至过量,溶液只变红不褪色,B错误;S为弱氧化剂,足量的S与56 g铁粉充分反应生成FeS,转移电子的物质的量为2 mol,C错误;应将浓硫酸和Cu反应后的混合物倒入水中,观察颜色变化以判断产物,D错误。
13. D 【解析】 在脱硫过程中,Fe2(SO4)3与H2S发生反应:Fe2(SO4)3+H2S===2FeSO4+H2SO4+S↓,然后发生反应:4FeSO4+O2+2H2SO4===2Fe2(SO4)3+2H2O,总反应为2H2S+O2===2S↓+2H2O,可见脱硫过程中由于反应产生水,使Fe2(SO4)3溶液的浓度逐渐降低,因此溶液的pH逐渐增大,A错误;CH4在反应过程中没有参加反应,因此不是天然气脱硫过程的催化剂,B错误;脱硫过程反应产生中间产物FeSO4,根据脱硫过程发生的两个反应知,FeSO4的物质的量不变,因此不需补充FeSO4,C错误;根据总反应化学方程式:2H2S+O2===2S↓+2H2O可知,n(H2S)∶n(O2)=2∶1,D正确。
14. (1) 检验H2O 检验SO2 除去SO2 检验SO2是否除尽 检验CO2 (2) H2O、SO2 CO2
【解析】 (1) 检验生成的水用无水硫酸铜,检验SO2用品红溶液,吸收SO2用酸性KMnO4溶液,检验CO2用澄清石灰水;在检验CO2之前,必须除尽SO2,因为SO2也能使澄清石灰水变浑浊,c装置用于检验SO2是否除尽,若品红未褪成无色,证明SO2已除尽。(2) 装置③和装置②位置不得变更,因为SO2、CO2均能使澄清石灰水变浑浊,故在用澄清石灰水来验证CO2前一定要排除SO2的干扰。
高考化学一轮复习讲练 第4章 第15讲 硫及其化合物 (含解析): 这是一份高考化学一轮复习讲练 第4章 第15讲 硫及其化合物 (含解析),共25页。试卷主要包含了6,形成酸雨等内容,欢迎下载使用。
2024年江苏高考化学一轮复习 第8讲 铁及其化合物 课时练(含解析): 这是一份2024年江苏高考化学一轮复习 第8讲 铁及其化合物 课时练(含解析),共17页。试卷主要包含了 利用H2和CO2合成甲醇, 铁黄是一种重要的化工产品等内容,欢迎下载使用。
2024年江苏高考化学一轮复习 第7讲 钠及其化合物 课时练(含解析): 这是一份2024年江苏高考化学一轮复习 第7讲 钠及其化合物 课时练(含解析),共13页。试卷主要包含了 下列关于钠的说法中不正确的是, 钙和钠相似,也能形成过氧化物,5 ml氧气, 有关Na2O2性质实验如下等内容,欢迎下载使用。












