




【高考化学模拟】高考名校仿真模拟联考试题(新课标全国卷)(07)
展开高考生物复习策略(仅供参考)
1、落实考点。一轮复习时要在熟读课本、系统掌握基础知识、基本概念和基本原理后,要找出重点和疑点;通过结合复习资料,筛选出难点和考点,有针对地重点复习。
2、注重理论联系实际,高三生物的考试并不仅仅是考概念,学会知识的迁移非常重要,并要灵活运用课本上的知识。
3、一轮复习基础知识的同时,还要重点“攻坚”,突出对重点和难点知识的理解和掌握。
这部分知识通常都是学生难于理解的内容,做题时容易出错的地方。分析近几年的高考生物试题,重点其实就是可拉开距离的重要知识点。
4、学而不思则罔,思而不学则殆。
这一点对高三生物一轮复习很重要。尤其是对于错题。错题整理不是把错题抄一遍。也不是所有的错题都需要整理。
高考名校仿真模拟联考试题(新课标全国卷)
化学(七)
第一部分 选择题
一、选择题:本题共7小题,每小题6分,在每小题给出的四个选项中,只有一项是符合题目要求的.
1.我国湖笔的制作技艺属于国家非物质文化遗产,相传古人制作该毛笔的过程为“以枯木为管,鹿毛为柱,羊毛为被(外衣)”,下列说法不正确的是
A.枯木、鹿毛、羊毛的主要成分均为天然高分子化合物,且均能够水解
B.枯木等木材隔绝空气加强热可以得到焦炭、苯、甲苯等
C.鹿毛的成分中一定含有C、H、O、N元素
D.采用灼烧法可以区分毛笔的 “外衣”是羊毛还是化学纤维
2.2019年5月国际上将使用新的“摩尔”定义,新的定义中指出阿伏加德罗常数将是一个确定的常数,设为阿伏加德罗常数的值,下列说法一定正确的是
A.含0.40 mol HCl的浓盐酸与足量的反应,可以生成0.1个分子
B.2.24 L(标准状况下)与金属完全反应时,转移电子数为0.4
C.由D和构成的水()中含有12个中子
D.40.0 g金刚砂(SiC)含有4个共价键
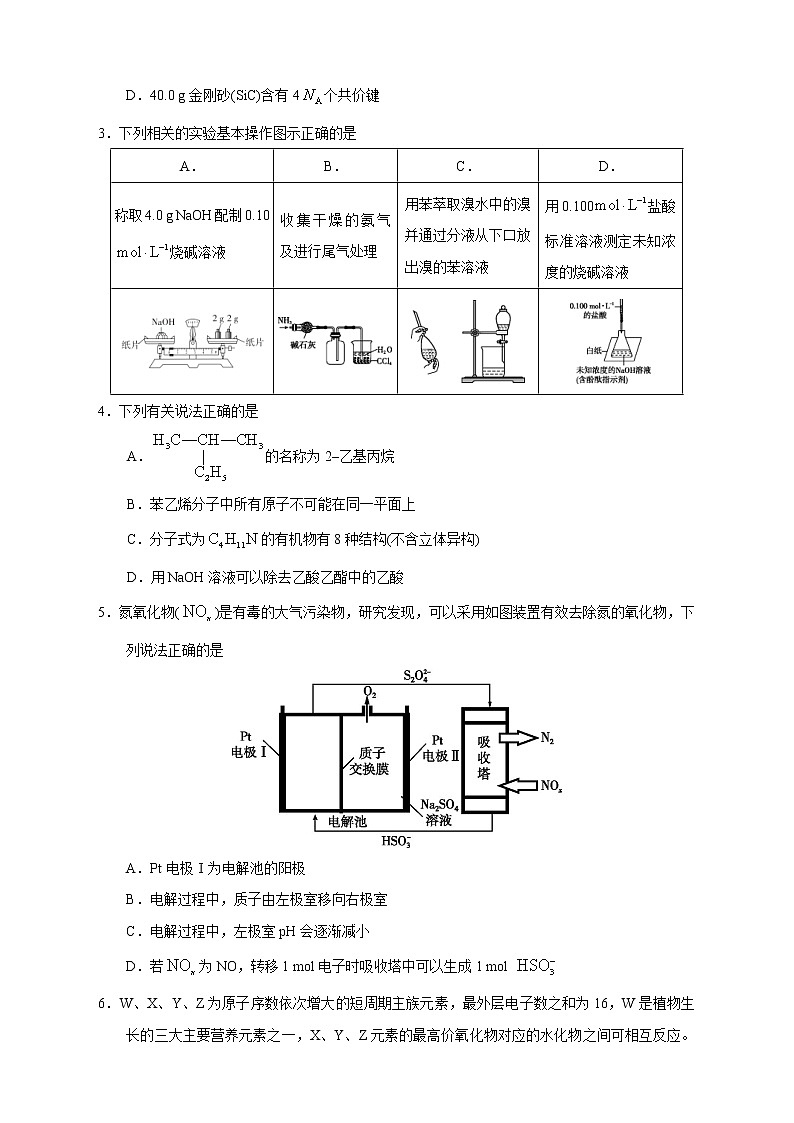
3.下列相关的实验基本操作图示正确的是
A. | B. | C. | D. |
称取4.0 g NaOH配制0.10 烧碱溶液 | 收集干燥的氨气及进行尾气处理 | 用苯萃取溴水中的溴并通过分液从下口放出溴的苯溶液 | 用0.100盐酸标准溶液测定未知浓度的烧碱溶液 |
4.下列有关说法正确的是
A.的名称为2‒乙基丙烷
B.苯乙烯分子中所有原子不可能在同一平面上
C.分子式为的有机物有8种结构(不含立体异构)
D.用NaOH溶液可以除去乙酸乙酯中的乙酸
5.氮氧化物()是有毒的大气污染物,研究发现,可以采用如图装置有效去除氮的氧化物,下列说法正确的是
A.Pt电极Ⅰ为电解池的阳极
B.电解过程中,质子由左极室移向右极室
C.电解过程中,左极室pH会逐渐减小
D.若为NO,转移1 mol电子时吸收塔中可以生成1 mol
6.W、X、Y、Z为原子序数依次增大的短周期主族元素,最外层电子数之和为16,W是植物生长的三大主要营养元素之一,X、Y、Z元素的最高价氧化物对应的水化物之间可相互反应。下列说法正确的是
A.简单离子半径:Z>Y>X>W
B.W与X可以形成也可以形成
C.Y和Z形成的二元化合物的水溶液呈中性
D.X与氧形成的化合物一定不含共价键
7.向含和的溶液中逐滴加入0.1的NaOH溶液,沉淀的质量与加入NaOH溶液体积的关系如图所示,已知,下列说法正确的是
A.原溶液中
B.该实验不能证明
C.水的电离程度:A>B>C
D.若向悬浊液中加入溶液,一定会有生成
第二部分 非选择题
分为必考题和选考题两部分
(一)必考题(共43分)
8.氯化亚铜(CuCl)在化工生产中常用作催化剂、媒染剂、脱色剂等。已知CuCl固体呈白色,微溶于水,难溶于乙醇,易被氧化。将通入与盐酸的混合溶液中即可制得CuCl,如图是实验室制备氯化亚铜的装置图(夹持装置已略)。
请回答下列问题:
(1)装置A中,使用70%的溶液比使用98%的溶液制备的反应速
率 (填“快”或“慢”)。
(2)装置B中导气管末端a处为多孔球泡,其作用是 。
(3)装置B中,随着反应进行,除生成氯化亚铜白色沉淀外,还可以观察到有白雾产生,写出发生反应的化学方程式 。
(4)实验操作过程中,通常先打开分液漏斗,反应一段时间后再打开恒压滴液漏斗让产生的与溶液反应,其原因是 。
(5)从装置B中获得氯化亚铜晶体,需要经过过滤、洗涤、真空干燥等操作。洗涤时一般选用乙醇作洗涤液,其优点是 。
(6)反应完毕,装置B中溶液共50.0 mL,取20.0 mL该溶液,滴加足量溶液可以得到2.33 g白色沉淀,若与盐酸混合溶液中=2.0,则制备氯化亚铜过程中,至少需要滴加该混合溶液的体积为 mL。
(7)实验研究表明,将铜粉放入一定浓度的氯化铜和盐酸的混合溶液中,也可以制备沉淀物氯化亚铜。
①写出该反应的离子方程式 。
②通过计算说明该反应能够进行完全的原因 (已知
=7.6×;=2.0×;大于1.0×,可以认为完全反应)。
9.和是高效消毒剂,已知为黄绿色气体,浓度较高时易爆炸,受热易分解。和均可由制备。其生产工艺流程如图所示。
请回答下列问题:
(1)写出发生器中与反应生成的离子方程式 。
(2)发生器中草酸()与氯酸钠也可以直接反应生成,该反应中氧化剂与还原剂的物质的量之比为 ;化工生产中加入草酸()的目的是 。
(3)若直接使用NaOH溶液吸收,得到的溶液中的纯度较低,原因是 。
(4)用NaOH溶液吸收,若同时加入,则生成的纯度较高,原因
是 (用离子方程式说明)。
(5)从吸收池中获得晶体,一般需要采用减压蒸发操作,目的是 。
(6)有效氯含量的定义为每克含氯消毒剂的氧化能力相当于多少克氯气的氧化能力。若上述生产得到的产品中检测得出有效氯含量为0.8,则该产品的纯度
为 。
(7)用处理自来水后,常有少量残留,水厂一般采用碘量法进行如下检测(已知存在于pH为4~6的溶液中,存在于中性溶液中;
):
①取0.50 L水样,加入一定量的碘化钾和氢氧化钠溶液,反应后溶液呈中性,再加入淀粉溶液,溶液变蓝。写出此时水样中与碘化钾反应的化学方程式 。
②向①所得溶液中滴加5.00× 的标准溶液至恰好反应,消耗溶液20.00 mL。判断达到滴定终点的方法是 ;该水样中的浓度是 。
10.氨的合成一直是众多科学家研究的热门领域,回答下列相关问题:
(1)关于的说法正确的是 (填标号)。
A.属于弱电解质,水溶液导电性弱于相同浓度的烧碱溶液
B.与硫酸、硝酸相遇,可以产生白烟现象
C.易液化,常用作制冷剂
D.是制备硝酸的主要原料,其中氨被氧化
E.是制备尿素、碳铵的原料,其过程属于氮的固定
(2)氢气是合成氨的原料气,其制备的方法中目前常用天然气作原料,已知:
① =+206.2
② =+247.4
写出(g)与(g)反应生成(g)和(g)的热化学方程式 。
(3)理论上与在室温下可以自发进行合成氨的反应,其原因是 。
(4)①在2 L恒容密闭容器中,充入0.60 mol (g)和1.60 mol (g)进行合成氨反应,研究发现在A、B、C三种不同的催化剂作用下,氨气的体积分数随反应时间的变化趋势如图所示。
计算在A催化剂作用下,0~4 min内反应速率= ;氮气的转化率= 。
②针对上述合成氨的反应,下列说法正确的是 (填标号)。
a.该反应的活化能大小顺序为
b.使用催化剂,可以使反应活化分子的百分数增大
c.使用催化剂,可以使反应的平衡常数增大,生成物含量增加
d.使用高效的催化剂,可提高原料的平衡转化率
(5)已知合成氨反应: =46.2 ,标准平衡常数,其中为标准压强,、、为各组分的平衡分压,如,为平衡总压,为平衡系统中的物质的量分数。若往一密闭容器中加入的、起始物质的量之比为1∶3,反应在恒定温度和标准压强下进行,的平衡产率为,则= (用含的最简式表示)。
(6)据文献报道在常温、常压和特定的催化剂作用下,会与水发生反应,反应原理为 =+765.2 。若一定量的和在绝热恒容的条件下发生上述反应,下列可以作为判断该反应达到平衡的标志有 。
a.混合气体的密度不变
b.混合气体中氨气的含量不变
c.氨气与氧气的物质的量之比不变
d.容器内温度不变
(二)选考题(共15分)。请从2道化学题中任选一题作答。如果多做,则按所做第一题计分。
11.[化学─选修3:物质结构与性质](15分)
钠、铝、钛的化合物是目前生活与生产上较为常用的物质,回答下列问题:
(1)下列Al原子的价电子排布图中属于激发态的是 ;属于基态的是 。
(2)氯化铝的熔点、沸点都明显低于氧化铝的原因是 。已知氯化铝常以二聚体形式存在,其分子模型为,则1个二聚体分子中含有配位键的个数为 。
(3)硫酸氧钛晶体中的阳离子为链状聚合形式的离子,该阳离子的结构片段如图所示,该阳离子的化学式为 ;阴离子的中心原子的轨道杂化类型为 。
(4)假设某氯化钠纳米颗粒的大小和形状恰好与该化合物的晶胞的大小和形状相同(如图所示),该纳米颗粒具有许多特殊的性质,主要是因为其表面原子数占总原子数的百分比极大,该百分比为 。
(5)钙钛矿()晶体的结构如图所示,Ti位于立方晶胞的顶点,被 个O包围成配位八面体,若晶胞的边长为a nm,则Ca与O间的最短距离为 nm。在钙钛矿晶胞结构的另一种表示中,Ca处于各顶角位置,则Ti处于 位置,O处于 位置。
12.[化学─选修5:有机化学基础](15分)
有机物K是合成普罗帕酮药物的一种重要中间体,合成有机物K的基本流程如下。
已知:
回答下列问题:
(1)有机物K中官能团的名称为 ;F分子中处于同一平面上的原子数最多为 。
(2)反应①的条件及所需试剂为 ;反应③的反应类型为 。
(3)H分子的质谱图中,最大的质荷比为 。
(4)反应⑤的化学方程式为 。
(5)符合下列条件的有机物F的同分异构体的数目为 ;其中核磁共振氢谱为四组峰,峰面积之比为1∶2∶2∶3的结构简式为 。
①属于芳香族化合物 ②可以与碳酸氢钠溶液反应
(6)以有机物C和异丙醇为有机原料,无机试剂任选,参照上述合成路线,写出的合成路线 。
【高考化学模拟】高考名校仿真模拟联考试题(新课标全国卷)(09): 这是一份【高考化学模拟】高考名校仿真模拟联考试题(新课标全国卷)(09),文件包含高考化学模拟高考名校仿真模拟联考试题新课标全国卷09doc、高考化学模拟高考名校仿真模拟联考试题新课标全国卷答案09doc等2份试卷配套教学资源,其中试卷共15页, 欢迎下载使用。
【高考化学模拟】高考名校仿真模拟联考试题(新课标全国卷)(08): 这是一份【高考化学模拟】高考名校仿真模拟联考试题(新课标全国卷)(08),文件包含高考化学模拟高考名校仿真模拟联考试题新课标全国卷08doc、高考化学模拟高考名校仿真模拟联考试题新课标全国卷答案08doc等2份试卷配套教学资源,其中试卷共15页, 欢迎下载使用。
【高考化学模拟】高考名校仿真模拟联考试题(新课标全国卷)(05): 这是一份【高考化学模拟】高考名校仿真模拟联考试题(新课标全国卷)(05),文件包含高考化学模拟高考名校仿真模拟联考试题新课标全国卷05doc、高考化学模拟高考名校仿真模拟联考试题新课标全国卷答案05doc等2份试卷配套教学资源,其中试卷共15页, 欢迎下载使用。












