






人教版化学中考一轮复习--基础梳理--第5课时 溶液(一)(课件)
展开· 考点1 溶液及溶解
· 考点2 溶液的组成及表示方法
考点1 溶液及溶解【6年2考】
①均一、稳定的液体一定是溶液。(×)理由:水均一、稳定,但不是溶液。②溶液一定都是无色的。(×)理由:硫酸铜溶液为蓝色,氯化亚铁溶液为浅绿色。
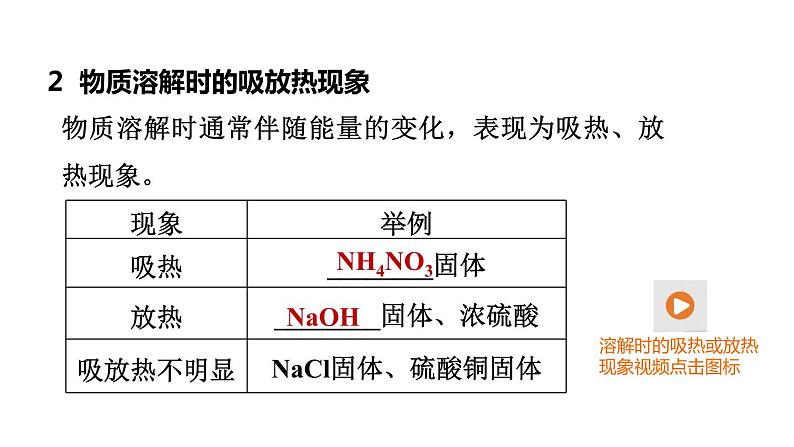
2 物质溶解时的吸放热现象
物质溶解时通常伴随能量的变化,表现为吸热、放热现象。
【注意】CaO固体加入水中也会放热,但它不是溶解放热,而是与水发生化学反应而放出热量。
(1)乳化:当在植物油中加入洗涤剂后,植物油就被分散成无数细小的液滴,而不能聚集成大的油珠,从而使油和水不再分层,这种现象称为乳化。(2)乳化作用:乳化剂所起的作用称为______________。
考点2 溶液的组成及表示方法【6年5考】
【注意】①溶液中未溶解的部分不能视为溶质。②溶液质量=溶质质量+溶剂质量,溶液体积≠溶质体积+溶剂体积。
2 溶质质量分数的计算
例:用27.0gNaCl配制20℃的NaCl饱和溶液(20℃时NaCl的溶解度为36.0g),需要水的质量是_________g。
3 一定质量分数的溶液的配制
(1)用固体配制溶液:配制50g质量分数为6%的氯化钠溶液。
【注意】a.称量固体时,注意“左物右码”,且在托盘两边各放一张质量相等的纸。b.配制溶液应在烧杯中进行,不能在量筒内混合,且用玻璃棒搅拌。
例:a.量取水时俯视读数→溶剂的质量________→溶质质量分数________。b.称量NaCl固体时,药品与砝码颠倒且使用了游码→溶质质量________→溶质质量分数________。c.砝码生锈或沾有污渍→溶质质量______→溶质质量分数________。
d.量取水时仰视读数→溶剂的质量______→溶质质量分数________。e.配制完成后,转移过程中有少量溶液洒出,溶质质量分数________。(2)用浓溶液配制稀溶液:用已配好的质量分数为6%的氯化钠溶液(密度约为1.04g/cm3),配制50g质量分数为3%的氯化钠溶液。①计算:依据稀释前后________的质量不变。
a.浓溶液的质量==________=________g;所需浓溶液的体积为________(保留一位小数)mL。b.加入水的质量=稀溶液的质量-浓溶液的质量=________g。所需水的体积为________mL。
②量取:用规格为________(填“20”“50”或“100”)mL的量筒量取6%氯化钠溶液和所需的水。③混匀:用玻璃棒搅拌,使溶液混合均匀。④装瓶贴标签。
· 考点1 溶液及溶解(1)
· 考点2 溶液的组成及表示方法(2 3 4 5 6)
1.【2022泉州实验中学模拟3分】下列有关物质的性质与用途对应不匹配的是( )
考点1 溶液及溶解
2.【2022福建3分】从植物“地不容”中提取抑制新冠病毒的新药——千金藤素,需用到5%的Na2CO3溶液。若配制100g该溶液,需要称取Na2CO3的质量为( ) A.95g B.90g C.20g D.5g
考点2 溶液的组成及表示方法
3.【2018福建3分】某同学模拟闽籍化学家侯德榜的“侯氏制碱法”制纯碱,需用50.0g水配制20℃的NaCl饱和溶液(20℃时NaCl的溶解度为36.0g),应称取NaCl的质量为( )A.18.0g B.16.0g C.13.2g D.11.5g
4.【2021福建节选4分】如图为我国古代“布灰种盐”生产海盐的部分场景,其过程为“烧草为灰,布在滩场,然后以海水渍之,俟晒结浮白,扫而复淋”。经过多次“扫而复淋”,提高卤水浓度获得“上等卤水”(氯化钠的质量分数约为15%),用于煎炼海盐。
(1)1000g“上等卤水”蒸干后,可得到氯化钠的质量约为________g。(2)从燃料利用角度分析,用获得的“上等卤水”而不直接用海水煎炼海盐的原因是________________________________。
产等量的海盐,后者消耗燃料更多
5.【2020福建节选1分】某84消毒液产品的部分说明如下图。
依据图中信息,将有效氯的质量分数为6.0%的84消毒液与水按质量比为1∶______进行稀释,即可用于餐具消毒。
中考化学复习基础梳理第6课时溶液(二)课件: 这是一份中考化学复习基础梳理第6课时溶液(二)课件,共27页。PPT课件主要包含了易错辨析,溶解度,1固体溶解度,2气体溶解度,溶解度曲线分析,升高温度,甲=乙<丙,乙>丙,甲和乙,丙甲乙等内容,欢迎下载使用。
中考化学复习基础梳理第5课时溶液(一)课件: 这是一份中考化学复习基础梳理第5课时溶液(一)课件,共31页。PPT课件主要包含了溶液的概念与特征,混合物,易错辨析,NH4NO3,NaOH,乳化现象,乳化作用,3除污方法,溶液的组成,操作步骤与方法等内容,欢迎下载使用。
人教版化学中考一轮复习--基础梳理--第10课时 酸和碱(二)(课件): 这是一份人教版化学中考一轮复习--基础梳理--第10课时 酸和碱(二)(课件),共34页。PPT课件主要包含了熟石灰,氢氧化钙的制取,化学性质,Na2CO3+H2O,CaCO3↓+H2O,CaCl2+2H2O,OH-,归纳总结,阳离子,教你来探究等内容,欢迎下载使用。












