
江苏常州市2020-2022三年中考化学真题知识点分类汇编-04碳和碳的氧化物
展开一、单选题
1.(2020·江苏常州·统考中考真题)下列气体含量过多会引起温室效应的是
A.氧气
B.氮气
C.稀有气体
D.二氧化碳
2.(2021·江苏常州·统考中考真题)下列气体既能用排水集气法,又能用向下排空气法收集的是
A.O2B.N2C.CO2D.H2
3.(2021·江苏常州·统考中考真题)下列物质的使用过程主要发生化学变化的是
A.金属丝导电B.盐酸除铁锈C.活性炭除臭D.木材制桌椅
4.(2022·江苏常州·统考中考真题)干冰可用于疫苗等特殊药品的低温运输。下列说法正确的是
A.干冰由水分子构成B.构成干冰的微粒静止不动
C.构成干冰的微粒间无间隙D.干冰升华吸热使环境温度降低
5.(2022·江苏常州·统考中考真题)某阻燃剂主要成分为碱式碳酸镁【Mga(OH)2(CO3)b】,遇热分解生成三种氧化物。称取一定质量阻燃剂样品,充分灼烧(其他成分未发生反应),将产生的气体依次通过浓硫酸和过量澄清石灰水,浓硫酸增重0.18g,澄清石灰水中生成4g白色沉淀。则Mga(OH)2(CO3)b中a值为
A.6B.5C.4D.3
二、填空题
6.(2021·江苏常州·统考中考真题)用符合要求的物质的序号填空:①干冰②金刚石③聚乙烯④明矾
(1)可用于切割玻璃的是__________;
(2)可用于生活净水的是__________;
(3)可用于人工降雨的是____________;
(4)可用于食品包装的是__________。
7.(2021·江苏常州·统考中考真题)青果巷是常州著名的历史文化街区,素有“一条青果,半部常州史”的美称。
(1)青砖瓦勾勒出古巷的容貌。烧制青砖时,需密封窑体,通过煤不完全燃烧生成CO气体,其化学反应方程式为____________。
(2)刘国钧故居中陈列的棉布曾畅销全国,棉布的主要成分是______(选填“天然纤维”或 “合成纤维”)。
(3)常州梳篦是国家级非物质文化遗产。展览的制作梳篦用的铁制工具表面出现了锈蚀,是由于铁与O2和______(填化学式)共同作用形成的。
(4)常州大麻糕香酥松脆,其主要成分是淀粉。淀粉在一定条件下与水反应转化为_______(填名称)其在人体内缓慢氧化提供能量。
8.(2022·江苏常州·统考中考真题)“一勤天下无难事”。请为下列日常生活劳动准备合适的用品(填序号)。
①食醋 ②食盐 ③小苏打 ④活性炭
(1)清洗水壶水垢_______。
(2)去除冰箱异味_______。
(3)烘焙面制糕点_______。
(4)腌制肉类食品_______。
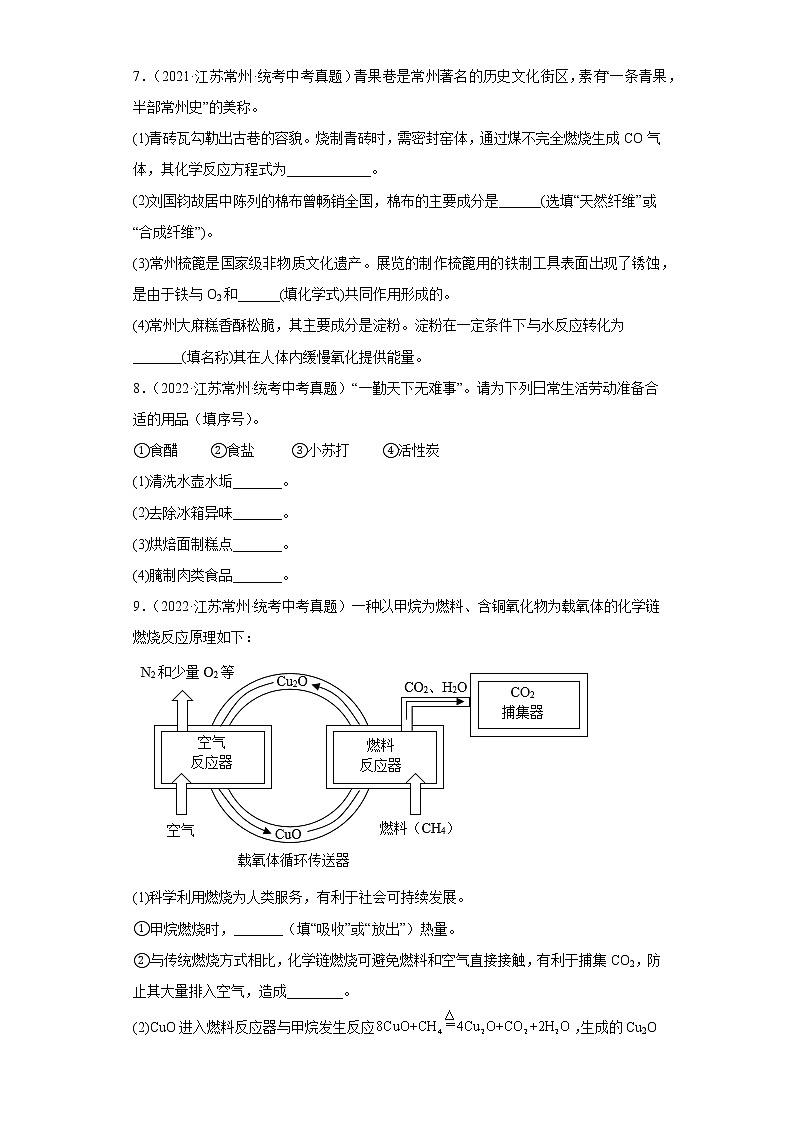
9.(2022·江苏常州·统考中考真题)一种以甲烷为燃料、含铜氧化物为载氧体的化学链燃烧反应原理如下:
(1)科学利用燃烧为人类服务,有利于社会可持续发展。
①甲烷燃烧时,_______(填“吸收”或“放出”)热量。
②与传统燃烧方式相比,化学链燃烧可避免燃料和空气直接接触,有利于捕集CO2,防止其大量排入空气,造成________。
(2)CuO进入燃料反应器与甲烷发生反应,生成的Cu2O再进入空气反应器,在一定温度下发生反应_____(填化学方程式),实现载氧体的循环再生。
(3)已知:空气中O2的体积分数约为21%。
从空气反应器排出的气体中O2体积分数随反应温度变化关系如图所示。
①在800~1100℃间,升高温度,排出的气体中N2体积分数______(填“增大”或“减小”)。
②空气反应器中最适宜的反应温度范围是______(填序号)
A.800-900℃ B.900-1000℃ C.1000-1030℃ D.1030-1100℃
三、实验题
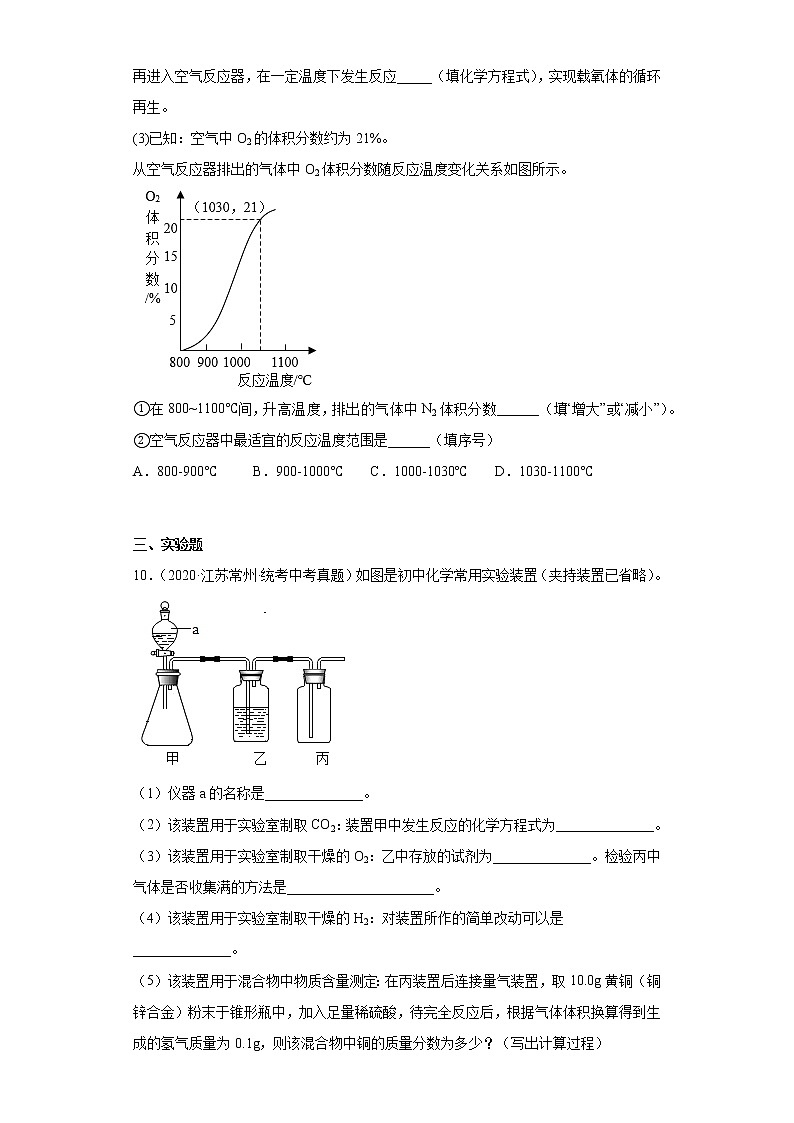
10.(2020·江苏常州·统考中考真题)如图是初中化学常用实验装置(夹持装置已省略)。
(1)仪器a的名称是______________。
(2)该装置用于实验室制取CO2:装置甲中发生反应的化学方程式为______________。
(3)该装置用于实验室制取干燥的O2:乙中存放的试剂为______________。检验丙中气体是否收集满的方法是_____________________。
(4)该装置用于实验室制取干燥的H2:对装置所作的简单改动可以是______________。
(5)该装置用于混合物中物质含量测定:在丙装置后连接量气装置,取10.0g黄铜(铜锌合金)粉末于锥形瓶中,加入足量稀硫酸,待完全反应后,根据气体体积换算得到生成的氢气质量为0.1g,则该混合物中铜的质量分数为多少?(写出计算过程)________________
11.(2020·江苏常州·统考中考真题)化学兴趣小组的同学模仿工业高炉炼铁原理,在如图所示装置中用CO还原CuO制取金属Cu。
(1)装置中气球的作用是______________。
(2)实验开始前,需要先通一段时间CO,然后开始加热,当观察到澄清石灰水______________的现象,说明CO与CuO已经发生反应。
(3)为确定反应的最佳温度,兴趣小组利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图所示(该图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同),据图回答下列问题:
①400℃时,反应的固体产物中含有Cu和______________。
②500℃时,该反应的化学方程式为_____________________。
③用CO还原CuO制取纯净的Cu,反应温度至少要控制在______________℃以上。
12.(2021·江苏常州·统考中考真题)兴趣小组同学模仿工业高炉炼铁原理,用图1实验装置(加热装置已省略)探究治炼铜的化学原理。实验操作过程如下:
①将CuO加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的CO2,此时用仪器测得CO2含量为ag/L,用气球密封试管口。
②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图1中虚线框部位,数据输出得到图11。恢复至与①相同的条件测得CO2含量为0.2ag/L。
④再次用酒精灯加热氧化铜部位,1分钟左右黑色固体变成紫红色。
(1)操作②中实验现象说明CO2___________(选填“能”或“不能”)与CuO反应。
(2)操作③中CO2含量减小的原因是__________。
(3)操作④中的化学反应方程式为_____________。
(4)实验结束后,一般将装置内的气体灼烧处理,目的是_________。
(5)由图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是_______。
四、综合应用题
13.(2021·江苏常州·统考中考真题)如图为体现CO2性质的趣味实验装置。
(1)仪器a的名称为_________。
(2)准备相同的两套装置,锥形瓶内均预先集满CO2。
①向其中一套锥形瓶内加入30mL水,搅一段时间后打开止水夹,观察到轻质塑料球向左移动一小段,移动原因是______,实验中b管的作用为:平衡气压有利于液体顺利滴下和______。
②向另一套装置的锥形瓶内加入30mL6%的NaOH溶液,搅排一段时间后打开止水夹,观察到轻质塑料球向左移动的距离比①中大得多,主要原因可用化学方程式表示为_______,随后,向锥形瓶内加入足量稀盐酸搅拌,可观察到轻质塑料球________(选填向左”、“向右”或“不”)移动。
(3)已知实验所用锥形瓶的容积为500mL,收集满一瓶二氧化碳(该实验条件下密度为2g/L)至少需要______克大理石(含CaCO3质量分数为80%)与足量盐酸反应?(写出计算过程)
五、科学探究题
14.(2021·江苏常州·统考中考真题)呼吸自救器是人在缺氧环境或出现高浓度有毒有害气体环境中使用的一种安全防护装置。如图是某化学氧自救器的示意图,其供氧装置由“初期生氧器”和“生氧罐”组成同学们对其工作原理进行了如下探究:
Ⅰ.探究“初期生氧器”
【查阅资料1】
①该化学氧自数器在工作初期,内部独立的“初期生氧器”首先启动,以解决初期供氧不足的问题。“初期生氧器”内有氯酸钾、二氧化锰、铁粉等成分。
②Fe3O4能与硫酸反应,其化学反应方程式为:Fe3O4+4H2SO4 =Fe2(SO4)3+FeSO4+4H2O
(1)“初期生氧器”主要依靠氯酸钾和二氧化锰制氧,其化学反应方程式为______________。
(2)小组成员为了解铁粉的作用展开了研究。
【实验探究1】
(3)“初期生氧器”中铁粉与氧气反应能__________,从而使氯酸钾的分解反应能持续进行。
Ⅱ.探究“生氧罐”
【查阅资料2】
①该化学氧自救器主体是由“生氧罐”供氧,内部装有颗粒状超氧化钾作为“制氧剂”,其反应原理为:4KO2+2H2O=4KOH+3O2↑;4KO2+2CO2=2K2CO3+3O2
②超氧化钾能与硫酸反应,其化学反应方程式为:4KO2+2H2SO4 =2K2SO4+3O2↑+2H2O
【实验探究2】
同学们对超氧化钾是否变质展开了研究,取出久置的“生氧罐”内颗粒状固体,称得样品质量为69.3g,进行如图所示实验,待实验结束测得C装置增重2.2g,E装置内固体变黑色且增重19.2g(实验前已排尽装置内空气,使用的药品均足量)
(1)反应开始后A装置中通入N2的目的是_________。
(2)E装置中发生反应的化学反应方程式为__________。
(3)超氧化钾________(选填“未”“部分”或“全部”)变质。
(4)生产该“生氧罐”时加入的超氧化钾的质量为________克。
序号
实验步骤
实验现象
实验结论
①
取“初生氧器”充分反应后的物质于纸上,将磁铁靠近并接触粉末
有黑色物质被磁铁吸引
被吸引物质可能是Fe、Fe3O4或两者都有
②
取①中被铁吸引的物质于试管中,向其中加入足量稀硫酸
固体完全溶解,得到澄清的黄色溶液
被吸引物质中一定含有__________(填化学式)
参考答案:
1.D
【详解】因为大气中的二氧化碳像温室的玻璃或塑料薄膜一样,既能让太阳光透过,又能使地面吸收的太阳光的热量不易向外散失,起到了对地球保温的作用,所以二氧化碳排放过多,会造成温室效应。氧气、氮气、稀有气体不会造成温室效应。故选D。
2.D
【详解】A、氧气密度大于空气,不能使用向下排空气法收集,故选项错误;
B、氮气密度接近空气,不能使用排空气法收集,故选项错误;
C、二氧化碳能溶于水,不能使用排水法收集,故选项错误;
D、氢气密度小于空气,可以使用向下排空气法收集,且氢气难溶于水,可以使用排水法收集,故选项正确。
故选D。
3.B
【详解】A、金属丝导电没有生成新物质,属于物理变化;
B、盐酸除铁锈,两者反应生成氯化铁和水,有新物质生成,属于化学变化;
C、活性炭除臭是利用了活性炭的吸附性,没有生成新物质,属于物理变化;
D、木材制桌椅只是物质形状的变化,没有生成新物质,属于物理变化。
故选B。
4.D
【详解】A、干冰是固态二氧化碳,由二氧化碳分子构成,故A错误;
B、微粒不断运动,构成干冰的微粒也在不断运动,不是静止不动的,故B错误;
C、构成干冰的二氧化碳分子之间有间隙,故C错误;
D、干冰升华吸热使环境温度降低,可用于冷冻与运输食品或药品,故D正确。
故选D。
5.B
【详解】某阻燃剂主要成分为碱式碳酸镁【Mga(OH)2(CO3)b】,遇热分解生成三种氧化物(氧化镁和水和二氧化碳气体),将产生的气体依次通过浓硫酸(吸收水分)和过量澄清石灰水(吸收二氧化碳气体),浓硫酸增重0.18g即为生成水的质量,澄清石灰水中生成4g白色沉淀(为二氧化碳与氢氧化钙反应生成碳酸钙的质量)。
根据质量守恒定律,化学反应前后元素的种类和质量不变,
由于生成水中氢元素质量全部来自样品中氢氧根,根据氢元素守恒,设氢氧根的质量为x,则有,,解得;
由于生成碳酸钙沉淀中碳元素质量全部来自样品中碳酸根,根据碳元素守恒,设碳酸根的质量为y,则有,,解得,则在碱式碳酸镁中,解得b=4;
根据化合物中正负化合价代数和为0的原则,即为,所以a=5。
故选B。
6.(1)②
(2)④
(3)①
(4)③
【分析】(1)
金刚石的硬度大,可用于切割玻璃,故选②;
(2)
明矾溶于水可吸附水中悬浮的杂质,形成沉淀,故选④;
(3)
干冰升华吸收大量的热,可用于人工降雨,故选①;
(4)
聚乙烯是最常见的塑料,常用于包装,故选③。
7.(1)2C+O22CO
(2)天然纤维
(3)H2O
(4)葡萄糖
【分析】(1)
煤不完全燃烧生成CO气体的化学方程式是2C+O22CO。
(2)
棉布的主要成分是天然纤维。
(3)
铁生锈是铁与氧气,水(化学式H2O)共同作用形成的。
(4)
葡萄糖是人体主要的供能物质,淀粉在一定条件下与水反应转化为葡萄糖在人体内缓慢氧化提供能量。
8.(1)①
(2)④
(3)③
(4)②
【详解】(1)水垢的主要成分是碳酸盐钙,食醋中含有醋酸,碳酸钙与醋酸反应生成可溶性醋酸钙、水和二氧化碳,所以可用食醋清洗水壶水垢,故选①;
(2)活性炭具有吸附性,能够吸附色素和异味,可用来去除冰箱异味,故选④;
(3)小苏打是碳酸氢钠,能与发酵产生的酸反应生成二氧化碳,受热分解也会生成二氧化碳气体,可以使糕点疏松多孔,所以小苏打可以用来烘焙面制糕点,故选③;
(4)食盐的主要成分是氯化钠,氯化钠无毒,具有咸味,可用来腌制肉类食品,故选②。
9.(1) 放出 温室效应
(2)
(3) 减小 A
【详解】(1)①甲烷燃烧属于氧化反应,氧化反应都是放热反应,燃烧时放出热量;
②大量的二氧化碳排放到空气中会引起温室效应;
(2)根据图中信息可知,Cu2O再进入空气反应器,在一定温度下与氧气反应生成CuO,化学方程式为:,故应填:;
(3)①根据图中信息,随着温度升高,氧气的体积分数变大,所以氮气的体积分数减小;
②由图可知,随着反应温度升高,从空气反应器排出的气体中O2体积分数逐渐增大,故空气反应器中最适宜的反应温度范围是800-900℃,此时排出的氧气最少,说明此时反应速率最快。
故选A。
10. 分液漏斗 CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸 将带火星的木条放在丙装置右侧导管口,若木条复燃,则集满 将原来乙装置短导管与丙装置长导管相连的胶皮管拆开,改成用胶皮管将乙装置的短导管与丙装置的短导管相连 67.5%(详见解析)
【详解】(1)根据图示,仪器a的名称是:分液漏斗。
(2)装置甲适用于固液反应,不需要加热制取气体,实验室常用大理石(或石灰石)和稀盐酸反应制取CO2,符合该装置要求。大理石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,故装置甲中发生反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑。
(3)该装置如果用于实验室制取氧气,则是利用过氧化氢溶液在二氧化锰催化作用下分解生成氧气,装置甲排出的气体中含有水蒸气。根据装置乙的特点,乙中的干燥剂必须是液态,浓硫酸常温下是液态,且氧气不跟浓硫酸反应,因此制取干燥的O2,乙中存放的试剂为:浓硫酸。因为氧气能使带火星的木条复燃,故检验丙中氧气是否收集满的方法是:将带火星的木条放在丙装置右侧导管口,若木条复燃,则集满。
(4)因为实验室常用锌和稀硫酸在常温下反应制取氢气,氢气也不跟浓硫酸反应,所以装置甲和装置乙不需要改动。又因为氢气的密度比空气小,所以用装置丙收集氢气必须是“短进(氢气)长出(空气)”,因此该装置用于实验室制取干燥的H2,对装置所作的简单改动是:将原来乙装置短导管与丙装置长导管相连的胶皮管拆开,改成用胶皮管将乙装置的短导管与丙装置的短导管相连。
(5)设:该混合物中锌的质量为x。
解得x=3.25g
该混合物中铜的质量分数为:
答:该混合物中铜的质量分数为67.5%。
【点睛】因为锌能和稀硫酸反应,而铜不能和稀硫酸反应,所以根据10.0g黄铜(铜锌合金)粉末中的锌跟足量的稀硫酸完全反应后,生成的氢气质量为0.1g,可以计算出混合物中锌的质量,然后计算出铜的质量,最后得出混合物中铜的质量分数。
11. 收集尾气,防止污染环境 变浑浊 500
【详解】(1)尾气中含有有毒的一氧化碳,装置中气球的作用是收集尾气,防止污染环境。
(2)实验开始前,需要先通一段时间CO,然后开始加热,当观察到澄清石灰水变浑浊的现象,说明CO与CuO已经发生反应,因为加热条件下一氧化碳与氧化铜反应会生成二氧化碳,二氧化碳使澄清石灰水变浑浊。
(3)①根据图示,400℃时,反应的固体产物中含有Cu和。
②根据图示,500℃时,固体产物中只含有Cu,则一氧化碳与氧化铜在加热条件下反应生成铜和二氧化碳,该反应的化学方程式为。
③根据图示,500℃以上时,固体产物只有铜,故用CO还原CuO制取纯净的Cu,反应温度至少要控制在500℃以上。
12.(1)不能
(2)二氧化碳与焦炭发生反应
(3)
(4)防止一氧化碳污染环境
(5)焦炭和二氧化碳的反应为吸热反应
【详解】(1)②用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,故操作②中实验现象说明CO2不能与CuO反应。
(2)操作③中CO2含量减小的原因是二氧化碳与焦炭发生反应生成一氧化碳。
(3)操作④中的化学反应为一氧化碳和氧化铜加热生成铜和二氧化碳,化学方程式为:。
(4)实验结束后,装置中可能存在一氧化碳,一氧化碳有剧毒,故一般将装置内的气体灼烧处理,目的是防止一氧化碳污染环境。
(5)图2可知,刚停止加热后焦炭区温度降低更快,可能的原因是焦炭和二氧化碳高温生成一氧化碳的反应为吸热反应。
13.(1)铁架台
(2) 二氧化碳溶于水(或与水反应)使气压减小 防止加入液体的体积导致锥形瓶内气体压强变化 向右
(3)解:设需要大理石的质量为x
x=2.84g
答:需要大理石的质量为2.84g。
【分析】(1)
仪器a的名称为铁架台。
(2)
①二氧化碳溶于水(或与水反应)使装置中气体减少,压强减小,导致轻质塑料球向左移动一小段;实验中b管使锥形瓶和分液漏斗形成一个连通器样的装置,其作用为:平衡气压有利于液体顺利滴下和防止加入液体的体积导致锥形瓶内气体压强变化。
②向另一套装置的锥形瓶内加入30mL6%的NaOH溶液,氢氧化钠和二氧化碳反应生成碳酸钠和水:,导致装置中气体减小更多,压强减小更大,故一段时间后打开止水夹,观察到轻质塑料球向左移动的距离比①中大得多;向锥形瓶内加入足量稀盐酸搅拌,稀盐酸和碳酸钠生成二氧化碳气体,装置中气体增多,压强变大,可观察到轻质型料球向右移动。
(3)
见答案。
14. 2KClO32KCl+3O2↑ Fe3O4 放出大量的热 将产生的CO2和O2排入后续的反应装置中参与反应 2Cu+O22CuO 部分 71
【详解】Ⅰ.探究“初期生氧器”:
(1)氯酸钾和二氧化锰制氧的化学方程式是2KClO32KCl+3O2↑。
(2)加入足量稀硫酸得到澄清的黄色溶液,说明反应后溶液中有Fe3+,所以被吸引物质中一定含有Fe3O4。
(3)因为氯酸钾的分解反应需要吸热,所以铁粉与氧气反应能放出大量的热才能维持氯酸钾的分解反应持续进行。
Ⅱ.探究“生氧罐”:
(1)反应开始后A装置中通入N2的目的是将产生的CO2和O2排入后续的反应装置中参与反应,使实验测量结果更准确。
(2)铜在加热条件下可以和氧气发生反应生成氧化铜,所以E装置中发生反应的化学反应方程式为2Cu+O22CuO。
(3)因为C装置增重2.2g说明有二氧化碳生成。所取样品中含有碳酸钾。E装置内固体变黑色且增重19.2g说明有超氧化钾发生反应生成氧气,所以超氧化钾部分变质。
(4)E装置内固体变黑色且增重19.2g,说明生产氧气19.2g根据4KO2+2H2SO4 =2K2SO4+3O2↑+2H2O,设参与该反应的KO2的质量为x,KO2与生成的氧气的质量关系为
C装置增重2.2g,说明有2.2g二氧化碳生成。根据4KO2+2CO2=2K2CO3+3O2,K2CO3+H2SO4=K2SO4+H2O+CO2↑,设变质的KO2的质量为y, K2CO3的质量为z。 KO2与生成的K2CO3,CO2的关系为
样品质量为69.3g中有氢氧化钾的质量为69.3g-56.8g-6.9g=5.6g。根据4KO2+2H2O=4KOH+3O2↑,设参与此反应的KO2的质量为m,KO2与KOH的关系为
所以生产该“生氧罐”时加入的超氧化钾的质量为56.8g+7.1g+7.1g=71g。
江苏苏州市2020-2022三年中考化学真题知识点分类汇编-04碳和碳的氧化物: 这是一份江苏苏州市2020-2022三年中考化学真题知识点分类汇编-04碳和碳的氧化物,共15页。试卷主要包含了单选题,填空题,流程题,实验题,科学探究题等内容,欢迎下载使用。
江苏省扬州市2020-2022三年中考化学真题知识点分类汇编-04碳和碳的氧化物: 这是一份江苏省扬州市2020-2022三年中考化学真题知识点分类汇编-04碳和碳的氧化物,共11页。试卷主要包含了单选题,多选题,填空题,实验题等内容,欢迎下载使用。
江苏省泰州市2020-2022三年中考化学真题知识点分类汇编-04碳和碳的氧化物: 这是一份江苏省泰州市2020-2022三年中考化学真题知识点分类汇编-04碳和碳的氧化物,共8页。试卷主要包含了单选题,填空题,推断题,实验题等内容,欢迎下载使用。












