

2023年高考第一次模拟考试卷:全国甲卷理综A卷(考试版)版
展开2023年高考第一次模拟考试卷(全国甲卷理综A卷)
高三理科综合
本卷满分300分,考试时间150分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 P 31 S 32 Fe 56 Co 59
一、选择题:本题共13小题,每小题6分,共78分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.膳食纤维一般是指不能被人类胃肠道消化吸收的食物成分,主要来自植物细胞壁,包含纤维素等,曾被认为是一种“无营养物质”而长期得不到足够的重视。通过一系列调查研究,人们发现膳食纤维与人体健康密切相关,现被认定为第七类营养素。下列有关纤维素的叙述,正确的是( )
A.纤维素、肝糖原分别是植物多糖、动物多糖,故彻底水解产物有差异
B.细菌、真菌等细胞壁的主要成分及功能都与植物细胞壁的相同
C.草食类动物的胃肠道能分泌分解纤维素的一系列消化酶
D.某些草食类动物能分解食物中的纤维素,并能吸收和利用分解产物合成糖原
2.超氧化物歧化酶(SOD)是生物体内一类重要的抗氧化酶,能够特异性清除自由基O2-,由2条或4条肽链组成,其活性中心含有铜、锌、锰、铁等金属离子中的一种或两种,可作为药用酶供患者使用。下列相关叙述错误的是( )
A.金属离子的存在可能直接影响SOD的活性
B.将SOD用作药用酶时,患者可以口服或注射
C.自由基O2-攻击蛋白质后,会使蛋白质活性下降,导致细胞衰老
D.通过胞吞方式进入细胞的药用SOD,能减缓细胞衰老
3.apoB-100蛋白由肝细胞和肾细胞分泌,apoB-48蛋白由小肠细胞分泌,它们都是负责脂质转运的载脂蛋白,包含apoB-100的脂蛋白会变成导致动脉粥样硬化的低密度脂蛋白,而包含apoB-48的脂蛋白不会。apoB-100蛋白和apoB-48蛋白都是apoB基因的表达产物(如图)。下列相关叙述错误的是( )
A.apoB-48蛋白的相对分子质量小于apoB-100蛋白的
B.apoB-48蛋白的编辑前mRNA长度与apoB-100蛋白的相等
C.apoB基因的转录和翻译过程中共有的碱基配对方式是A与U配对,G与C配对
D.与肝细胞相比,小肠细胞中apoB基因突变导致mRNA上的终止密码子提前出现
4.朱鹮是濒临灭绝的鸟类,当前我国的野生朱鹮主要散布在陕西洋县、浙江德清、河南董寨等地。游客在旅游时观察到游隼击杀朱鹮的场面,专家认为这是自然界的常态,人类不能过分干预。下列相关叙述正确的是( )
A.为了逃避游隼的击杀,朱鹮易于生出快速飞翔和警觉性强的后代
B.游隼的击杀会改变朱鹮的基因频率,人类的干预不会改变朱鹮的基因频率
C.陕西洋县、浙江德清、河南董寨三个地方的朱鹮种群基因库是不同的
D.陕西洋县、浙江德清、河南董寨的朱鹮之间若存在地理隔离,则必然存在生殖隔离
5.如图表示不同浓度的生长素(IAA)对植物某器官的作用结果。图中虚线表示IAA浓度为0时,单位生长长度所需的时间,下列叙述正确的是( )
A.植物横放时,茎的近地侧生长素浓度可能会由c对应的浓度变为d对应的浓度
B.植物横放时,根的近地侧生长素浓度可能会由a对应的浓度变为b对应的浓度
C.对茎的作用效果为b的生长素浓度对根的作用效果可能为d
D.具有顶端优势的植物,顶芽和侧芽生长素浓度可能分别为a和b对应的浓度
6.某同学分别在住宅和农田区域设置鼠笼捕获布氏田鼠,调查布氏田鼠的种群数量变化。以捕获数÷置笼数×100%计算捕获率,结果如图所示。下列相关叙述错误的是( )
A.成年的布氏田鼠可能在冬末春初集体进入繁殖期
B.根据实验获取的数据可直接计算布氏田鼠的种群密度
C.住宅区布氏田鼠种群的K值降低可能与住宅区环境卫生提高有关
D.年龄组成和性别比例不能直接决定布氏田鼠种群数量的变化
7.化学与环境,材料、信息、能源关系密切。下列说法正确的是
A.“地沟油”属于有机化合物
B.光导纤维的主要材料属于酸性氧化物
C.航母拦阻索的主要材料特种钢属于非金属材料
D.人类活动产生的大量会导致酸雨的发生
8.某有机化合物X的结构如图所示。下列说法正确的是( )
A. X存在芳香族同分异构体 B. X分子中有3种官能团
C. 1mol X最多能与4mol NaOH反应 D. X不能与溴水反应
9.设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.5.5 g P4O6()中含P—O键的数目为0.3NA
B.1 L 0.1 mol·L-1 Ca(ClO)2溶液中含ClO-的数目为0.2NA
C.0.2 mol乙酸与0.1 mol乙醇在浓硫酸催化下充分反应,生成的乙酸乙酯分子数为0.1NA
D.22.4 L NH3发生反应4NH3+3F2 NF3+3NH4F,转移的电子数为1.5NA
10.下列物质性质实验对应的离子方程式书写正确的是
A.钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+
B.用碳酸钠溶液处理水垢中的硫酸钙:CO+Ca2+=CaCO3↓
C.硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-=AlO+2H2O
D.酸性KMnO4溶液中滴加H2O2溶液:2MnO+5H2O2+6H+=2Mn2++5O2↑+8H2O
11.短周期主族元素W、X、Y、Z、Q的原子序数依次增大。X、Y、Z同周期,且相邻,Y的原子序数与Q的最外层电子数相同,WQ的水溶液为强酸,五种元素可形成有机化合物M,其结构简式如图(W未表示出来)。下列说法错误的是
A.简单氢化物的沸点:Z>Y>Q>X
B.最高价含氧酸的酸性:Q>Y>X
C.简单离子的半径:Q
12.铝的冶炼在工业上通常采用电解Al2O3的方法,装置示意图如图。研究表明,电解AlCl3-NaCl熔融盐也可得到Al,熔融盐中铝元素主要存在形式为AlCl和Al2Cl。下列说法不正确的是
A.电解Al2O3装置中B电极为阴极,发生还原反应
B.电解Al2O3过程中碳素电极虽为惰性电极,但生产中会有损耗,需定期更换
C.电解AlCl3-NaCl时阴极反应式可表示为4Al2Cl+3e—=Al+7AlCl
D.电解AlCl3-NaCl时AlCl从阳极流向阴极
13.由下列实验操作及现象能得出相应结论的是
实验操作
实验现象
实验结论
A
向盛有浓HNO3溶液的两支试管中分别加入除去氧化膜的镁带和铝片
加入镁带的试管中迅速产生红棕色气体。加入铝片试管中无明显现象
金属活泼性:
Mg>Al
B
向某溶液中先滴加少量KSCN溶液后,再加入足量H2O2溶液
始终无明显现象
原溶液中不含有Fe2+
C
将苯、液溴、铁粉混合物反应产生的气体通入到AgNO3溶液中
生成淡黄色沉淀
证明苯与液溴在Fe 催化下发生取代反应
D
一块除去铁锈的铁片上滴一滴铁氰化钾溶液,静置2~3min
生成蓝色沉淀
铁片上可能发生了电化学腐蚀
二、选择题:本题共8小题,每小题6分,共48分。在每小题给出的四个选项中,第14~18题只有一项符合题目要求,第19~21题有多项符合题目要求。全部选对的得6分,选对但不全的得3分,有选错的得0分。
14.北京时间2022年10月7日21时10分,中国太原卫星发射中心在黄海海域使用长征十一号海射运载火箭,采用“一箭双星”方式,成功将微厘空间北斗低轨导航增强系统S5/S6试验卫星发射升空,卫星顺利进入预定轨道,发射任务获得圆满成功。若试验卫星绕地球做匀速圆周运动,周期为T,离地高度为h,已知地球半径为R,万有引力常量为G,则( )
A.试验船的运行速度为 B.地球的第一宇宙速度为
C.地球的质量为 D.地球表面的重力加速度为
15.如图所示,质量为,倾角的粗糙斜面置于水平面上,质量为的物块在水平向右的推力作用下,沿斜面向上匀速运动,物块上滑过程中斜面体始终静止。下列结论正确的是( )
A.物块一定不受摩擦力作用
B.由于不知道的大小,所以物块可能受到沿斜面向上的摩擦力
C.水平面对斜面体的摩擦力大小为
D.水平面对斜面体的支持力大小为
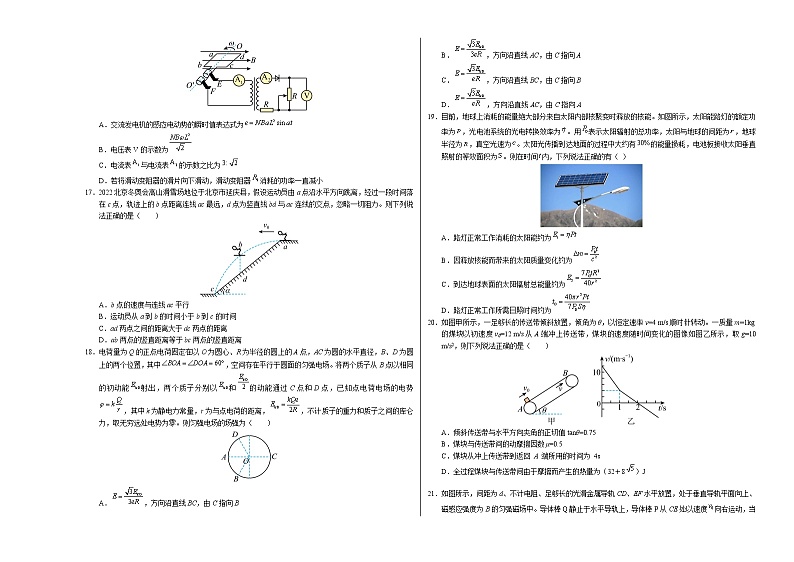
16.如图所示,某交流发电机内有一边长为、匝数为、电阻不计的正方形线圈,在磁感应强度大小为的匀强磁场中绕转轴以角速度匀速转动,轴垂直于磁感线。它与理想变压器的原线圈连接,变压器原、副线圈的匝数之比为,二极管的正向电阻为零,反向电阻无穷大,定值电阻的阻值为,滑动变阻器的接入电路的阻值为且最大阻值与定值电阻的阻值相等,滑片置于滑动变阻器的中间,电表均为理想电表。从正方形线圈转到图示位置开始计时,下列判断正确的是( )
A.交流发电机的感应电动势的瞬时值表达式为
B.电压表V的示数为
C.电流表与电流表的示数之比为
D.若将滑动变阻器的滑片向下滑动,滑动变阻器消耗的功率一直减小
17.2022北京冬奥会高山滑雪场地位于北京市延庆县,假设运动员由a点沿水平方向跳离,经过一段时间落在c点,轨迹上的b点距离连线ac最远,d点为竖直线bd与ac连线的交点,忽略一切阻力。则下列说法正确的是( )
A.b点的速度与连线ac平行
B.运动员从a到b的时间小于b到c的时间
C.ad两点之间的距离大于dc两点的距离
D.ab两点的竖直距离等于bc两点的竖直距离
18.电荷量为Q的正点电荷固定在以O为圆心、R为半径的圆上的A点,AC为圆的水平直径,B、D为圆上的两个位置,其中,空间存在平行于圆面的匀强电场。将两个质子从B点以相同的初动能射出,两个质子分别以和的动能通过C点和D点,已知点电荷电场的电势,其中k为静电力常量,r为与点电荷的距离,,不计质子的重力和质子之间的库仑力,取无穷远处电势为零。则匀强电场的场强为( )
A.,方向沿直线BC,由C指向B
B.,方向沿直线AC,由C指向A
C.,方向沿直线BC,由C指向B
D.,方向沿直线AC,由C指向A
19.目前,地球上消耗的能量绝大部分来自太阳内部核聚变时释放的核能。如图所示,太阳能路灯的额定功率为,光电池系统的光电转换效率为。用表示太阳辐射的总功率,太阳与地球的间距为,地球半径为,真空光速为。太阳光传播到达地面的过程中大约有的能量损耗,电池板接收太阳垂直照射的等效面积为。则在时间内,下列说法正确的有( )
A.路灯正常工作消耗的太阳能约为
B.因释放核能而带来的太阳质量变化约为
C.到达地球表面的太阳辐射总能量约为
D.路灯正常工作所需日照时间约为
20.如图甲所示,一足够长的传送带倾斜放置,倾角为θ,以恒定速率v=4 m/s顺时针转动。一质量m=1kg的煤块以初速度v0=12 m/s从A端冲上传送带,煤块的速度随时间变化的图像如图乙所示,取g=10 m/s2,则下列说法正确的是( )
A.倾斜传送带与水平方向夹角的正切值tanθ=0.75
B.煤块与传送带间的动摩擦因数μ=0.5
C.煤块从冲上传送带到返回 A 端所用的时间为 4s
D.全过程煤块与传送带间由于摩擦而产生的热量为(32+8)J
21.如图所示,间距为d、不计电阻、足够长的光滑金属导轨CD、EF水平放置,处于垂直导轨平面向上、磁感应强度为B的匀强磁场中。导体棒Q静止于水平导轨上,导体棒P从CE处以速度向右运动,当导体棒Q在水平轨道上速度最大时,另一与导体棒P相同的导体棒以速度滑上导轨CE处,以后每当Q速度达到最大时,均重复前面操作。已知导体棒的长度均为d、质量均为m、电阻均为R,导体棒运动过程中始终与导轨接触良好且与导轨垂直,重力加速度为g,下列说法正确的是( )
A.导体棒P的最小速度为
B.导体棒P的速度为(第三根棒未放)时,导体棒P的加速度大小为
C.不论有几个导体棒在导轨上运动,几个导体棒组成的系统动量均守恒
D.导体棒Q从静止开始运动经足够长时间后,流过导体棒Q的电量为
三、非选择题:共174分,第22~32题为必考题,每个试题考生都必须作答。第33~38题为选考题,考生根据要求作答。
(一)必考题:共129分。
22. (6分)某研究性学习小组,将毫安表的表盘改装成可直接读取重力数值的表盘,电路图如图甲所示。
实验器材如下:
电源E(电动势1.5V,内阻为)
灵敏毫安表mA(满偏电流1mA,内阻为)
电阻箱R(最大阻值为)
拉力敏感电阻丝
开关S,导线若干
已知拉力敏感电阻丝的阻值随拉力F变化的规律如图乙所示。
(1)未悬挂重物时,调节电阻箱,使灵敏毫安表满偏,此时电阻箱R的阻值为_________,改装后的表盘重力“0”刻度位于表盘的______(填“左”或“右”)端。
(2)若毫安表指针指向表盘正中间刻度,此时拉力敏感电阻丝的阻值为_________。
(3)若拉力敏感电阻丝的阻值为,电阻丝与竖直方向的夹角(),则通过毫安表的电流为_________mA,此处若标注重物的重力,该数值为_________。
23. (9分)某同学用气垫导轨装置验证动量守恒定律,如图所示。其中G1、G2为两个光电门,它们与数字计时器相连。两个滑块A、B(包含挡光片)质量分别为m1、m2,当它们通过光电门时,计时器可测得挡光片被遮挡的时间。
(1)先调节气垫导轨水平,经过调整后,轻推一下B,若它通过光电门G1、G2的时间它都能________,或将其轻放在气垫导轨上任何位置都能静止,则气垫导轨已调至水平。
(2)将B静置于两光电门之间,将A置于光电门G1右侧,用手轻推一下A,使其向左运动,与B发生碰撞,为了使A碰后不返回,则m1________m2。(填“>”、“=”或“<”);
(3)光电门G1记录的挡光时间为Δt1,滑块B、A先后通过光电门时,G2记录的挡光时间分别为Δt2、Δt3,为了减小误差,挡光片的宽度应选择___________(填“窄”或者“宽”)的,若m1、m2、Δt1、Δt2、Δt3满足________(写出关系式)则可验证动量守恒定律;若Δt1、Δt2、Δt3满足一个关系式_________,则说明A、B发生的是弹性碰撞。
24.(14分)如图甲所示,质量为m=0.5kg的小物块静止在倾角为37°的足够长固定斜面的底端,现对其施一沿斜面向上的力F,力随时间变化的情况如图乙所示,5s后撤去力F。已知sin37°=0.6,cos37°=0.8,物块与斜面间的动摩擦因数μ=0.5,不计空气阻力,g取10m/s2。求:
(1)力F作用下小物块的加速度大小;
(2)小物块沿斜面向上运动的最大距离;
(3)小物块在斜面运动的总时间。(结果可保留根号)
25.(18分)如图甲所示,在xOy平面的第一象限内存在周期性变化的磁场,规定磁场垂直纸面向内的方向为正,磁感应强度B随时间t的变化规律如图乙所示。质量为m、电荷量为+q的粒子,在t=0时刻沿x轴正方向从坐标原点O射入磁场。图乙中T0为未知量,不计粒子的重力(sin37°=0.6,cos37°=0.8)。
(1)若粒子射入磁场时的速度为v0,求时间内粒子做匀速圆周运动的半径;
(2)若粒子恰好不能从Oy轴射出磁场,求磁感应强度变化的周期;
(3)若使粒子能从坐标为(d,d)的D点平行于Ox轴射出,求射入磁场时速度大小。
26.(14分)苯胺()是一种无色油状液体,加热至370℃会分解,微溶于水,易溶于有机溶剂,能被二氧化锰氧化成对苯醌()。一种用苯胺还原软锰矿(主要成分是MnO2,含SiO2、Fe2O3、Al2O3等杂质)制备MnSO4·H2O的工艺流程如图。
溶液中金属离子开始沉淀和完全沉淀时的pH如下表所示:
金属离子
Mn2+
Fe2+
Fe3+
Al3+
开始沉淀时(c=0.01mol/L)的pH
8.1
7.5
2.2
3.7
完全沉淀时(c=1×10-5mol/L)的pH
9.6
9.0
3.2
4.7
回答下列问题:
(1)还原酸浸前将软锰矿粉碎的目的是_______________________________________,为达到该目的在加入苯胺和稀硫酸后常采取的操作为 。
(2)沉淀1的主要成分为___________(填化学式),写出还原酸浸时主要发生反应的化学方程式:_______________________________________________________。
(3)根据上表数据,Ksp[Mn(OH)2]、Ksp[Fe(OH)3]、Ksp[Al(OH)3]由大到小的顺序为______________。调pH步骤中应控制的pH范围是________________。
(4)MnSO4溶液结晶温度越低,MnSO4所带结晶水就越多,在9℃时,可结晶出MnSO4·7H2O,在26℃时,可结晶出MnSO4·4H2O,在100℃左右时,可结晶出MnSO4·H2O,则从操作A所得的溶液中获得MnSO4·H2O晶体需要进行的操作是___________________________________、洗涤、干燥。从制取的产品中,称取一定质量的MnSO4·H2O样品用BaCl2标准溶液滴定(操作过程产生的误差很小,可忽略),计算所得样品的质量分数大于100%,可能的原因是___________________________________。
27.(14分)过二硫酸钠(,其中S的化合价为)是白色品状粉末,易溶于水,加热至较高温度时发生分解,常用作漂白剂、金属表面处理剂等。某化学小组在实验室对过二硫酸钠的制备和成品含量测定进行探究。已知:。
回答下列问题:
(1) 中含有的过氧键(键)数目为_______。
(2)①在下,以过二硫酸铵溶液和溶液为原料采用“复分解法”制备过二硫酸钠,装置如图所示(部分夹持仪器已略去)。
有关反应的化学方程式为_______,装置A的适宜加热方式为_______。
②装置B的作用是_______,反应过程中需要持续通入的主要原因是_______。
(3)由过二硫酸钠溶液经过减压蒸发浓缩、冷却结品、干燥等操作即可得到过二硫酸纳晶体,采用“减压蒸发浓缩”的原因是_______。
(4)过二硫酸钠成品的含量可用“碘量法”测得。称取试样,置于碘量瓶中,移取足量的溶液于其中,并加入少量乙酸溶液,密闭,在暗处放置,生成的用硫代硫酸钠标准溶液滴定,有关反应为。达到滴定终点时平均消耗标准溶液的体积为,则滴定中选用的指示剂为_______,成品中过二硫酸钠的含量为_______(用含m、V的代数式表示,需化简)。
28.(15分)含氯化合物的反应在化学工业中具有重要的地位。回答下列问题:
(1)次氯酸钠氧化法可以制备Na2FeO4。
已知:2H2(g) +O2(g)=2H2O(l) ΔH=a kJ·mol-1
NaCl(aq)+H2O(l)=NaClO(aq)+ H2(g) ΔH =b kJ·mol-1
4Na2FeO4 (aq) + 10H2O(l)=4Fe(OH)3(s) +3O2 (g)+8NaOH(aq) ΔH=c kJ·mol-1
反应2Fe(OH)3(s)+3NaClO(aq)+4NaOH(aq)=2Na2FeO4(aq)+3NaCl(aq)+5H2O(l)的ΔH=_____kJ·mol-1。
(2)光气(COCl2)是重要的含氯化合物。常用于医药、农药制造,工业上利用一氧化碳和氯气反应制备,反应方程式为CO(g)+Cl2(g) COCl2(g)。在1 L恒温恒容密闭容器 中充入2.5molCO和1.5molCl2,在催化剂作用下发生反应,测得CO及COCl2的物质的量随时间变化如图1所示:
①0~15s内,Cl2的平均反应速率为_______mol· L-1·min-1。
②第一次平衡时,CO的平衡转化率为_______;此温度下,该反应的平衡常数KC=_______(保留两位有效数字)。
③在第20 s时,改变的条件是_______。
(3)工业上常用氯苯(C6H5—Cl)和硫化氢(H2S)反应来制备一种用途广泛的有机合成中间体苯硫酚
(C6H5—SH),但会有副产物苯(C6 H6)生成。
Ⅰ.C6H5—Cl(g)+H2S(gC6H5-SH(g)+HCl(g) ΔH1= -16.8 kJ·mol-1;
Ⅱ.C6H5—Cl(g)+H2S(g)=C6H6(g)+HCl(g)+S8(g) ΔH2= - 45.8 kJ·mol-1。
①将一定量的C6H5—Cl和H2S的混合气体充入恒容的密闭容器中,控制反应温度为T(假设只发生反应Ⅰ),下列可以作为反应Ⅰ达到平衡的判据是_______(填字母)。
A.气体的压强不变 B.平衡常数不变
C.v正(H2S)= v逆(HCl) D.容器内气体密度不变
②现将一定量的C6H5—Cl和H2S置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20 min测定生成物的浓度,得到图2和图3。
(R为H2S与C6H6—Cl的起始物质的量之比),图2显示温度较低时C6H5—SH浓度的增加程度大于C6H6,从活化能角度分析其主要原因是_______;结合图2和图3,该模拟工业生产制备C6H5—SH的适宜条件为_______。
29.害虫防治是生态农业的一项重要课题,害虫的趋光特性有季节性的节律变化。为探明几种常见农业害虫的趋光行为间的差异,为灯光诱捕器类产品研发改进提供理论依据,研究人员通过室内比较研究在不同光照强度的荧光灯刺激下,几种常见农业害虫的趋光行为,实验结果如图所示。回答下列问题:
(1)间接影响某害虫种群密度的数量特征有________________。某些害虫迁入农田的初期,其种群数量在较短一段时间内呈现近似“J”形增长,原因是______________。
(2)害虫用于生长、发育和繁殖的能量不会全部流入其天敌,原因是其中的一部分能量________,一部分能量暂时未被利用。从能量流动的角度分析,农田害虫防治的意义在于_________________________。
(3)根据调查结果可知,被调查的几种害虫中__________最不适合用灯光进行诱捕。利用灯光诱捕害虫时,需要考虑光照强度、____________________等因素。
30.已知玉米属于C4植物、水稻属于C3植物,在高光强高温和干旱条件下C4植物比C3植物具有更高的光合效率。研究发现C4植物的光合作用先后发生在叶肉细胞和维管束鞘细胞。已知其维管束鞘细胞中的叶绿体几乎无基粒,叶肉细胞中的叶绿体有发达的基粒。C4植物细胞中的PEP羧化酶和RuBP羧化酶均是催化CO2固定的酶,且PEP羧化酶对CO2的亲和性远高于RuBP羧化酶。C3植物和C4物的光反应阶段完全相同,但CO2固定的场所和方式不同。如图表示C4物暗反应的过程及场所,回答下列问题:
(1)C3物和C4物光反应分别发生在________(分别填细胞名称),该阶段主要的物质变化为________。
(2)CO2被玉米吸收后,可被________物质固定,而水稻吸收的CO2接参与卡尔文循环,据此分析,在高光强、高温和干旱条件下玉米的光合效率高于水稻的原因是___________。若将玉米和水稻放在同一密闭容器中培养,给予适宜的温度和光照条件,存活时间较长的是______。
(3)为了提高粮食产量,农业生产上常选择其他农作物与玉米进行分行种植(间作),适合与玉米进行间作的植物应具备的特点是__________(至少写2点),间作能提高粮食产量与其可充分利用____________(答两点)有关。
31.钾在动植物食品中含量丰言,人体钾的来源全靠从食物中获得,图A是人体钾代谢途径,图B是K+通过Na+-K+泵进入细胞示意图。回答相关问题:
(1)食物中的钾离子进入细胞需要经过______________系统,内环境在这个过程中发挥的作用是______________。
(2)胰岛素可激活细胞膜上的Na+-K+泵,协助小肠上皮细胞进行葡萄糖的运输,正常人饭后血钾含量会有所降低,原因是______________。
(3)血清钾高于5.5mmol/L以上,称为高血钾。尿毒症患者会出现高血清钾症是因为尿毒症患者的______________(填器官)排出钾功能障碍,______________是钾离子排出体外的主要途径,导致钾离子滞留在体内出现高血清钾症。
(4)大量研究表明,钾通道是钾离子转移至细胞外的主要途径,细胞丢钾是细胞凋亡的必要条件。据此,试提出一种治疗细胞毒性T细胞攻击正常组织细胞引起的自身免疫病的思路:______________。
32.某昆虫有正常眼和粗糙眼(A/a),直刚毛和焦刚毛(B/b)两对相对性状,控制两对相对性状的两对等位基因均不位于Y染色体上,现进行如下杂交实验:
回答下列问题:
(1)仅根据实验一,能否确定基因B/b位于常染色体上,并说明原因。__________________________。
(2)结合实验二,若让实验一F1中的个体自由交配,子代中焦刚毛所占的比例为__________。
实验二亲本的基因型为__________。实验二F1中出现上述表现型比例的原因是_______________。
(3)现有实验二F2中的一只正常眼直刚毛雌性个体,欲探究其基因型,请写出实验思路及预期结果。
实验思路: __________________________________________;
预期结果: _____________________________________________。
(二)选考题:共45分。请考生从2道物理题、2道化学题、2道生物题中每科任选一题作答。如果多做,则每科按所做的第一题计分。
33.【选修3-3】(15分)[来源:学|科|网]
(1)(5分)
下列说法正确的是_________。(填正确答案标号,选对1个给2分,选对2个得4分,选对3个得5分,每选错1个扣3分,最低得分0分)
A.熵是物体内分子运动无序程度的量度
B.扩散现象在气体、液体和固体中都能发生
C.某种物体的温度为0°C时,该物体中分子的平均动能为零
D.脱脂棉脱脂的目的是使它可以被水浸润,以便吸取药液
E.气体分子的体积等于气体的摩尔体积除以阿伏伽德罗常数
(2)(10分)
如图所示,新冠疫情期间,学校杀菌消毒用的压缩式喷雾器储液桶的总容量为6.0L,现倒入5.0L的消毒药液后盖紧盖子,开始打气,每打一次都能把体积为200mL、压强与大气压相同的空气打进储液桶,假设打气过程中药液不会向外喷出,储液桶气密性良好,出液管体积及出液口与储液桶底间高度差不计,周围环境温度不变,气体可视为理想气体,外界大气压恒为。求:
(1)当打气20次后,喷雾器内空气的压强及这个压强下最多能喷出的药液体积;
(2)要使喷雾器内的药液一次性全部喷完,至少需要打气的次数。
34.【选修3-4】(15分)
(1)(5分)
则下列说法正确的是_________。(填正确答案标号,选对1个给2分,选对2个得4分,选对3个得5分,每选错1个扣3分,最低得分0分)
A.变化的磁场产生变化的电场,变化的电场产生变化的磁场
B.如果波在传播过程中遇到尺寸比波长大得多的障碍物,该波就不能发生衍射现象
C.敲击音叉,围绕振动的音叉转一圈的过程中,会听到声音忽强忽弱,这是干涉现象
D.一束白光通过三棱镜后,在屏上出现彩色条纹,这是光的一种折射现象
E.在不同的惯性参考系中,一切物理规律都是相同的
(2)(10分)
一列简谐横波沿x轴负方向传播。图甲是t=1s时的波形图,图乙是该列波中某振动质点的振动图象,求;
(1)该波的传播速度。
(2)图甲中x=5m处的质点在振动过程中的位移随时间变化的关系式(不要求推导过程)。
35.[化学——选修3:物质结构与性质](15分)
回答下列问题:
(1)氨硼烷(NH3BH3)是一种潜在的储氢材料,它可由六元环状化合物(BH=NH)3通过3CH4+2(HB=NH)3 +6H2O=3CO2 + 6H3BNH3制得。
①N原子价电子排布式是___________,核外电子运动状态有___________种。
②NH3BH3中B原子的杂化类型是___________。
(2)已知液态的二氧化硫可以发生类似的水自身电离反应:2SO2(l) SO2++SO。SO2+与氮气是等电子体,其中的σ键和π键数目之比为___________,SO空间构型是___________。
(3)由O、Cl元素可组成不同的单质和化合物,其中Cl2O2能破坏臭氧层。Cl2O2的沸点比H2O2低,原因是___________。
(4)氮化镓是一种半导体材料。如图所示,晶胞结构可看作金刚石晶胞内部的碳原子被N原子代替(如b),顶点和面心的碳原子被Ga原子代替(如a)。
①与同一个Ga原子相连的N原子构成的空间构型为___________。
②用三维坐标表示原子的位置,若A点的坐标是(0,0,0),b点的坐标是___________。
③阿伏加德罗常数的值为NA,GaN晶体的密度为ρg·cm-3,则GaN晶胞边长为___________pm。
36.[化学——选修5:有机化学基础](15分)
化合物Ⅸ是合成一种新型多靶向抗肿瘤药物的中间体,其合成路线流程图如下:
回答下列问题:
(1)写出化合物Ⅰ的名称 ,化合物Ⅰ→Ⅱ的反应类型 。
(2)化合物Ⅲ由C、H、O三种原子组成,结构简式为 。
(3)化合物Ⅳ分子结构中的含氧官能团有 (填名称)。
(4)化合物Ⅴ在酸性下水解,有一种产物能在一定条件下自身聚合形成高聚物。形成该高聚物的反应方程式为 。
(5)化合物X是V的同系物,其相对分子质量比V小28,化合物X同时满足如下条件的同分异构体有_______种。
①苯环上有两种取代基,且能与溶液发生显色反应;
②能与溶液反应生成气体。
这些同分异构体中满足核磁共振氢谱峰面积比为6∶2∶2∶1∶1的结构简式 。
(6)根据上述信息,写出以苯乙烯( )与化合物Ⅶ为主要原料合成有机物 的路线流程为 。
37.[生物——选修1:生物技术实践](15分)
甜酒又名米酒、醪糟,是我国古代劳动人民创造出的一种经微生物发酵制作的营养食品。酿制后的甜酒口味香甜醇美、营养成分更易于人体吸收,能刺激消化液的分泌,增进食欲,是中老年人、孕产妇和身体虚弱者补气养血之佳品。酿制甜酒的主要原料是糯米和天然微生物酒曲。如图是甜酒酿制流程示意图,回答下列问题:
(1)酿制过程中所需的糯米需要蒸熟,其目的主要有两个:一是高温将糯米中大分子营养物质转化为小分子物质,更容易被微生物分解利用,二是________________________________。蒸熟的米饭相当于微生物培养中的________。
(2)加酒曲相当于微生物培养中的接种过程。酒曲中含有曲霉、毛霉和________等微生物,它们的代谢类型不尽相同,其中在甜酒酿制过程中促进酒精生成的微生物的代谢类型是________。
(3)沥冷是用水淋米饭,使其温度降低的过程,该过程中所用的水最好是________;将酒曲与米饭混匀的目的是________________________________________。
(4)为了在较短时间内获得品质上佳的甜酒产品,最好将发酵瓶置于温度为________℃条件下进行发酵。发酵过程中大多数微生物不能生长繁殖的原因是________________。
38.[生物——选修3:现代生物科技专题](15分)
我国现有的转基因抗虫棉对棉铃虫、红铃虫、卷叶虫等鳞翅目的害虫具有非常显著的抗性。苏云金芽孢杆菌的Bt基因能指导产生一种Bt杀虫蛋白,它对多种害虫具有毒杀作用。科学家将苏云金芽孢杆菌的Bt基因导入到棉花的叶肉细胞中,经过植物组织培养技术得到抗虫棉,抗虫棉的出现大大减少了农药的使用,保护了环境,抗虫培育过程如图所示。回答下列问题:
(1)获得的Bt基因常利用PCR技术在体外快速扩增,原理是________。从理论上推测,PCR扩增目的基因至第四轮循环产物中仅含有其中一种引物的DNA片段所占的比例为________。若退火温度过高,对扩增的影响是________(“无Bt基因”“Bt基因纯度低”或“Bt基因多”)。
(2)如果从限制酶A、B和C任选两种酶对Ti质粒进行切割产生不同末端,均会将Ti质粒切成两段,则形成的DNA片段有________种。重组质粒除了含有目的基因、复制原点、启动子和终止子外,还需要有________,作用是________________________________________________。
(3)Bt基因导入棉花叶肉细胞的方法是________。与诱变育种和杂交育种相比,利用基因工程技术培育的抗虫棉花植株,具有突出的优点是__________________________________________(答两点)。
2023年高考压轴卷——理综(全国甲卷) Word版含解析: 这是一份2023年高考压轴卷——理综(全国甲卷) Word版含解析,共38页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
2023高考压轴卷——理综(全国甲卷)(Word版附解析): 这是一份2023高考压轴卷——理综(全国甲卷)(Word版附解析),共38页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
2023高考压轴卷——理综(全国甲卷)(PDF版): 这是一份2023高考压轴卷——理综(全国甲卷)(PDF版),共39页。












