还剩13页未读,
继续阅读
成套系列资料,整套一键下载
2020-2022年北京市丰台区中考化学一模试题汇编-综合题
展开
这是一份2020-2022年北京市丰台区中考化学一模试题汇编-综合题,共16页。试卷主要包含了流程题,科学探究题,计算题,科普阅读题等内容,欢迎下载使用。
2020-2022年北京市丰台区中考化学一模试题汇编-综合题
一、流程题
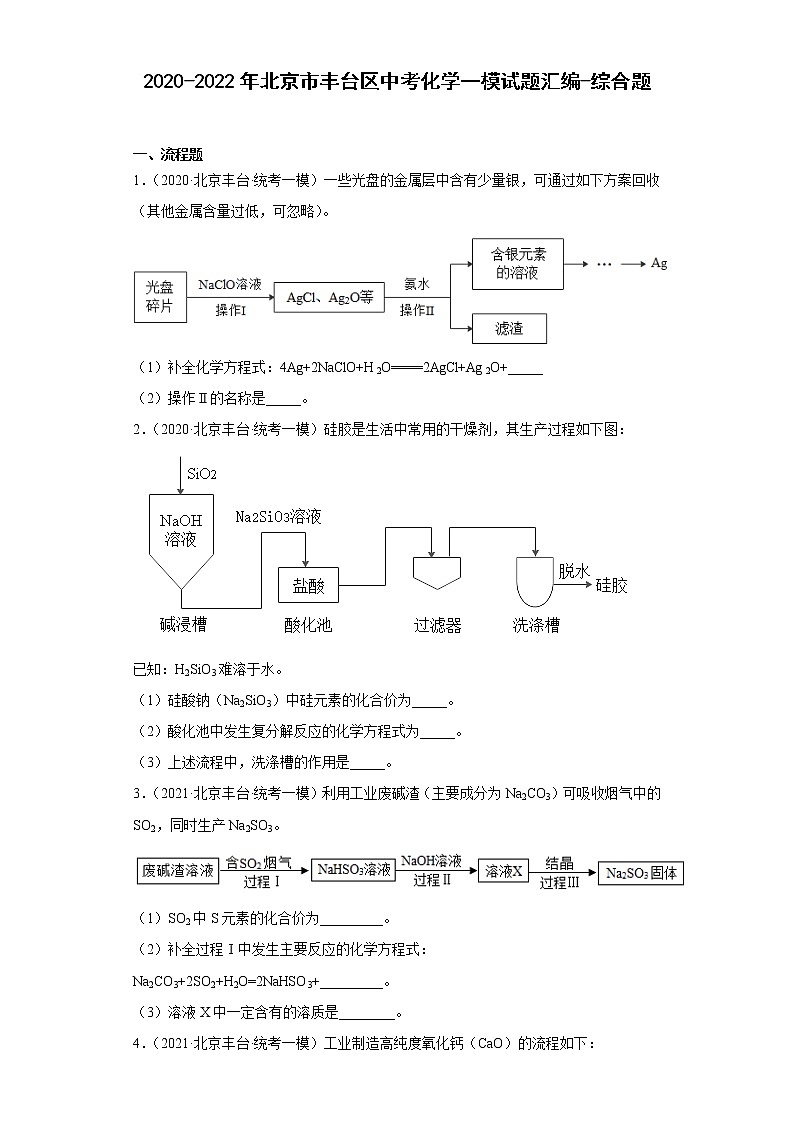
1.(2020·北京丰台·统考一模)一些光盘的金属层中含有少量银,可通过如下方案回收(其他金属含量过低,可忽略)。
(1)补全化学方程式:4Ag+2NaClO+H2O====2AgCl+Ag2O+_____
(2)操作Ⅱ的名称是_____。
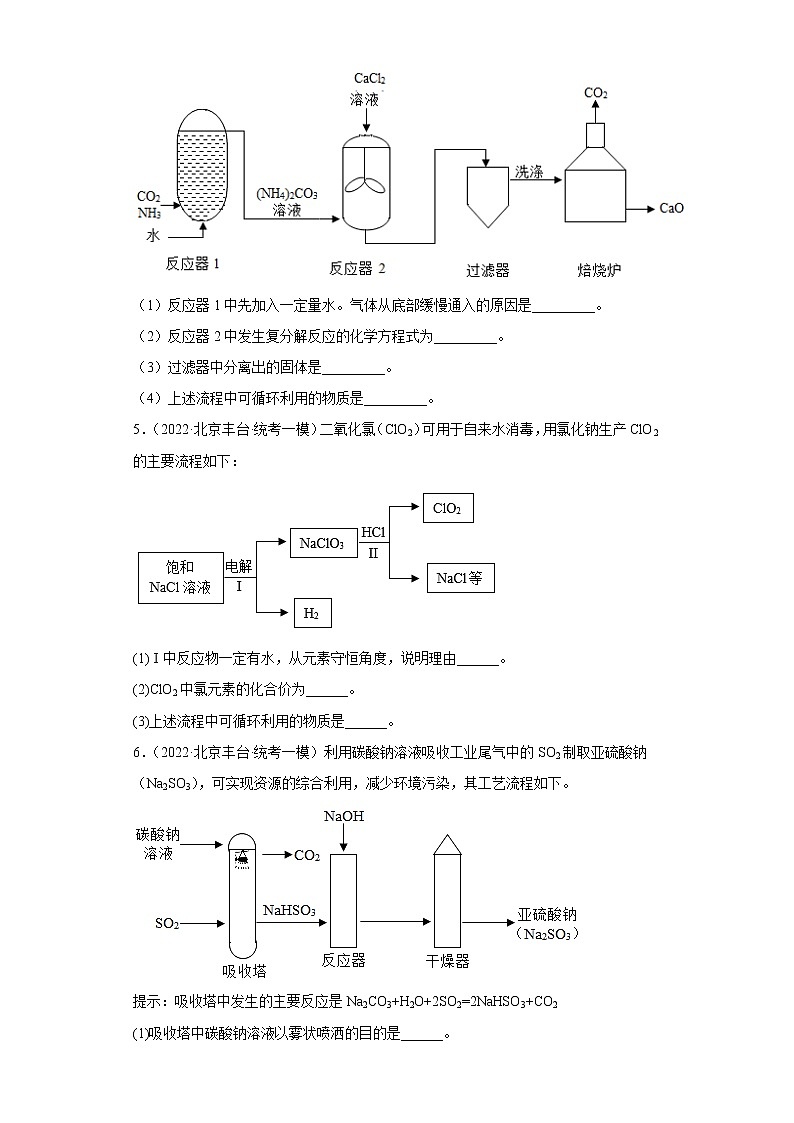
2.(2020·北京丰台·统考一模)硅胶是生活中常用的干燥剂,其生产过程如下图:
已知:H2SiO3难溶于水。
(1)硅酸钠(Na2SiO3)中硅元素的化合价为_____。
(2)酸化池中发生复分解反应的化学方程式为_____。
(3)上述流程中,洗涤槽的作用是_____。
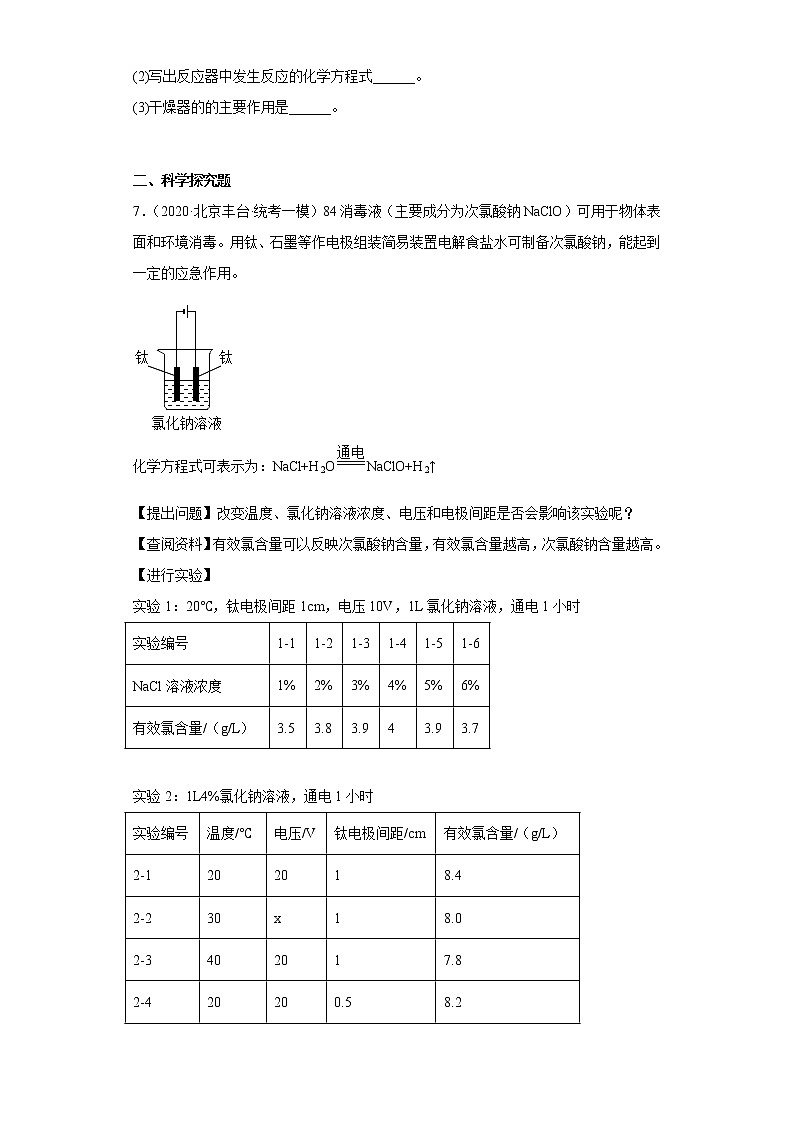
3.(2021·北京丰台·统考一模)利用工业废碱渣(主要成分为Na2CO3)可吸收烟气中的SO2,同时生产Na2SO3。
(1)SO2中S元素的化合价为_________。
(2)补全过程Ⅰ中发生主要反应的化学方程式:Na2CO3+2SO2+H2O=2NaHSO3+_________。
(3)溶液X中一定含有的溶质是________。
4.(2021·北京丰台·统考一模)工业制造高纯度氧化钙(CaO)的流程如下:
(1)反应器1中先加入一定量水。气体从底部缓慢通入的原因是_________。
(2)反应器2中发生复分解反应的化学方程式为_________。
(3)过滤器中分离出的固体是_________。
(4)上述流程中可循环利用的物质是_________。
5.(2022·北京丰台·统考一模)二氧化氯(ClO2)可用于自来水消毒,用氯化钠生产ClO2的主要流程如下:
(1)Ⅰ中反应物一定有水,从元素守恒角度,说明理由______。
(2)ClO2中氯元素的化合价为______。
(3)上述流程中可循环利用的物质是______。
6.(2022·北京丰台·统考一模)利用碳酸钠溶液吸收工业尾气中的SO2制取亚硫酸钠(Na2SO3),可实现资源的综合利用,减少环境污染,其工艺流程如下。
提示:吸收塔中发生的主要反应是Na2CO3+H2O+2SO2=2NaHSO3+CO2
(1)吸收塔中碳酸钠溶液以雾状喷洒的目的是______。
(2)写出反应器中发生反应的化学方程式______。
(3)干燥器的的主要作用是______。
二、科学探究题
7.(2020·北京丰台·统考一模)84消毒液(主要成分为次氯酸钠NaClO)可用于物体表面和环境消毒。用钛、石墨等作电极组装简易装置电解食盐水可制备次氯酸钠,能起到一定的应急作用。
化学方程式可表示为:NaCl+H2ONaClO+H2↑
【提出问题】改变温度、氯化钠溶液浓度、电压和电极间距是否会影响该实验呢?
【查阅资料】有效氯含量可以反映次氯酸钠含量,有效氯含量越高,次氯酸钠含量越高。
【进行实验】
实验1:20℃,钛电极间距1cm,电压10V,1L氯化钠溶液,通电1小时
实验编号
1-1
1-2
1-3
1-4
1-5
1-6
NaCl溶液浓度
1%
2%
3%
4%
5%
6%
有效氯含量/(g/L)
3.5
3.8
3.9
4
3.9
3.7
实验2:1L4%氯化钠溶液,通电1小时
实验编号
温度/℃
电压/V
钛电极间距/cm
有效氯含量/(g/L)
2-1
20
20
1
8.4
2-2
30
x
1
8.0
2-3
40
20
1
7.8
2-4
20
20
0.5
8.2
2-5
20
20
1.5
8
【解释与结论】
(1)由实验1可知,有效氯含量随氯化钠溶液浓度变化的规律是_____。
(2)设计实验2-1、2-4、2-5的目的是_____。
(3)实验2-2中,x=_____。
(4)能证明电压对有效氯含量有影响的实验是_____(填实验编号)。
【反思与评价】
(5)实验过程需在通风处进行并严禁烟火,原因是_____。
(6)84消毒液对皮肤和口腔黏膜具有腐蚀性和刺激性。一般市售84消毒液有效氯含量为50g/L,根据使用需要加水稀释成0.2g/L、0.5g/L、1g/L。
结合本实验,下列分析正确的是_____(填字母)。
A 使用84消毒液时建议佩戴防护口罩与手套
B 本实验中,温度越高,有效氯含量越高
C 实验2-1中,有效氯含量达到市售84消毒液标准
D 本实验制备的次氯酸钠溶液需稀释后使用
8.(2021·北京丰台·统考一模)俗话说“碱去油污、酸除锈”,纯碱(Na2CO3)能做日常生活中的去油污剂。
Ⅰ.探究温度和浓度对Na2CO3溶液去油污效果的影响
【进行实验】室温下,取8个大小相同涂有0.5g植物油的玻璃片,分别浸泡在100g试剂中15分钟,取出干燥后观察实验现象。实验结果如下:
第1组
第2组
第3组
实验编号
①
②
③
④
⑤
⑥
⑦
⑧
温度
20℃
20℃
20℃
20℃
30℃
30℃
40℃
40℃
试剂
水
1% Na2CO3溶液
5% Na2CO3溶液
10% Na2CO3溶液
水
10% Na2CO3溶液
水
10% Na2CO3溶液
去油污效果
5%
16%
20%
27%
60%
90%
75%
97%
已知:去油污效果=去除油脂质量/初始油脂质量
【解释与结论】
(1)配制100g 10% Na2CO3溶液,需要称量Na2CO3固体_________g。
(2)设计实验①的目的是_________。
(3)欲探究“浓度对Na2CO3溶液去油污效果的影响”需对比的实验是_________(填实验编号)。
(4)对比实验④⑥⑧可得到的结论是_________。
Ⅱ.探究温度和浓度对Na2CO3溶液碱性的影响
【查阅资料】相同温度下,溶液的pH越大,碱性越强。
【进行实验】
实验⑨:20℃时,用pH传感器测定不同浓度Na2CO3溶液的pH(结果如图1)。
实验⑩:用pH传感器和温度传感器测定不同温度下10% Na2CO3溶液的pH(结果如图2)。
【解释与结论】
(5)结合第1组实验和图1数据分析,欲得出“溶液的碱性越强,Na2CO3溶液去油污效果越好”的依据是_________。
(6)由图2可知,10% Na2CO3溶液的pH与温度的关系是_________。
【反思与评价】
【查阅资料】相同浓度下,Na2CO3溶液的温度越高,碱性越强
(7)综合以上实验分析,下列说法正确的是_________(填字母序号)。
A 热Na2CO3溶液去油污效果更好可能与“温度升高,水的去油污能力增强”有关
B 热Na2CO3溶液去油污效果更好可能与“温度升高,溶液碱性增强”有关
C 10% Na2CO3溶液在不同温度时,pH可能相同
D 溶液碱性增强,pH一定增大
三、计算题
9.(2021·北京丰台·统考一模)氧烛(主要成分为NaClO3)是一种用于缺氧环境中自救的化学氧源,广泛用于航空、航海等领域。其产生氧气的主要反应原理为。计算213g NaClO3完全分解时产生氧气的质量。
10.(2022·北京丰台·统考一模)工业用二氧化碳和氨气(NH3)合成尿素[CO(NH2)2],反应的化学方程式如下:2NH3 + CO2CO(NH2)2 + H2O。计算68g氨气完全反应,消耗二氧化碳的质量。
四、科普阅读题
11.(2020·北京丰台·统考一模)阅读下面科普短文。
藜麦营养成分丰富且比例均衡,被列为“全球十大健康营养食品之一”。
藜麦的蛋白质含量与牛肉相当,且品质不亚于肉源蛋白与奶源蛋白。同时它还含有种类丰富的矿物元素(见图1),以及多种人体所需要的维生素。藜麦不含胆固醇,富含膳食纤维,能加速肠道蠕动。其脂肪含量与热量都较低,食用后有饱腹感,有利于减肥人群控制体重。
我国很多地区开展了藜麦种植。农业研究小组研究了化肥与藜麦产量的关系。实验数据如表1、图2所示。
表1化肥用量说明
化肥种类
磷肥
钾肥
符号
P0
P1
K0
K1
K2
K3
用量/(千克/公顷)
0
40
0
40
80
120
相关实验数据为国内的藜麦种植及推广提供了依据。
请依据文章内容回答下列问题:
(1)藜麦所含人体必需的营养素有_____(任写两种)。
(2)藜麦中的铁元素可以预防_____(填“贫血”或“佝偻病”)。
(3)藜麦被列为“全球十大健康营养食品之一”的原因是_____。
(4)由图2可知,磷肥、钾肥最佳的施用量为_____。
(5)下列说法正确的是_____。
A 藜麦适合减肥人群食用
B 胆固醇高的人,不适合食用藜麦
C 藜麦中,钙、铁、锌的含量均高于小麦和稻米
D 种植藜麦时,施用钾肥的量越大,产量越高
12.(2021·北京丰台·统考一模)阅读下面科普短文。
2021年3月,三星堆遗址新出土重要文物500多件,有高2.62米的青铜大立人(图1)、高3.95米的青铜神树、由金箔包裹的权杖、重约286克的金面具及玉石器和象牙等,多属前所未见的稀世之珍。
青铜是金属冶铸史上最早出现的合金,与纯铜相比,其强度高、熔点低、铸造性好、耐磨且耐腐蚀。《周礼·考工记》中对制作钟鼎、斧斤、戈戟等青铜器物中铜锡的比例作了详细的规定(图2)。在地下埋藏的青铜器表面会出现绿色的铜锈,其主要成分为碱式碳酸铜[Cu2(OH)2CO3]。
金属的冶炼和使用在不断发展,人们在冶炼青铜的基础上逐渐掌握了冶炼铁的技术。中国目前发现的最古老铁器是甘肃省出土的两块铁条,经碳14检测,其冶炼年代约在3510~3310年前,两块铁条锈蚀严重。
随着科学技术的发展,铝、钛等金属逐渐被冶炼并使用,但金属矿物的储量是有限的。据不完全统计,世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%~40%。金属资源的合理利用与保护十分重要。
依据文章内容回答下列问题。
(1)下列属于金属材料的是_________(填字母序号)。
A 青铜大立人 B 金面具 C 象牙 D 玉石器
(2)青铜与纯铜相比,提升了哪些性能_________(答一条即可)。
(3)依据铜锈的主要成分Cu2(OH)2CO3,可推断铜生锈的过程是铜与空气中的CO2、O2和_________等发生化学反应的过程。
(4)依据图2可知,用于生产戈戟的青铜器中,铜和锡的比例为_________。
(5)下列说法正确的是_________(填字母序号)。
A 青铜器中铜锡比例不同,所得合金的性能也不同
B 人类大规模使用金属的先后顺序与金属活动性有关
C 金属资源是取之不尽的
D 将废旧金属回收利用可节约金属资源
13.(2022·北京丰台·统考一模)阅读下面科普短文。
玫瑰红、草绿、钴蓝、柠檬黄…这些漂亮的颜色深受人们喜爱。每一种新的颜料出现,其所展现的颜色便被赋予了新的名字。
人类获取颜料主要有以下三个途径。
天然矿物:早期颜料主要来源,且大多数来自特殊地区出产的矿物。北宋《千里江山图》便是用朱砂、赭石(主要成分为Fe2O3)、石青和孔雀石等所绘,时隔千年,画卷中颜色依然层次分明、色彩浓丽、常见的矿石颜料还有紫云、蓝闪石、雄黄等。
动植物:从雌胭脂虫体内提取的胭脂虫红,用于食品、化妆品、纺织品等生产。
从蓝草、桑、紫草中提取的色素,广泛应用于各行各业、我们常见的紫甘蓝细胞液中含有一种花色苷的化合物,在pH环境不同的条件下,会发生反应,呈现出不同颜色(见下表),用其绘画十分有趣。
pH
1
3
5
7
9
11
13
颜色
红
紫红
浅紫
紫
蓝
绿
黄
合成:近代有机化学蓬勃发展,涌现出了大量合成颜料。但据记载早在公元四世纪,人类就掌握了合成颜料——铅白的加工方法。将铅条堆放在醋和发酵物上,置于密闭空间内,利用发酵产生的热量和二氧化碳,最终生成铅白。
随着科技的发展,一定会有更多靓丽的颜色点缀我们的生活。
依据文章内容回答下列问题。
(1)写出一种来自天然矿物的颜料______。
(2)千里江山图历经千年,颜色依然分明,说明所用矿石颜料化学性质______(填“稳定”或“不稳定”)。
(3)向稀盐酸中加入紫甘蓝汁液,可能呈现的颜色是______(填“红色”或“蓝色”)。
(4)公元四世纪,人类使用铅条(Pb)与氧气、水和二氧化碳发生反应,最终获得了铅白[Pb3(OH)4CO3]。铅白由______种元素组成。
(5)下列说法正确的是______(填字母序号)。A.颜料的命名多与来源有关 B.矿物颜料取之不尽、用之不竭
C.新颜料的出现与科技发展有关 D.铅白可能具有毒性
参考答案:
1. 2NaOH 过滤
【详解】(1)该反应符合质量手恒定律,反应前后各元素的原子个数不变,反应物比生成物多2个钠原子、2个氧原子和2个氢原子,补全化学方程式:4Ag+2NaClO+H2O====2AgCl+Ag2O+2NaOH;
(2)操作Ⅱ将固体与体液分离的名称是:过滤。
2. +4 Na2SiO3+2HCl=2NaCl+H2SiO3↓ 洗去H2SiO3沉淀表面残留的滤液
【详解】(1)解:设硅酸钠(Na2SiO3)中硅元素的化合价为x,则(+1)×2+x+(-2)×3=0,x=+4;
(2)酸化池中硅酸钠与稀盐酸发生反应产生氯化钠和硅酸沉淀的化学方程式为Na2SiO3+2HCl=2NaCl+H2SiO3↓。
(3)上述流程中,洗涤槽的作用是:洗去H2SiO3沉淀表面残留的滤液,得到纯净的硅酸产品。
3. +4 CO2 Na2SO3
【详解】(1)SO2中氧元素的化合价为-2,根据化合物中各元素化合价的代数和为零,S元素的化合价为+4。
(2)反应前有2Na、C、8O、2S、2H,反应后(X除外)有2Na、6O、2S、2H,根据化学反应前后各种原子个数相等,生成物中还应含1个C、2个O,故过程Ⅰ中发生主要反应的化学方程式为:Na2CO3+2SO2+H2O=2NaHSO3+CO2。
(3)因为溶液X经过结晶得到Na2SO3固体,则溶液X中一定含有的溶质是Na2SO3。
4. 使反应物充分接触,充分反应 CaCO3 CO2
【详解】(1)反应器1中先加入一定量水。气体从底部缓慢通入的原因是:使反应物充分接触,充分反应;
(2)反应器2中,氯化钙和碳酸铵反应生成氯化铵和碳酸钙,该反应的化学方程式为:;
(3)氯化钙和碳酸铵反应生成氯化铵和碳酸钙,碳酸钙难溶于水,故过滤器中分离出的固体是CaCO3;
(4)由图可知,二氧化碳既是反应物。又是生成物,可以循环利用。
5.(1)生成物中含有氢、氧元素
(2)+4##+4价
(3)NaCl##氯化钠
【详解】(1)根据质量守恒定律可知反应前后元素种类不变,由反应后生成的两种物质化学式是,反应后元素是钠元素、氢元素、氧元素和氯元素,而反应前氯化钠只含钠元素和氯元素,故反应物还有水反应,故填:生成物中含有氢、氧元素;
(2)化合物中化合价代数和为0,设氯元素化合价为,,故填:+4或+4价;
(3)能循环使用的物质在流程中既是反应物又是生成物,故由题意判断上述流程中可循环利用的物质是氯化钠,故填:氯化钠或。
6.(1)增大接触面积,使反应更充分
(2)
(3)除去水
【详解】(1)吸收塔中碳酸钠溶液以雾状喷洒是为了增大接触面积,使反应更充分;
(2)根据流程可知,亚硫酸氢钠和氢氧化钠反应生成亚硫酸钠和水,化学方程式为:;
(3)反应是在溶液中进行的,故要得到亚硫酸钠固体,则应在干燥器中除去水,故填:除去水。
7. 其他条件相同时,随着氯化钠溶液浓度从1%到6%,有效氯含量先增大后减小 探究改变钛电极间距是否影响该实验 20 1-4和2-1 生成可燃性气体氢气,遇明火易爆炸 AD
【详解】1)由实验1可知,有效氯含量随氯化钠溶液浓度变化的规律是:他条件相同时,随着氯化钠溶液浓度从1%到6%,有效氯含量先增大后减小,4% 时最大;
(2)设计实验2-1、2-4、2-5中钛电极距离不同的目的是:探究改变钛电极间距是否影响该实验;
(3)实验2-2中,电压属于控制定量,与其他实验电压相等,x=20。
(4)能证明电压对有效氯含量有影响的实验是:1-4和2-1中电压分别是10V和20V,其他条件都相同,但有效氯含量不同;
(5)实验过程需在通风处进行并严禁烟火,原因是:生成的氢气具有可燃性,在空气中达到一定浓度,遇明火易爆炸;
(6)84消毒液对皮肤和口腔黏膜具有腐蚀性和刺激性。一般市售84消毒液有效氯含量为50g/L,根据使用需要加水稀释成0.2g/L、0.5g/L、1g/L。
结合本实验,下列分析正确的是:
A、84消毒液有刺激性气味,且具有腐蚀性,使用时建议佩戴防护口罩与手套;故选项正确;
B、本实验中,温度为20℃时,有效氯含量最高;故选项错误;
C、实验2-1中,有效氯含量为8.4g/L,没有达到市售84消毒液标准(有效氯含量50g/L);故选项错误;
D、本实验制备的次氯酸钠溶液的有效氯含量为实验1-1(3.5g/L)依然大于实用最高有效氯含量(1g/L),需稀释后使用;故选项正确;
故选:AD。
8. 10 20℃时,排除水对本实验的影响 ②③④ 相同浓度时,温度越高,Na2CO3溶液去油污效果越好 相同温度时,浓度越大,Na2CO3溶液的pH越大,碱性越强,去油污效果越好 在20℃至80℃范围内,随温度升高,10%Na2CO3溶液的pH先升高后减小 ABC
【详解】(1)配制100g 10% Na2CO3溶液,需要称量Na2CO3固体的质量为:100g×10%=10g。
(2)设计实验①的目的是:对照实验,20℃时,排除水对本实验的影响。
(3)对比实验必须控制变量,变量唯一性,所以欲探究“浓度对Na2CO3溶液去油污效果的影响”,除了浓度不同,其它因素都应相同,故需对比的实验是②③④。
(4)④⑥⑧只是温度不同,其它条件相同,所以对比实验④⑥⑧可得到的结论是相同浓度时,温度越高,Na2CO3溶液去油污效果越好。
(5)结合第1组实验和图1数据分析,欲得出“溶液的碱性越强,Na2CO3溶液去油污效果越好”的依据是相同温度时,浓度越大,Na2CO3溶液的pH越大,碱性越强,去油污效果越好。
(6)由图2可知,10% Na2CO3溶液的pH与温度的关系是在20℃至80℃范围内,随温度升高,10%Na2CO3溶液的pH先升高后减小。
(7)A 、由实验④⑥⑧可知,热Na2CO3溶液去油污效果更好可能与“温度升高,水的去油污能力增强”有关,此选项正确;
B、在20℃至50℃范围内,随温度升高,10%Na2CO3溶液的pH增大,即碱性增强,所以热Na2CO3溶液去油污效果更好可能与“温度升高,溶液碱性增强”有关,此选项正确;
C、由图2可知,10% Na2CO3溶液在不同温度时,pH可能相同,此选项正确;
D、由图2可知,溶液碱性增强,pH不一定增大,此选项错误。
故选ABC。
9.解:设产生氧气的质量为x
解得x=96 g。
答:产生氧气的质量为96 g。
【详解】见答案。
10.设:消耗二氧化碳的质量为x。
x=88 g
答:消耗二氧化碳的质量为88g。
【分析】利用化学方程式姐姐反应中物质的质量关系,可由反应的氨气质量计算需要二氧化碳的质量。
【详解】见答案。
11. 蛋白质、维生素(其他合理答案均可) 贫血 藜麦营养成分丰富且比例均衡 磷肥40千克/公顷,钾肥80千克/公顷 AC
【详解】(1)藜麦的蛋白质含量与牛肉相当,且品质不亚于肉源蛋白与奶源蛋白,同时它还含有种类丰富的矿物元素,以及多种人体所需要的维生素;藜麦所含人体必需的营养素有:蛋白质、维生素。
(2)藜麦中的铁元素可以预防贫血。
(3)藜麦被列为“全球十大健康营养食品之一”的原因是:藜麦营养成分丰富且比例均衡,有助于身体健康。
(4)由图2可知,磷肥、钾肥最佳的施用量为:磷肥40千克/公顷,钾肥80千克/公顷,因为该肥料培育出的穗粒最饱满,质量最大;
(5)下列说法正确的是:
A、藜麦营养成分丰富且比例均衡,适合减肥人群食用;故选项正确;
B、藜麦中含有丰富的维生素,胆固醇高的人,依然适合食用藜麦;故选项错误;
C、由图1可知:藜麦中,钙、铁、锌的含量均高于小麦和稻米;故选项正确;
D、种植藜麦时,磷肥40千克/公顷,钾肥80千克/公顷,产量最高;故选项错误;
故选:AC。
12. AB 强度高、熔点低、铸造性好、耐磨、耐腐蚀(答一条即可) H2O 4:1 ABD
【详解】(1)青铜是铜的合金,青铜和金属于金属材料。
故选AB;
(2)青铜是金属冶铸史上最早出现的合金,与纯铜相比,其强度高、熔点低、铸造性好、耐磨且耐腐蚀;
(3)根据质量守恒定律,化学反应前后,元素的种类不变,反应物中含Cu、O、H、C,生成物中也应含Cu、O、H、C,故铜生锈的过程是铜与空气中的二氧化碳、氧气和H2O发生化学反应的过程;
(4)依据图2可知,用于生产戈戟的青铜器中,铜和锡的比例为:80%:20%=4:1;
(5)A、青铜器中铜锡比例不同,所得合金的性能也不同,说法正确,符合题意;
B、人类大规模使用金属的先后顺序与金属活动性有关,金属活动性越强,使用的时间越晚,符合题意;
C、金属资源有限,应保护金属资源,不符合题意;
D、将废旧金属回收利用可节约金属资源,符合题意。
故选ABD。
13.(1)朱砂、赭石、石青、孔雀石等
(2)稳定
(3)红色
(4)四##4
(5)ACD
【详解】(1)由题干信息可知,常见的矿石颜料朱砂、赭石、石青、孔雀石、紫云、蓝闪石、雄黄等;
(2)千里江山图历经千年,颜色依然分明,说明所用矿石颜料化学性质稳定,很难与其它物质反应;
(3)稀盐酸为强酸,显酸性,由表可知,向稀盐酸中加入紫甘蓝汁液,可能呈现的颜色是红色;
(4)由化学式可知,铅白由Pb、O、H、C四种元素组成;
(5)A、由题干信息可知,颜料的命名多与来源有关,如从雌胭脂虫体内提取的颜料名称为胭脂虫红,符合题意;
B、矿物颜料是有限的,应合理使用,不符合题意;
C、由题干信息可知,新颜料的出现与科技发展有关,随着科技的发展,一定会有更多靓丽的颜色点缀我们的生活,符合题意;
D、铅白中含铅元素,故铅白可能具有毒性,符合题意。
故选ACD。
2020-2022年北京市丰台区中考化学一模试题汇编-综合题
一、流程题
1.(2020·北京丰台·统考一模)一些光盘的金属层中含有少量银,可通过如下方案回收(其他金属含量过低,可忽略)。
(1)补全化学方程式:4Ag+2NaClO+H2O====2AgCl+Ag2O+_____
(2)操作Ⅱ的名称是_____。
2.(2020·北京丰台·统考一模)硅胶是生活中常用的干燥剂,其生产过程如下图:
已知:H2SiO3难溶于水。
(1)硅酸钠(Na2SiO3)中硅元素的化合价为_____。
(2)酸化池中发生复分解反应的化学方程式为_____。
(3)上述流程中,洗涤槽的作用是_____。
3.(2021·北京丰台·统考一模)利用工业废碱渣(主要成分为Na2CO3)可吸收烟气中的SO2,同时生产Na2SO3。
(1)SO2中S元素的化合价为_________。
(2)补全过程Ⅰ中发生主要反应的化学方程式:Na2CO3+2SO2+H2O=2NaHSO3+_________。
(3)溶液X中一定含有的溶质是________。
4.(2021·北京丰台·统考一模)工业制造高纯度氧化钙(CaO)的流程如下:
(1)反应器1中先加入一定量水。气体从底部缓慢通入的原因是_________。
(2)反应器2中发生复分解反应的化学方程式为_________。
(3)过滤器中分离出的固体是_________。
(4)上述流程中可循环利用的物质是_________。
5.(2022·北京丰台·统考一模)二氧化氯(ClO2)可用于自来水消毒,用氯化钠生产ClO2的主要流程如下:
(1)Ⅰ中反应物一定有水,从元素守恒角度,说明理由______。
(2)ClO2中氯元素的化合价为______。
(3)上述流程中可循环利用的物质是______。
6.(2022·北京丰台·统考一模)利用碳酸钠溶液吸收工业尾气中的SO2制取亚硫酸钠(Na2SO3),可实现资源的综合利用,减少环境污染,其工艺流程如下。
提示:吸收塔中发生的主要反应是Na2CO3+H2O+2SO2=2NaHSO3+CO2
(1)吸收塔中碳酸钠溶液以雾状喷洒的目的是______。
(2)写出反应器中发生反应的化学方程式______。
(3)干燥器的的主要作用是______。
二、科学探究题
7.(2020·北京丰台·统考一模)84消毒液(主要成分为次氯酸钠NaClO)可用于物体表面和环境消毒。用钛、石墨等作电极组装简易装置电解食盐水可制备次氯酸钠,能起到一定的应急作用。
化学方程式可表示为:NaCl+H2ONaClO+H2↑
【提出问题】改变温度、氯化钠溶液浓度、电压和电极间距是否会影响该实验呢?
【查阅资料】有效氯含量可以反映次氯酸钠含量,有效氯含量越高,次氯酸钠含量越高。
【进行实验】
实验1:20℃,钛电极间距1cm,电压10V,1L氯化钠溶液,通电1小时
实验编号
1-1
1-2
1-3
1-4
1-5
1-6
NaCl溶液浓度
1%
2%
3%
4%
5%
6%
有效氯含量/(g/L)
3.5
3.8
3.9
4
3.9
3.7
实验2:1L4%氯化钠溶液,通电1小时
实验编号
温度/℃
电压/V
钛电极间距/cm
有效氯含量/(g/L)
2-1
20
20
1
8.4
2-2
30
x
1
8.0
2-3
40
20
1
7.8
2-4
20
20
0.5
8.2
2-5
20
20
1.5
8
【解释与结论】
(1)由实验1可知,有效氯含量随氯化钠溶液浓度变化的规律是_____。
(2)设计实验2-1、2-4、2-5的目的是_____。
(3)实验2-2中,x=_____。
(4)能证明电压对有效氯含量有影响的实验是_____(填实验编号)。
【反思与评价】
(5)实验过程需在通风处进行并严禁烟火,原因是_____。
(6)84消毒液对皮肤和口腔黏膜具有腐蚀性和刺激性。一般市售84消毒液有效氯含量为50g/L,根据使用需要加水稀释成0.2g/L、0.5g/L、1g/L。
结合本实验,下列分析正确的是_____(填字母)。
A 使用84消毒液时建议佩戴防护口罩与手套
B 本实验中,温度越高,有效氯含量越高
C 实验2-1中,有效氯含量达到市售84消毒液标准
D 本实验制备的次氯酸钠溶液需稀释后使用
8.(2021·北京丰台·统考一模)俗话说“碱去油污、酸除锈”,纯碱(Na2CO3)能做日常生活中的去油污剂。
Ⅰ.探究温度和浓度对Na2CO3溶液去油污效果的影响
【进行实验】室温下,取8个大小相同涂有0.5g植物油的玻璃片,分别浸泡在100g试剂中15分钟,取出干燥后观察实验现象。实验结果如下:
第1组
第2组
第3组
实验编号
①
②
③
④
⑤
⑥
⑦
⑧
温度
20℃
20℃
20℃
20℃
30℃
30℃
40℃
40℃
试剂
水
1% Na2CO3溶液
5% Na2CO3溶液
10% Na2CO3溶液
水
10% Na2CO3溶液
水
10% Na2CO3溶液
去油污效果
5%
16%
20%
27%
60%
90%
75%
97%
已知:去油污效果=去除油脂质量/初始油脂质量
【解释与结论】
(1)配制100g 10% Na2CO3溶液,需要称量Na2CO3固体_________g。
(2)设计实验①的目的是_________。
(3)欲探究“浓度对Na2CO3溶液去油污效果的影响”需对比的实验是_________(填实验编号)。
(4)对比实验④⑥⑧可得到的结论是_________。
Ⅱ.探究温度和浓度对Na2CO3溶液碱性的影响
【查阅资料】相同温度下,溶液的pH越大,碱性越强。
【进行实验】
实验⑨:20℃时,用pH传感器测定不同浓度Na2CO3溶液的pH(结果如图1)。
实验⑩:用pH传感器和温度传感器测定不同温度下10% Na2CO3溶液的pH(结果如图2)。
【解释与结论】
(5)结合第1组实验和图1数据分析,欲得出“溶液的碱性越强,Na2CO3溶液去油污效果越好”的依据是_________。
(6)由图2可知,10% Na2CO3溶液的pH与温度的关系是_________。
【反思与评价】
【查阅资料】相同浓度下,Na2CO3溶液的温度越高,碱性越强
(7)综合以上实验分析,下列说法正确的是_________(填字母序号)。
A 热Na2CO3溶液去油污效果更好可能与“温度升高,水的去油污能力增强”有关
B 热Na2CO3溶液去油污效果更好可能与“温度升高,溶液碱性增强”有关
C 10% Na2CO3溶液在不同温度时,pH可能相同
D 溶液碱性增强,pH一定增大
三、计算题
9.(2021·北京丰台·统考一模)氧烛(主要成分为NaClO3)是一种用于缺氧环境中自救的化学氧源,广泛用于航空、航海等领域。其产生氧气的主要反应原理为。计算213g NaClO3完全分解时产生氧气的质量。
10.(2022·北京丰台·统考一模)工业用二氧化碳和氨气(NH3)合成尿素[CO(NH2)2],反应的化学方程式如下:2NH3 + CO2CO(NH2)2 + H2O。计算68g氨气完全反应,消耗二氧化碳的质量。
四、科普阅读题
11.(2020·北京丰台·统考一模)阅读下面科普短文。
藜麦营养成分丰富且比例均衡,被列为“全球十大健康营养食品之一”。
藜麦的蛋白质含量与牛肉相当,且品质不亚于肉源蛋白与奶源蛋白。同时它还含有种类丰富的矿物元素(见图1),以及多种人体所需要的维生素。藜麦不含胆固醇,富含膳食纤维,能加速肠道蠕动。其脂肪含量与热量都较低,食用后有饱腹感,有利于减肥人群控制体重。
我国很多地区开展了藜麦种植。农业研究小组研究了化肥与藜麦产量的关系。实验数据如表1、图2所示。
表1化肥用量说明
化肥种类
磷肥
钾肥
符号
P0
P1
K0
K1
K2
K3
用量/(千克/公顷)
0
40
0
40
80
120
相关实验数据为国内的藜麦种植及推广提供了依据。
请依据文章内容回答下列问题:
(1)藜麦所含人体必需的营养素有_____(任写两种)。
(2)藜麦中的铁元素可以预防_____(填“贫血”或“佝偻病”)。
(3)藜麦被列为“全球十大健康营养食品之一”的原因是_____。
(4)由图2可知,磷肥、钾肥最佳的施用量为_____。
(5)下列说法正确的是_____。
A 藜麦适合减肥人群食用
B 胆固醇高的人,不适合食用藜麦
C 藜麦中,钙、铁、锌的含量均高于小麦和稻米
D 种植藜麦时,施用钾肥的量越大,产量越高
12.(2021·北京丰台·统考一模)阅读下面科普短文。
2021年3月,三星堆遗址新出土重要文物500多件,有高2.62米的青铜大立人(图1)、高3.95米的青铜神树、由金箔包裹的权杖、重约286克的金面具及玉石器和象牙等,多属前所未见的稀世之珍。
青铜是金属冶铸史上最早出现的合金,与纯铜相比,其强度高、熔点低、铸造性好、耐磨且耐腐蚀。《周礼·考工记》中对制作钟鼎、斧斤、戈戟等青铜器物中铜锡的比例作了详细的规定(图2)。在地下埋藏的青铜器表面会出现绿色的铜锈,其主要成分为碱式碳酸铜[Cu2(OH)2CO3]。
金属的冶炼和使用在不断发展,人们在冶炼青铜的基础上逐渐掌握了冶炼铁的技术。中国目前发现的最古老铁器是甘肃省出土的两块铁条,经碳14检测,其冶炼年代约在3510~3310年前,两块铁条锈蚀严重。
随着科学技术的发展,铝、钛等金属逐渐被冶炼并使用,但金属矿物的储量是有限的。据不完全统计,世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%~40%。金属资源的合理利用与保护十分重要。
依据文章内容回答下列问题。
(1)下列属于金属材料的是_________(填字母序号)。
A 青铜大立人 B 金面具 C 象牙 D 玉石器
(2)青铜与纯铜相比,提升了哪些性能_________(答一条即可)。
(3)依据铜锈的主要成分Cu2(OH)2CO3,可推断铜生锈的过程是铜与空气中的CO2、O2和_________等发生化学反应的过程。
(4)依据图2可知,用于生产戈戟的青铜器中,铜和锡的比例为_________。
(5)下列说法正确的是_________(填字母序号)。
A 青铜器中铜锡比例不同,所得合金的性能也不同
B 人类大规模使用金属的先后顺序与金属活动性有关
C 金属资源是取之不尽的
D 将废旧金属回收利用可节约金属资源
13.(2022·北京丰台·统考一模)阅读下面科普短文。
玫瑰红、草绿、钴蓝、柠檬黄…这些漂亮的颜色深受人们喜爱。每一种新的颜料出现,其所展现的颜色便被赋予了新的名字。
人类获取颜料主要有以下三个途径。
天然矿物:早期颜料主要来源,且大多数来自特殊地区出产的矿物。北宋《千里江山图》便是用朱砂、赭石(主要成分为Fe2O3)、石青和孔雀石等所绘,时隔千年,画卷中颜色依然层次分明、色彩浓丽、常见的矿石颜料还有紫云、蓝闪石、雄黄等。
动植物:从雌胭脂虫体内提取的胭脂虫红,用于食品、化妆品、纺织品等生产。
从蓝草、桑、紫草中提取的色素,广泛应用于各行各业、我们常见的紫甘蓝细胞液中含有一种花色苷的化合物,在pH环境不同的条件下,会发生反应,呈现出不同颜色(见下表),用其绘画十分有趣。
pH
1
3
5
7
9
11
13
颜色
红
紫红
浅紫
紫
蓝
绿
黄
合成:近代有机化学蓬勃发展,涌现出了大量合成颜料。但据记载早在公元四世纪,人类就掌握了合成颜料——铅白的加工方法。将铅条堆放在醋和发酵物上,置于密闭空间内,利用发酵产生的热量和二氧化碳,最终生成铅白。
随着科技的发展,一定会有更多靓丽的颜色点缀我们的生活。
依据文章内容回答下列问题。
(1)写出一种来自天然矿物的颜料______。
(2)千里江山图历经千年,颜色依然分明,说明所用矿石颜料化学性质______(填“稳定”或“不稳定”)。
(3)向稀盐酸中加入紫甘蓝汁液,可能呈现的颜色是______(填“红色”或“蓝色”)。
(4)公元四世纪,人类使用铅条(Pb)与氧气、水和二氧化碳发生反应,最终获得了铅白[Pb3(OH)4CO3]。铅白由______种元素组成。
(5)下列说法正确的是______(填字母序号)。A.颜料的命名多与来源有关 B.矿物颜料取之不尽、用之不竭
C.新颜料的出现与科技发展有关 D.铅白可能具有毒性
参考答案:
1. 2NaOH 过滤
【详解】(1)该反应符合质量手恒定律,反应前后各元素的原子个数不变,反应物比生成物多2个钠原子、2个氧原子和2个氢原子,补全化学方程式:4Ag+2NaClO+H2O====2AgCl+Ag2O+2NaOH;
(2)操作Ⅱ将固体与体液分离的名称是:过滤。
2. +4 Na2SiO3+2HCl=2NaCl+H2SiO3↓ 洗去H2SiO3沉淀表面残留的滤液
【详解】(1)解:设硅酸钠(Na2SiO3)中硅元素的化合价为x,则(+1)×2+x+(-2)×3=0,x=+4;
(2)酸化池中硅酸钠与稀盐酸发生反应产生氯化钠和硅酸沉淀的化学方程式为Na2SiO3+2HCl=2NaCl+H2SiO3↓。
(3)上述流程中,洗涤槽的作用是:洗去H2SiO3沉淀表面残留的滤液,得到纯净的硅酸产品。
3. +4 CO2 Na2SO3
【详解】(1)SO2中氧元素的化合价为-2,根据化合物中各元素化合价的代数和为零,S元素的化合价为+4。
(2)反应前有2Na、C、8O、2S、2H,反应后(X除外)有2Na、6O、2S、2H,根据化学反应前后各种原子个数相等,生成物中还应含1个C、2个O,故过程Ⅰ中发生主要反应的化学方程式为:Na2CO3+2SO2+H2O=2NaHSO3+CO2。
(3)因为溶液X经过结晶得到Na2SO3固体,则溶液X中一定含有的溶质是Na2SO3。
4. 使反应物充分接触,充分反应 CaCO3 CO2
【详解】(1)反应器1中先加入一定量水。气体从底部缓慢通入的原因是:使反应物充分接触,充分反应;
(2)反应器2中,氯化钙和碳酸铵反应生成氯化铵和碳酸钙,该反应的化学方程式为:;
(3)氯化钙和碳酸铵反应生成氯化铵和碳酸钙,碳酸钙难溶于水,故过滤器中分离出的固体是CaCO3;
(4)由图可知,二氧化碳既是反应物。又是生成物,可以循环利用。
5.(1)生成物中含有氢、氧元素
(2)+4##+4价
(3)NaCl##氯化钠
【详解】(1)根据质量守恒定律可知反应前后元素种类不变,由反应后生成的两种物质化学式是,反应后元素是钠元素、氢元素、氧元素和氯元素,而反应前氯化钠只含钠元素和氯元素,故反应物还有水反应,故填:生成物中含有氢、氧元素;
(2)化合物中化合价代数和为0,设氯元素化合价为,,故填:+4或+4价;
(3)能循环使用的物质在流程中既是反应物又是生成物,故由题意判断上述流程中可循环利用的物质是氯化钠,故填:氯化钠或。
6.(1)增大接触面积,使反应更充分
(2)
(3)除去水
【详解】(1)吸收塔中碳酸钠溶液以雾状喷洒是为了增大接触面积,使反应更充分;
(2)根据流程可知,亚硫酸氢钠和氢氧化钠反应生成亚硫酸钠和水,化学方程式为:;
(3)反应是在溶液中进行的,故要得到亚硫酸钠固体,则应在干燥器中除去水,故填:除去水。
7. 其他条件相同时,随着氯化钠溶液浓度从1%到6%,有效氯含量先增大后减小 探究改变钛电极间距是否影响该实验 20 1-4和2-1 生成可燃性气体氢气,遇明火易爆炸 AD
【详解】1)由实验1可知,有效氯含量随氯化钠溶液浓度变化的规律是:他条件相同时,随着氯化钠溶液浓度从1%到6%,有效氯含量先增大后减小,4% 时最大;
(2)设计实验2-1、2-4、2-5中钛电极距离不同的目的是:探究改变钛电极间距是否影响该实验;
(3)实验2-2中,电压属于控制定量,与其他实验电压相等,x=20。
(4)能证明电压对有效氯含量有影响的实验是:1-4和2-1中电压分别是10V和20V,其他条件都相同,但有效氯含量不同;
(5)实验过程需在通风处进行并严禁烟火,原因是:生成的氢气具有可燃性,在空气中达到一定浓度,遇明火易爆炸;
(6)84消毒液对皮肤和口腔黏膜具有腐蚀性和刺激性。一般市售84消毒液有效氯含量为50g/L,根据使用需要加水稀释成0.2g/L、0.5g/L、1g/L。
结合本实验,下列分析正确的是:
A、84消毒液有刺激性气味,且具有腐蚀性,使用时建议佩戴防护口罩与手套;故选项正确;
B、本实验中,温度为20℃时,有效氯含量最高;故选项错误;
C、实验2-1中,有效氯含量为8.4g/L,没有达到市售84消毒液标准(有效氯含量50g/L);故选项错误;
D、本实验制备的次氯酸钠溶液的有效氯含量为实验1-1(3.5g/L)依然大于实用最高有效氯含量(1g/L),需稀释后使用;故选项正确;
故选:AD。
8. 10 20℃时,排除水对本实验的影响 ②③④ 相同浓度时,温度越高,Na2CO3溶液去油污效果越好 相同温度时,浓度越大,Na2CO3溶液的pH越大,碱性越强,去油污效果越好 在20℃至80℃范围内,随温度升高,10%Na2CO3溶液的pH先升高后减小 ABC
【详解】(1)配制100g 10% Na2CO3溶液,需要称量Na2CO3固体的质量为:100g×10%=10g。
(2)设计实验①的目的是:对照实验,20℃时,排除水对本实验的影响。
(3)对比实验必须控制变量,变量唯一性,所以欲探究“浓度对Na2CO3溶液去油污效果的影响”,除了浓度不同,其它因素都应相同,故需对比的实验是②③④。
(4)④⑥⑧只是温度不同,其它条件相同,所以对比实验④⑥⑧可得到的结论是相同浓度时,温度越高,Na2CO3溶液去油污效果越好。
(5)结合第1组实验和图1数据分析,欲得出“溶液的碱性越强,Na2CO3溶液去油污效果越好”的依据是相同温度时,浓度越大,Na2CO3溶液的pH越大,碱性越强,去油污效果越好。
(6)由图2可知,10% Na2CO3溶液的pH与温度的关系是在20℃至80℃范围内,随温度升高,10%Na2CO3溶液的pH先升高后减小。
(7)A 、由实验④⑥⑧可知,热Na2CO3溶液去油污效果更好可能与“温度升高,水的去油污能力增强”有关,此选项正确;
B、在20℃至50℃范围内,随温度升高,10%Na2CO3溶液的pH增大,即碱性增强,所以热Na2CO3溶液去油污效果更好可能与“温度升高,溶液碱性增强”有关,此选项正确;
C、由图2可知,10% Na2CO3溶液在不同温度时,pH可能相同,此选项正确;
D、由图2可知,溶液碱性增强,pH不一定增大,此选项错误。
故选ABC。
9.解:设产生氧气的质量为x
解得x=96 g。
答:产生氧气的质量为96 g。
【详解】见答案。
10.设:消耗二氧化碳的质量为x。
x=88 g
答:消耗二氧化碳的质量为88g。
【分析】利用化学方程式姐姐反应中物质的质量关系,可由反应的氨气质量计算需要二氧化碳的质量。
【详解】见答案。
11. 蛋白质、维生素(其他合理答案均可) 贫血 藜麦营养成分丰富且比例均衡 磷肥40千克/公顷,钾肥80千克/公顷 AC
【详解】(1)藜麦的蛋白质含量与牛肉相当,且品质不亚于肉源蛋白与奶源蛋白,同时它还含有种类丰富的矿物元素,以及多种人体所需要的维生素;藜麦所含人体必需的营养素有:蛋白质、维生素。
(2)藜麦中的铁元素可以预防贫血。
(3)藜麦被列为“全球十大健康营养食品之一”的原因是:藜麦营养成分丰富且比例均衡,有助于身体健康。
(4)由图2可知,磷肥、钾肥最佳的施用量为:磷肥40千克/公顷,钾肥80千克/公顷,因为该肥料培育出的穗粒最饱满,质量最大;
(5)下列说法正确的是:
A、藜麦营养成分丰富且比例均衡,适合减肥人群食用;故选项正确;
B、藜麦中含有丰富的维生素,胆固醇高的人,依然适合食用藜麦;故选项错误;
C、由图1可知:藜麦中,钙、铁、锌的含量均高于小麦和稻米;故选项正确;
D、种植藜麦时,磷肥40千克/公顷,钾肥80千克/公顷,产量最高;故选项错误;
故选:AC。
12. AB 强度高、熔点低、铸造性好、耐磨、耐腐蚀(答一条即可) H2O 4:1 ABD
【详解】(1)青铜是铜的合金,青铜和金属于金属材料。
故选AB;
(2)青铜是金属冶铸史上最早出现的合金,与纯铜相比,其强度高、熔点低、铸造性好、耐磨且耐腐蚀;
(3)根据质量守恒定律,化学反应前后,元素的种类不变,反应物中含Cu、O、H、C,生成物中也应含Cu、O、H、C,故铜生锈的过程是铜与空气中的二氧化碳、氧气和H2O发生化学反应的过程;
(4)依据图2可知,用于生产戈戟的青铜器中,铜和锡的比例为:80%:20%=4:1;
(5)A、青铜器中铜锡比例不同,所得合金的性能也不同,说法正确,符合题意;
B、人类大规模使用金属的先后顺序与金属活动性有关,金属活动性越强,使用的时间越晚,符合题意;
C、金属资源有限,应保护金属资源,不符合题意;
D、将废旧金属回收利用可节约金属资源,符合题意。
故选ABD。
13.(1)朱砂、赭石、石青、孔雀石等
(2)稳定
(3)红色
(4)四##4
(5)ACD
【详解】(1)由题干信息可知,常见的矿石颜料朱砂、赭石、石青、孔雀石、紫云、蓝闪石、雄黄等;
(2)千里江山图历经千年,颜色依然分明,说明所用矿石颜料化学性质稳定,很难与其它物质反应;
(3)稀盐酸为强酸,显酸性,由表可知,向稀盐酸中加入紫甘蓝汁液,可能呈现的颜色是红色;
(4)由化学式可知,铅白由Pb、O、H、C四种元素组成;
(5)A、由题干信息可知,颜料的命名多与来源有关,如从雌胭脂虫体内提取的颜料名称为胭脂虫红,符合题意;
B、矿物颜料是有限的,应合理使用,不符合题意;
C、由题干信息可知,新颜料的出现与科技发展有关,随着科技的发展,一定会有更多靓丽的颜色点缀我们的生活,符合题意;
D、铅白中含铅元素,故铅白可能具有毒性,符合题意。
故选ACD。












