
广西梧州市2020-2022三年中考化学真题知识点分类汇编1-几种化学反应(含解析)
展开广西梧州市2020-2022三年中考化学真题知识点分类汇编1-几种化学反应(含解析)
一、单选题
1.(2022·广西梧州·统考中考真题)下列化学反应方程式与描述相符,且书写完全正确的是
A.用稀盐酸除铁锈:FeO+ 2HCl=FeCl2+H2O
B.红磷在氧气中燃烧: P+O2P2O5
C.石灰石与二氧化硅高温反应: CaCO3+ SiO2CaSiO3+ CO2↑
D.工业上用电解法冶炼铝:2Al2O3=4Al+3O2
2.(2022·广西梧州·统考中考真题)我国湿法炼铜的工艺在宋、元时期已相当成熟。小军同学在实验室模拟湿法炼铜,他取48.0g铁片放入一定质量的氯化铜溶液中,反应一段时间后, 得到50.0g固体。则所得固体中铁的质量分数为
A.28.0% B.68.0% C.92.5% D.96.0%
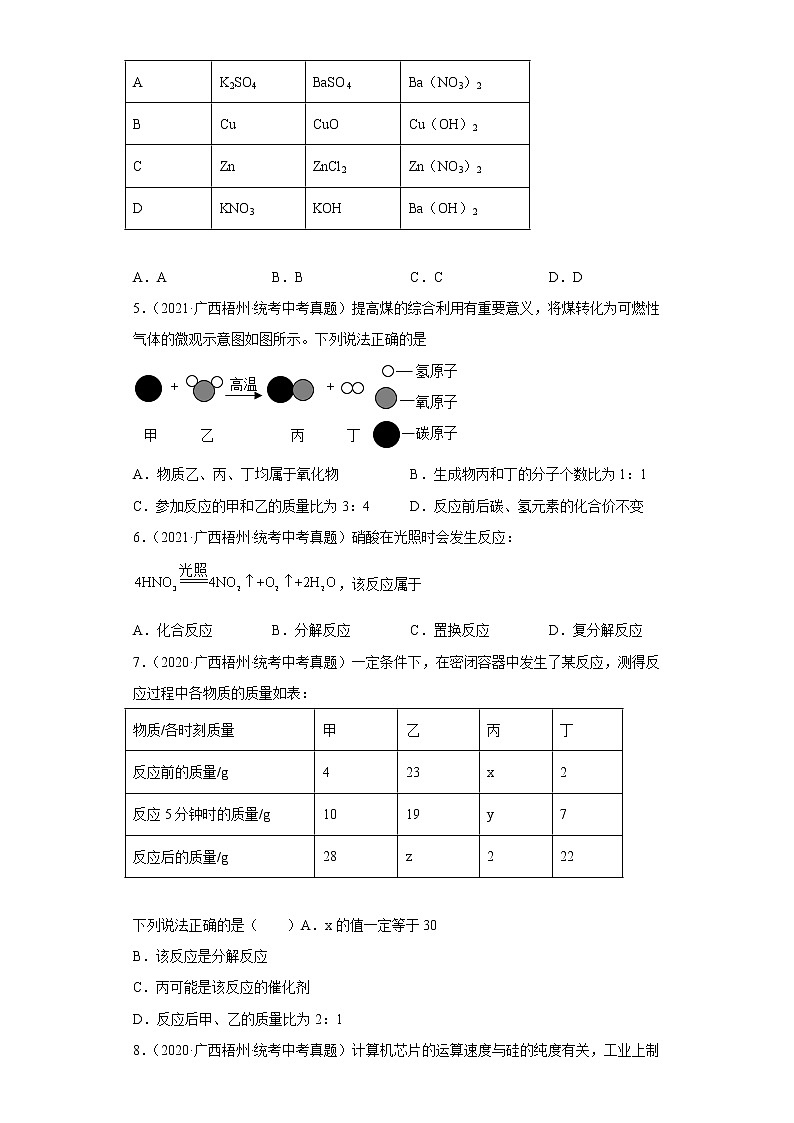
3.(2021·广西梧州·统考中考真题)一定条件下,甲、乙、丙、丁四种物质在密闭容器中发生反应,测得反应前后各物质的质量如图3所示,图中x、y分别表示乙和丙的质量。下列说法错误的是
A.反应后甲的质量分数是8% B.x的取值范围:0≤x≤40
C.y≤30时,生成物只有一种 D.参加反应的甲与丁的质量比为2:1
4.(2021·广西梧州·统考中考真题)“X→Y→Z”物质间转化,均可通过一步反应实现的是
物质 选项 | X | Y | Z |
A | K2SO4 | BaSO4 | Ba(NO3)2 |
B | Cu | CuO | Cu(OH)2 |
C | Zn | ZnCl2 | Zn(NO3)2 |
D | KNO3 | KOH | Ba(OH)2 |
A.A B.B C.C D.D
5.(2021·广西梧州·统考中考真题)提高煤的综合利用有重要意义,将煤转化为可燃性气体的微观示意图如图所示。下列说法正确的是
A.物质乙、丙、丁均属于氧化物 B.生成物丙和丁的分子个数比为1:1
C.参加反应的甲和乙的质量比为3:4 D.反应前后碳、氢元素的化合价不变
6.(2021·广西梧州·统考中考真题)硝酸在光照时会发生反应:,该反应属于
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
7.(2020·广西梧州·统考中考真题)一定条件下,在密闭容器中发生了某反应,测得反应过程中各物质的质量如表:
物质/各时刻质量 | 甲 | 乙 | 丙 | 丁 |
反应前的质量/g | 4 | 23 | x | 2 |
反应5分钟时的质量/g | 10 | 19 | y | 7 |
反应后的质量/g | 28 | z | 2 | 22 |
下列说法正确的是( )A.x的值一定等于30
B.该反应是分解反应
C.丙可能是该反应的催化剂
D.反应后甲、乙的质量比为2:1
8.(2020·广西梧州·统考中考真题)计算机芯片的运算速度与硅的纯度有关,工业上制取高纯硅的化学方程式为SiCl4+2H2Si+4HCl。该反应属于( )
A.复分解反应 B.分解反应 C.化合反应 D.置换反应
9.(2020·广西梧州·统考中考真题)向滴有酚酞的氢氧化钠溶液中,逐滴滴加稀盐酸至过量,下列有关说法正确的是( )
A.溶液由无色变为红色
B.溶液的pH先升高,后降低
C.氢氧化钠与盐酸的反应不是复分解反应
D.氯化钠的质量逐渐增加,最后保持不变
二、填空题
10.(2022·广西梧州·统考中考真题)近几年,我国在科学技术领域取得了举世瞩目的成就。
(1)①2022年北京冬奥会,国家速滑馆选用了二氧化碳跨临界制冷系统制冰。水结成冰的过程中,需要____(填“吸收”或“放出”)能量。
②火炬“飞扬”采用高压储氢工艺贮存氢气,储氢过程中氢分子间的间隔________(填“增大”或“减小”)。
(2)2022年6月5日,我国神舟十四号载人飞船发射成功。
①在发射现场看到的大量红棕色的烟,是引燃后产生的一氧化氮气体遇到氧气反应生成的二氧化氮,该反应的化学方程式为________。
②空间站的太阳能板采用砷化镓材料,光电转化效率较高。砷元素(As)最外层电子数是5,砷化镓中镓(Ga)元素显+3价,该化合物的化学式为_________。
(3)嫦娥五号在月球上升起的五星红旗是由高性能芳纶纤[(C14H10O2N2)n]特制而成,芳纶纤维中碳元素与氮元素的质量最简比为________。
11.(2021·广西梧州·统考中考真题)化学在科技、生活和社会发展中都起到了重要的作用。
(1)2021年3月全国两会期间,“碳中和”成为热词。我国科学家研制了全球首套捕集二氧化碳合成甲醇(CH3OH)的装置,有利于实现“碳中和”。
①甲醇分子中C、H、O元素的质量比为______。
②请你说出日常生活中的一种低碳行为:______。
(2)2021年5月22日,“祝融号”火星车成功登陆火星表面,该车的车身使用了新型铝基碳化硅复合材料。
①工业上冶炼铝的化学反应方程式为______。
②碳化硅能与熔融的氢氧化钠发生反应:,其中X的化学式为______,SiC中碳元素的化合价为______。
三、流程题
12.(2021·广西梧州·统考中考真题)1926年,我国化工专家侯德榜创造出的“侯氏制碱法”,结束了由美、英、法等国垄断世界纯碱市场的时代。其基本工业流程如下:
已知:常温下,氨气的溶解度很大,CO2的溶解度很小。回答下列问题:
(1)纯碱的化学式为______。
(2)“侯氏制碱法”的反应温度一般控制为30-35°C,因为在此温度时, NaHCO3的溶解度较______(填“大”或“小”)。
(3)若向饱和食盐水中先通入CO2,会导致 NaHCO3产量减少,原因是______。
(4)写出步骤①、②发生的总反应方程式______。
(5)“侯氏制碱法”中能循环利用的物质有NaCl、H2O和______。
四、科学探究题
13.(2020·广西梧州·统考中考真题)酒精和含氯消毒液在抗击新冠肺炎疫情中发挥了重要作用。体积分数为75%的酒精可直接用于消毒,酒精属于______(填“无机物”或“有机物”)。大面积喷洒酒精易引起燃爆,这是因为酒精具有挥发性和______,故应小面积擦拭消毒。84消毒液是我国科研人员于1984年研制的一种含氯消毒液。某品牌84消毒液的使用说明如图1,梧州市某中学化学兴趣小组对如何科学使用84消毒液进行了探究。
【查阅资料】
(1)84消毒液的主要成分是次氯酸钠(NaClO)。
(2)次氯酸(HClO)的漂白、消毒效果都强于次氯酸钠,但前者不稳定,保存和运输不方便。
(3)氯气(Cl2)是一种黄绿色的气体,有毒。
(4)某些洗涤剂含有盐酸。
【探究1】小吴将少量84消毒液滴在pH试纸上,发现pH试纸先变蓝后褪色,说明84消毒液显______性,并有漂白性,所以使用时应尽量不接触皮肤和眼睛。
【探究2】根据“使用说明2”同学们猜测,在浸泡过程中,次氯酸钠与空气中的某种物质发生了反应。为了证实这一猜测,小周进行了以下实验:
操作 | 现象 | ||
将一块有色布条分成3等份,放入三个装有同浓度同体积的84消毒液的烧杯中 | 向烧杯1中通入O2 | 布条褪色较慢 | |
向烧杯2中通入N2 | 布条褪色较慢 | ||
向烧杯3中通入______ | 布条迅速褪色 | ||
老师提示,烧杯3中发生了反应,生成碳酸氢钠和一种漂白、消毒效果更强的物质。写出该反应的化学方程式______,所以使用84消毒液时,浸泡30分钟效果更好。
【探究3】在老师的指导下,小施在通风橱中进行如图2所示实验:滴入盐酸后,有黄绿色气体产生。请结合该实验现象。写出锥形瓶中反应的化学方程式,并说明84消毒液不能与其他洗涤剂混用的原因______。
【拓展探究】
漂白粉的漂白、消毒原理与84消毒液相似。已知漂白粉可溶于水,有效成分是次氯酸钙,保存不当易转化为碳酸钙。请设计一个简单的实验,判断漂白粉是否变质:______。
五、计算题
14.(2020·广西梧州·统考中考真题)已知某样品中含有NaOH和Na2CO3。为了测定该样品中NaOH的质量分数,某同学取50.0g样品于锥形瓶中,加水全部溶解后,逐滴加入稀盐酸至过量,测得生成气体的质量与所加稀盐酸的质量关系如图所示,请计算:
(1)HCl的相对分子质量为______。
(2)该样品中NaOH的质量分数。(精确到0.1%)
参考答案:
1.C
【详解】A、用稀盐酸除铁锈是氧化铁与盐酸反应生成氯化铁和水,该反应的化学方程式为,故A项错误;
B、红磷在空气中燃烧生成五氧化二磷,该反应的化学方程式为,故B项错误;
C、石灰石与二氧化硅高温反应生成硅酸钙和二氧化碳,该反应的化学方程式为 ,故C项正确;
D、氧化铝在通电条件下生成铝和氧气,该反应的化学方程式为,故D项错误;
故选C。
2.B
【详解】由方程式可知铁和铜的质量关系为56~64,设:参加反应的铁的质量为a,则生成铜的质量为,那么有,则a=14g,所以所得固体中铁的质量分数为。
故选:B。
3.B
【详解】A、反应后甲的质量为10g,质量分数为,故选项正确;
B、由质量守恒定律可知,反应前后物质的总质量不变,即30+40+30+25=10+15+x+y,x+y=100,乙为生成物地,反应后质量大于大于40,即x的值大于40,y的值最小为0 ,故x的最大值为100,则x的取值范围为0≤ x≤100,故选项错误;
C、y≤30时,则丙不参加反应,或属于反应物,则只有乙是生成物,故选项正确;
D、根据图可知,参加反应的甲的质量为20g,参加反应的乙的质量为10g,参加反应的甲与丁的质量比为2:1,故选项正确。
故选:B。
4.C
【详解】A、硫酸钾和氯化钡反应生成硫酸钡和氯化钾,硫酸钡难溶于水和酸,不能转化为硝酸钡,不符合题意;
B、铜与氧气在加热的条件下反应生成氧化铜,氧化铜不能一步转化为氢氧化铜,不符合题意;
C、锌与稀盐酸反应生成氯化锌和氢气,氯化锌和硝酸银反应生成硝酸锌和氯化银,符合题意;
D、假设硝酸钾能转化为氢氧化钾,氢氧化钾溶于水,硝酸盐均溶于水,不满足复分解反应的条件,同理,假设氢氧化钾能转化为氢氧化钡,氢氧化钡溶于水,钾盐均溶于水,不满足复分解反应的条件,均不能一步转化,不符合题意。
故选C。
5.B
【分析】由图可知,该反应为碳和水蒸气在高温下反应生成一氧化碳和氢气,该反应的化学方程式为:。
【详解】A、物质乙为水,水是由H、O元素组成的化合物,属于氧化物;丙为一氧化碳,一氧化碳是由C、O元素组成的化合物,属于氧化物,丁为氢气,氢气是由氢元素组成的纯净物,属于单质,不符合题意;
B、由化学方程式可知,生成物丙和丁的分子个数比为:1:1,符合题意;
C、参加反应的甲和乙的质量比为:12:18=2:3,不符合题意;
D、化学反应前后,碳元素由游离态转化为化合态,氢元素由化合态转化为游离态,碳、氢元素的化合价都发生了改变,不符合题意。
故选B。
6.B
【详解】根据,可知该反应 是“一变多”,属于分解反应。
故选:B。
【点睛】本考点考查了基本反应类型的判断和质量守恒定律,要牢记四个基本反应类型的概念,并会理解应用。本考点基础性比较强,主要出现在选择题和填空题中。
7.A
【详解】A、由表中数据分析可知,反应前后甲的质量增加,故是生成物;同理可以确定乙是反应物,至反应5分钟时,生成的甲和参加反应的乙的质量比为(10g﹣4g):(23g﹣19g)=3:2,则完全反应后参加反应的乙的质量为(28g﹣4g)×=16g,则z的数值为23﹣16=7。则x的数值为28+7+2+22﹣4﹣23﹣2=30,故选项说法正确。
B、反应后质量增加的属于生成物,反应后质量减少的属于反应物,该反应的反应物为乙和丙,生成物是甲和丁,不符合“一变多”的形式,不属于分解反应,故选项说法错误。
C、反应前后丙的质量减少,是反应物,故选项说法错误。
D、反应后甲、乙的质量比为28g:7g=4:1,故选项说法错误。
故选:A。
8.D
【详解】根据反应的化学方程式可知,该反应符合一种单质和一种化合物反应生成另一种单质和另一种化合物,属于置换反应。
故选D。
9.D
【详解】A、氢氧化钠溶液显碱性,能使酚酞试液变红色,逐滴滴加稀盐酸至过量,溶液由红色变无色,该选项说法不正确;
B、加入稀盐酸后,溶液碱性减弱,直至显酸性,pH降低,该选项说法不正确;
C、氢氧化钠和盐酸反应生成氯化钠和水,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,是复分解反应,该选项说法不正确;
D、随着反应进行,氯化钠质量增大,完全反应后不再变化,该选项说法正确。
故选:D。
10.(1) 放出 减小
(2) 2NO+O2=2NO2 GaAs
(3)6:1
【解析】(1)
①水结成冰是一个放热的过程中;
②火炬“飞扬”采用高压储氢工艺贮存氢气,储氢过程中氢分子间的间隔会减小;
故填:①放出;②减小
(2)
①一氧化氮气体能与氧气反应生成的二氧化氮,该反应的化学方程式为:2NO+O2=2NO2;
②镓原子的最外层电子数为3,在化学反应中易失去3个电子而形成带3个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+3价;砷的元素符号为As,在砷化镓中砷显-3价,则砷化镓的化学式为GaAs;
故填:①2NO+O2=2NO2;②GaAs;
(3)
芳纶纤[(C14H10O2N2)n]中,碳元素和氮元素的质量之比为(12×14n):(14×2n)=6:1;
故填:6:1
11. 3:1:4 骑自行车上学 Na2SiO3 -4
【详解】(1)①甲醇分子中C、H、O元素的质量比为:12:4:16=3:1:4;
②日常生活中的低碳行为,如:骑自行车上学,乘坐公共交通工具出行;
(2)①工业上通常用电解氧化铝生成铝和氧气,该反应的化学方程式为:;
②根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Si、C、Na、O、H的个数分别是1、1、2、6、2,生成物中含Si、C、Na、O、H的个数分别是0、1、0、3、2,故生成物中还应含1个Si、2个Na、3个O,故X的化学式为:Na2SiO3;
碳化硅中硅元素显+4价,设碳元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:x+(+4)=0,x=-4。
12. Na2CO3 小 食盐水显中性,二氧化碳在中性溶液中,溶解度较小 CO2
【详解】(1)纯碱是碳酸钠的俗称,化学式为:Na2CO3;
(2)“侯氏制碱法”的反应温度一般控制为30-35°C,因为在此温度时, NaHCO3的溶解度较小,碳酸氢钠可以结晶析出;
(3)若向饱和食盐水中先通入CO2,会导致 NaHCO3产量减少,原因是:饱和食盐水显中性,氯化钠在中性溶液中溶解的较少;
(4)步骤①、②发生的总反应为氯化钠和氨气、二氧化碳、水反应生成碳酸氢钠和氯化铵,该反应的化学方程式为:;
(5)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,故二氧化碳既是反应物又是生成物,可以循环利用,故填:CO2。
13. 有机物 可燃性 碱 二氧化碳 NaClO+H2O+CO2=NaHCO3+HClO 次氯酸钠和盐酸反应生成氯化钠、水和氯气,反应的化学方程式:NaClO+2HCl=NaCl+H2O+Cl2↑,因为次氯酸钠能和盐酸反应生成氯化钠、水和氯气,因此84消毒液不能与其他洗涤剂混用 实验步骤:取少量漂白粉于烧杯中,加入足量水,搅拌;实验现象:漂白粉不能完全溶解;实验结论:漂白粉变质
【详解】①酒精是含有碳元素的化合物,是有机物。
②大面积喷洒酒精易引起燃爆,这是因为酒精具有挥发性和可燃性,故应小面积擦拭消毒。
③次氯酸(HClO)的漂白、消毒效果都强于次氯酸钠。将少量84消毒液滴在pH试纸上,发现pH试纸先变蓝后褪色,说明84消毒液显碱性,并有漂白性。
④烧杯1、2中布条分别通入O2、N2褪色较慢,那么有可能是空气中二氧化碳的作用,故向烧杯3中通入二氧化碳观察现象。
⑤由题干可知:次氯酸(HClO)的漂白、消毒效果都强于次氯酸钠;老师提示,烧杯3中发生了反应,生成碳酸氢钠和一种漂白、消毒效果更强的物质。那么反应应该为次氯酸钠和水、二氧化碳反应生成碳酸氢钠和次氯酸,反应的化学方程式:NaClO+H2O+CO2=NaHCO3+HClO。
⑥由题干可知:氯气(Cl2)是一种黄绿色的气体;反应前后元素种类不变。那么次氯酸钠和盐酸反应会生成氯化钠、水和氯气,反应的化学方程式:NaClO+2HCl=NaCl+H2O+Cl2↑;因为次氯酸钠能和盐酸反应生成氯化钠、水和氯气,因此84消毒液不能与其他洗涤剂混用。
⑦已知漂白粉可溶于水,碳酸钙难溶于水;故实验可以设计为
实验步骤:取少量漂白粉于烧杯中,加入足量水,搅拌;
实验现象:漂白粉不能完全溶解;
实验结论:漂白粉变质。
14.(1)36.5;
(2)设样品中碳酸钠的质量为x
x=21.2g;
所以该样品中NaOH的质量分数为:。
【详解】(1)HCl的相对分子质量为1+35.5=36.5。
(2)见答案。
2020-2022广西梧州市中考化学三年真题知识点分类汇编9-盐和化肥(含解析): 这是一份2020-2022广西梧州市中考化学三年真题知识点分类汇编9-盐和化肥(含解析),共25页。试卷主要包含了单选题,填空题,推断题,流程题,科学探究题,计算题等内容,欢迎下载使用。
2020-2022广西梧州市中考化学三年真题知识点分类汇编8-酸和碱、中和反应(含解析): 这是一份2020-2022广西梧州市中考化学三年真题知识点分类汇编8-酸和碱、中和反应(含解析),共15页。试卷主要包含了单选题,流程题,科学探究题,计算题等内容,欢迎下载使用。
2020-2022广西梧州市中考化学三年真题知识点分类汇编7-水、溶液(含解析): 这是一份2020-2022广西梧州市中考化学三年真题知识点分类汇编7-水、溶液(含解析),共12页。试卷主要包含了单选题,填空题,流程题,计算题等内容,欢迎下载使用。












