




高考化学一轮复习精讲精练第14讲 富集在海水中的元素——卤素(精练)(2份打包,解析版+原卷版,可预览)
展开1.(江西省井冈山中学模拟)化学来源于生活,也服务于生活。下列有关生活中的化学知识叙述正确的是( )
A.氯气和活性炭均可作为漂白剂,若同时使用,漂白效果会明显加强
B.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
C.测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH,测定结果无影响
D.洁厕灵不能与84消毒液混用,原因是两种溶液混合产生的HClO易分解
2.(湖南常德高三调研)下列说法正确的是( )
①氯气的性质活泼,它与氢气混合后立即发生爆炸
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收
③新制氯水的氧化性强于久置氯水的
④检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液中
⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水中
A.①②③ B.②③④
C.③ D.③⑤
3.(北京房山高三模拟)Cl2是一种重要的工业原料,液氯储存区贴有的说明卡如下:
包装 | 钢瓶 |
储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
下列解释事实的方程式不正确的是( )
A.电解饱和食盐水制取Cl2:2Cl-+2H2O2OH-+H2↑+Cl2↑
B.氯气用于自来水消毒:Cl2+H2O2H++Cl-+ClO-
C.浓氨水检验泄漏的氯气,产生白烟:8NH3+3Cl2===6NH4Cl+N2
D.氯气“泄漏处理”中NaHSO3溶液的作用:HSO+Cl2+H2O===SO+3H++2Cl-
4.(山东省淄博市四中模拟)下列有关卤素的说法错误的是( )
A.从HF、HCl、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规律
B.HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强
C.淀粉碘化钾溶液在空气中变蓝:4I-+O2+2H2O===2I2+4OH-
D.碘在碘化钾溶液中的溶解度大于在纯水中的溶解度
5.(吉林通化高三调研)氯胺(NH2Cl)是一种长效缓释有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的4~5倍。下列有关氯胺的说法一定不正确的是( )
A.氯胺的水解产物为NH2OH(羟氨)和HCl
B.氯胺的电子式为
C.氯胺中氯元素的化合价为+1价
D.氯胺的消毒原理与漂白粉相似
6.(山东东营模拟)锡为ⅣA族元素,四碘化锡是常用的有机合成试剂(SnI4,熔点144.5 ℃,沸点364.5 ℃,易水解)。实验室以过量锡箔为原料通过反应Sn+2I2SnI4制备SnI4。下列说法错误的是( )
A.加入碎瓷片的目的是防止暴沸
B.SnI4可溶于CCl4中
C.装置Ⅰ中a为冷凝水进水口
D.装置Ⅱ的主要作用是吸收挥发的I2
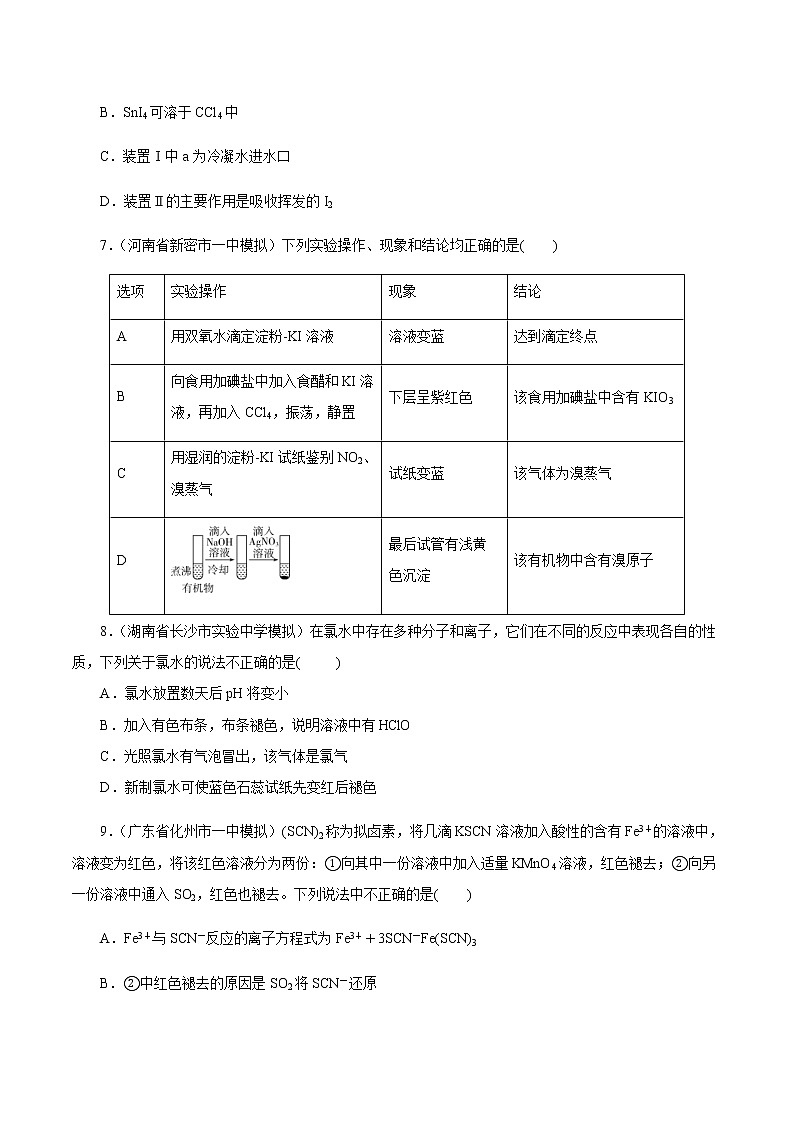
7.(河南省新密市一中模拟)下列实验操作、现象和结论均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | 用双氧水滴定淀粉KI溶液 | 溶液变蓝 | 达到滴定终点 |
B | 向食用加碘盐中加入食醋和KI溶液,再加入CCl4,振荡,静置 | 下层呈紫红色 | 该食用加碘盐中含有KIO3 |
C | 用湿润的淀粉-KI试纸鉴别NO2、溴蒸气 | 试纸变蓝 | 该气体为溴蒸气 |
D | 最后试管有浅黄色沉淀 | 该有机物中含有溴原子 |
8.(湖南省长沙市实验中学模拟)在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质,下列关于氯水的说法不正确的是( )
A.氯水放置数天后pH将变小
B.加入有色布条,布条褪色,说明溶液中有HClO
C.光照氯水有气泡冒出,该气体是氯气
D.新制氯水可使蓝色石蕊试纸先变红后褪色
9.(广东省化州市一中模拟)(SCN)2称为拟卤素,将几滴KSCN溶液加入酸性的含有Fe3+的溶液中,溶液变为红色,将该红色溶液分为两份:①向其中一份溶液中加入适量KMnO4溶液,红色褪去;②向另一份溶液中通入SO2,红色也褪去。下列说法中不正确的是( )
A.Fe3+与SCN-反应的离子方程式为Fe3++3SCN-Fe(SCN)3
B.②中红色褪去的原因是SO2将SCN-还原
C.①中现象说明SCN-与Cl-相似,有还原性
D.SCN-在适当条件下可被氧化剂氧化为(SCN)2
10.(山东青岛高三调研)ClO2和NaClO2均具有漂白性,工业上由ClO2气体制取NaClO2固体的工艺流程如图所示,下列说法错误的是( )
A.通入的空气可将发生器中产生的ClO2全部驱赶到吸收器中
B.吸收器中生成NaClO2的离子方程式为2ClO2+H2O2===2ClO+2H++O2↑
C.步骤a的操作包括过滤、洗涤和干燥
D.工业上将ClO2气体制成NaClO2固体,其主要目的是便于贮存和运输
11.(福建省三明市第一中学模拟)在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质,下列实验现象和结论一 致且正确的是
A.加入有色布条,褪色,说明溶液中有 Cl2 存在
B.溶液呈现黄绿色,且有刺激性气味,说明有 Cl2 存在
C.先加入盐酸酸化,再加入硝酸银溶液产生白色沉淀,说明有 Cl-存在
D.新制氯水放置数天后酸性将减弱
12.(河南省郑州市第一中学质检)下列说法中不正确的是( )
A.钠在空气中燃烧生成淡黄色的过氧化钠
B.过氧化钠与水反应时可放出氧气
C.氯气与铁反应生成氯化铁
D.久置的氯水,因氯气几乎完全挥发掉,剩下的全是水
13.(江苏省宿迁市模拟)下列有关物质的用途说法不正确的是
A.Si 可用于制造光导纤维 B.钠、钾合金可用于原子反应堆作热交换剂
C.FeCl3 溶液可作为铜质电路板蚀刻剂 D.漂白粉可用于自来水杀菌消毒
14.( 陕西省丹凤中学模拟)某同学用下列装置制备并检验Cl2的性质。下列说法错误的是
A.Ⅰ图中:如果MnO2过量,浓盐酸就可全部被消耗
B.Ⅱ图中:溶液变蓝
C.Ⅲ图中:生成棕黄色的烟
D.Ⅳ图中:干燥的有色布条不褪色,湿润的有色布条褪色
15.(黑龙江省大庆铁人中学质检)下列关于氯及其化合物说法正确的是( )
A.氯气溶于水的离子方程式:Cl2+H2O2H++Cl-+ClO-
B.洁厕灵不能与“84”消毒液混用,原因是两种溶液混合产生的HClO易分解
C.漂白粉在空气中久置变质是因为漂白粉中的CaCl2与空气中的CO2反应生成CaCO3
D.氯气可以使湿润的有色布条褪色,实际起漂白作用的物质是次氯酸,而不是氯气
16.(陕西省宝鸡市渭滨中学模拟)已知高锰酸钾与浓盐酸在常温下反应能产生氯气。若用下图所示的实验装置来制备纯净、干燥的氯气,并实验其与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
A.①和②处 B.只有②处
C.②和③处 D.②、③、④处
17.(四川大学附属中学模拟)如图,A处通入Cl2,关闭B阀时,C中的湿润红色布条看不到明显变化;打开B阀后,C中的湿润红色布条逐渐褪色.则D瓶中盛放的是( )
A.浓盐酸 B.饱和NaCl溶液
C.浓硫酸 D.NaOH溶液
18.(重庆市凤鸣山中学模拟)溴化碘(IBr)的化学性质很像卤素的单质,它能与大多数金属、非金属化合生成卤化物,它也能与水发生以下反应:IBr+H2O=HBr+HIO,下列有关IBr的叙述中,不正确的是( )。
A.在很多反应中IBr是强氧化剂
B.IBr与水反应时既作氧化剂,又作还原剂
C.IBr与AgNO3溶液反应会生成AgBr沉淀
D.IBr与NaOH溶液反应时,生成NaBr和NaIO
19.(湖南省娄底市三中模拟)ICl(氯化碘)是红棕色液体,熔点为13.9 ℃,沸点为97.4 ℃,易水解,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组的同学拟用下列仪器制备氯化碘。回答下列问题:
(1)检查A装置气密性的方法为_____________________________________________。
(2)上述装置,按气流方向连接的顺序为____________(装置可重复使用),A装置中发生反应的离子方程式为_______________________________________________________。
(3)C装置的作用是_____________________________________________________。
(4)E装置中的物质反应时需放在水浴中,控制温度大约40 ℃,其目的是________________________________________________________________________。
(5)按上述连接好的装置进行实验,实验步骤如下:
①检查装置气密性后,装入药品
②打开分液漏斗活塞
③关闭分液漏斗活塞
④停止加热E装置,充分冷却
⑤水浴加热E装置
请按正确的顺序填入上述步骤的序号:_______________________________________。
(6)在A装置后可连接如图所示装置,当反应结束关闭分液漏斗活塞后,关闭K,该装置的作用是_________________________________________________________________。
(7)ICl和水反应的化学方程式为__________________________________________。
20.(广东省广州市三中模拟)溴和碘的提取方法有多种,试解决下列问题。
Ⅰ.全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65 mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一。其工艺流程如下:
(1)写出步骤③的离子方程式:______________________________________________。
(2)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃,温度过高或过低都不利于生产。实验室里蒸馏所用的主要仪器名称为______,为控制温度,最好采用的加热方式为________;溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离,分离仪器的名称是________________。
(3)溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通过________(填试剂名称)溶液,以除去氯气。
(4)步骤①中用硫酸酸化可提高Cl2的利用率,理由是____________________________。
(5)提取溴单质,采用蒸馏“溴水混合物Ⅱ”而不是蒸馏“溴水混合物Ⅰ”,请说明原因:________________________________________________________________________。
Ⅱ.实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为________________________;该操作将I2还原为I-的目的是________________________。
操作X的名称为________。
老师,您好!感谢您下载使用学科网资料。欢迎参加同步精品课堂用户调研,我们需要您的宝贵意见,以便更好地建设各类资源,为您提供更优质的服务。填写本问卷,您将获得学科网2储值或200学豆奖励。点击下方链接或者扫描二维码,即可参与调研,赢取奖励!(活动截止时间2020年11月30日)
https://www.wjx.cn/jq/87822727.aspx
高考化学一轮复习精讲精练第16讲 氮及其化合物(精练)(2份打包,解析版+原卷版,可预览): 这是一份高考化学一轮复习精讲精练第16讲 氮及其化合物(精练)(2份打包,解析版+原卷版,可预览),文件包含高考化学一轮复习精讲精练第16讲氮及其化合物精练解析版doc、高考化学一轮复习精讲精练第16讲氮及其化合物精练原卷版doc等2份试卷配套教学资源,其中试卷共24页, 欢迎下载使用。
高考化学一轮复习精讲精练第15讲 硫及其化合物(精练)(2份打包,解析版+原卷版,可预览): 这是一份高考化学一轮复习精讲精练第15讲 硫及其化合物(精练)(2份打包,解析版+原卷版,可预览),文件包含高考化学一轮复习精讲精练第15讲硫及其化合物精练解析版doc、高考化学一轮复习精讲精练第15讲硫及其化合物精练原卷版doc等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。
高考化学一轮复习精讲精练第10讲 钠及其重要化合物(精练)(2份打包,解析版+原卷版,可预览): 这是一份高考化学一轮复习精讲精练第10讲 钠及其重要化合物(精练)(2份打包,解析版+原卷版,可预览),文件包含高考化学一轮复习精讲精练第10讲钠及其重要化合物精练解析版doc、高考化学一轮复习精讲精练第10讲钠及其重要化合物精练原卷版doc等2份试卷配套教学资源,其中试卷共23页, 欢迎下载使用。












