
重庆市万州第二高级中学2022-2023学年高二上学期开学考试化学试题(Word版含答案)
展开万州二中2021级高二上期人学考试化学试题
命题人:袁婷 审题人:彭泰婷
可能用到的相对原子质量:H-1,C-12,O-16,Na-23,Zn-65
一、单选题(本大题共14小题,每小题3分,共42分)
1.2022年2月北京冬奥会尽显化学科技,科技助力体现环保理念,下列说法正确的是( )
A.火炬“飞扬”外壳由有机高分子材料碳纤维制成
B.火炬“飞扬”采用氢能为燃料,体现“绿色低碳”的发展理念
C.奥运场馆采用硫化镉发电玻璃,实现了电能向化学能的转化
D.奥运“战袍”利用微信小程序调控石墨烯片加热保暖,石墨烯属于烯烃
2.下列有关化学用语正确的是( )
A.的电子式: B.聚丙烯的结构简式:
C.的结构式: D.的电离方程式:
3.糖类、油脂、蛋白质为食物中的基本营养物质.下列说法正确的是( )
A.多糖、油脂、蛋白质都是高分子化合物
B.工业上可利用油脂来制肥皂
C.向鸡蛋清中加入浓硝酸,无明显现象
D.淀粉、纤维素分子式均为,二者互为同分异构体
4.为阿伏加德罗常数的值.下列说法不正确的是( )
A.常温常压下,中含有质子的数目为
B.溶液中含有的的数目为
C.与一定量盐酸反应最终产生失去的电子数为
D.标准状况下,氦气中含有原子的数目为
5.反应,在不同条件下反应,其平均反应速率如下,其中反应速率最大的是( )
A. B.
C. D.
6.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.溶液:
B.无色透明的溶液中:
C.与反应能放出的溶液中:
D.能使酚酞显红色的溶液中:
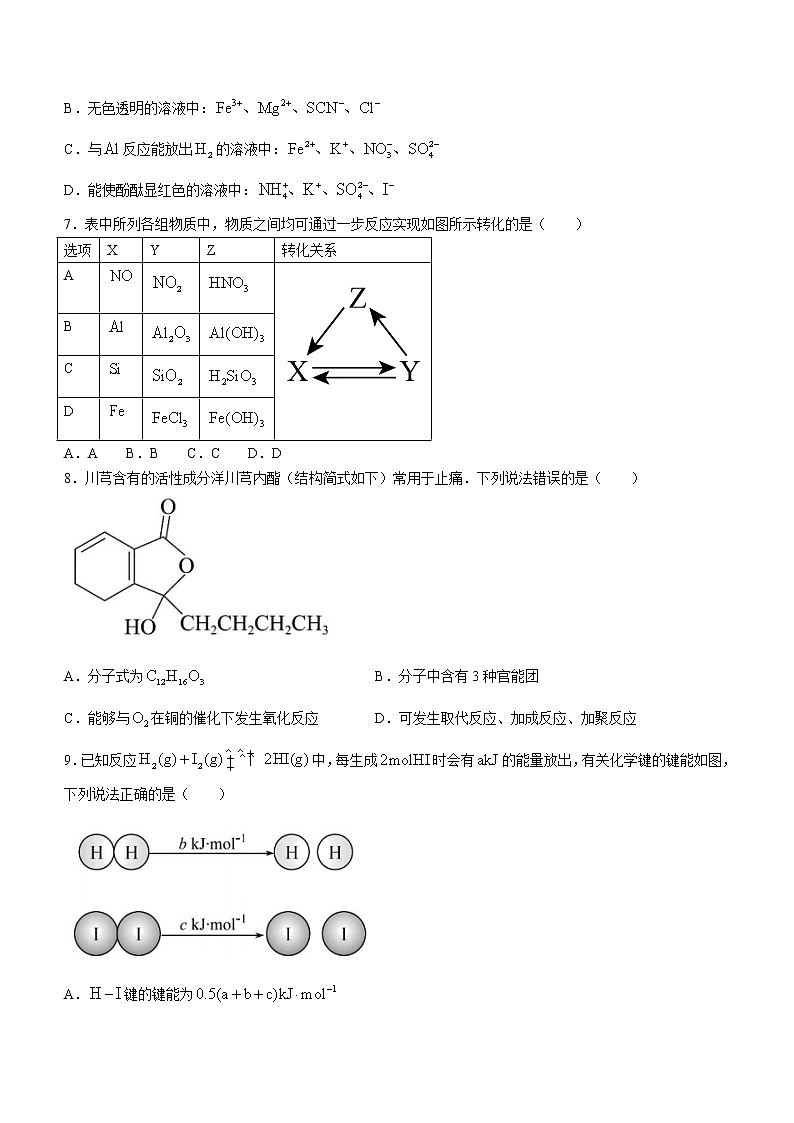
7.表中所列各组物质中,物质之间均可通过一步反应实现如图所示转化的是( )
选项 | X | Y | Z | 转化关系 |
A | ||||
B | ||||
C | ||||
D |
A.A B.B C.C D.D
8.川芎含有的活性成分洋川芎内酯(结构简式如下)常用于止痛.下列说法错误的是( )
A.分子式为 B.分子中含有3种官能团
C.能够与在铜的催化下发生氧化反应 D.可发生取代反应、加成反应、加聚反应
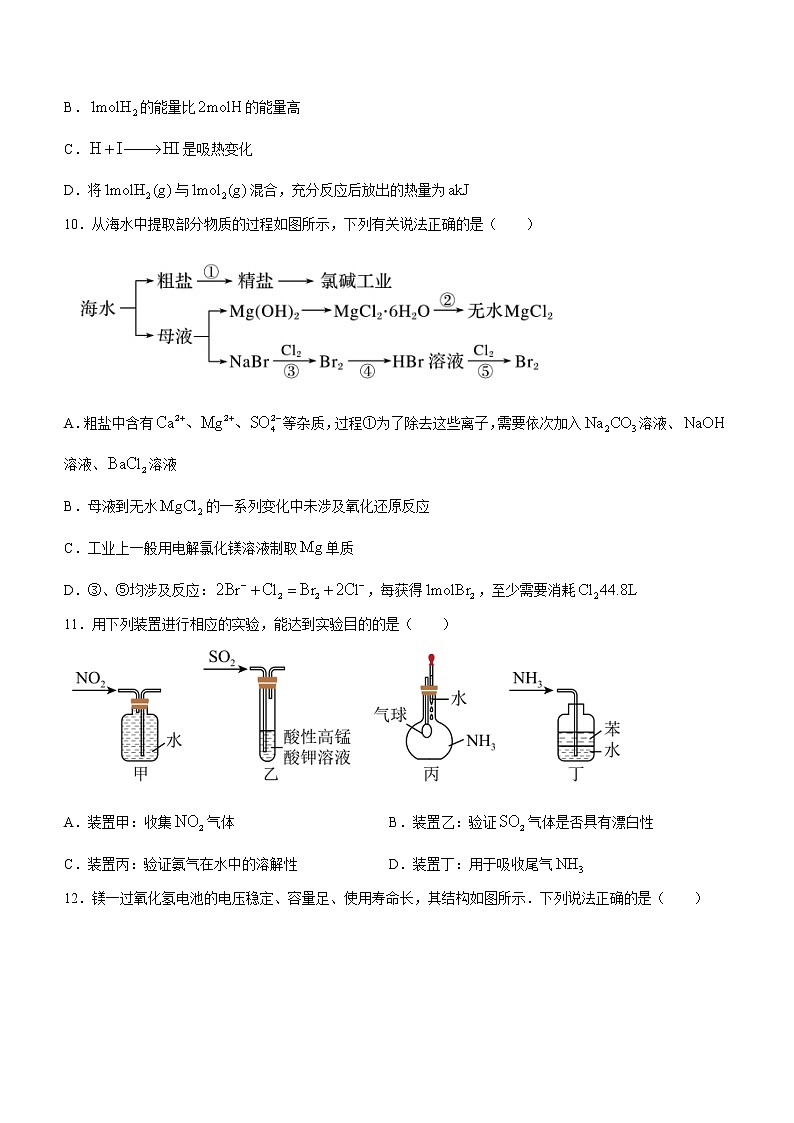
9.已知反应中,每生成时会有的能量放出,有关化学键的键能如图,下列说法正确的是( )
A.键的键能为
B.的能量比的能量高
C.是吸热变化
D.将与混合,充分反应后放出的热量为
10.从海水中提取部分物质的过程如图所示,下列有关说法正确的是( )
A.粗盐中含有等杂质,过程①为了除去这些离子,需要依次加入溶液、溶液、溶液
B.母液到无水的一系列变化中未涉及氧化还原反应
C.工业上一般用电解氯化镁溶液制取单质
D.③、⑤均涉及反应:,每获得,至少需要消耗
11.用下列装置进行相应的实验,能达到实验目的的是( )
A.装置甲:收集气体 B.装置乙:验证气体是否具有漂白性
C.装置丙:验证氨气在水中的溶解性 D.装置丁:用于吸收尾气
12.镁一过氧化氢电池的电压稳定、容量足、使用寿命长,其结构如图所示.下列说法正确的是( )
A.镁为正极,电极反应式为
B.放电时正极周围溶液的减小
C.放电时溶液中的向正极移动
D.该电池总反应的离子方程式为
13.汽车尾气中的、碳氢化合物通过排气系统的净化装置(催化剂主要由等物质和稀土材料组成)转化为无害气体,净化原理如图.下列正确的是( )
A.的水溶液能导电,为电解质 B.发生了氧化反应
C.转化为时,转化为 D.催化剂能改变
14.下列实验操作、现象及解释或结论均正确的是( )
选项 | 操作 | 现象 | 解释或结论 |
A | 某钠盐晶体完全溶解于稀盐酸,所得澄清溶液中滴加试剂 | 澄清溶液中出现白色沉淀 | 该盐为 |
B | 稀硫酸滴加到纯碱中,产生的气体通入的溶液中 | 的溶液中出现白色沉淀 | 非金属性: |
C | 向某溶液中滴入后,再加入溶液 | 溶液呈血红色 | 溶液中一定含有 |
D | 蔗糖中滴加稀硫酸,加热一段时间后,滴加银氨溶液,再加热 | 未出现银镜现象 | 蔗糖没有发生水解生成葡萄糖 |
A.A B.B C.C D.D
二、非选择题(本大题共4小题,共58分)
15.(14分)乳酸乙酯是白酒的香气成份之一,广泛用于食品香精.乳酸乙酯发生如图变化:
(已知烃A是衡量一个国家化工水平的重要标志)
(1)B中含氧官能团的名称是_____________;②的反应类型是_______________;
(2)A分子的空间结构是_________________;
(3)③的化学方程式是_________________________;⑤的化学方程式是_______________;
(4)与足量反应,可生成_______ ;
(5)绿色化学的核心内容之一是“原子经济性”,即原子利用率为.下列转化符合绿色化学要求的是_______(填序号).
a.乙醇制取乙醛 b.甲烷制备 c.
16.(14分)现有在实验室中模拟甲醇的合成反应,在的恒容密闭容器内以物质的量之比充入和.在时,发生反应:.体系中随时间的变化如表1:
时间 | 0 | 1 | 2 | 3 | 5 |
0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
(1)如图1表示反应中的变化曲线,其中合理的是_______.
(2)用表示内该反应的平均速率__________.
(3)反应在时达到平衡,此时的转化率为_______.
(4)能说明该反应已达到平衡状态的是_______.
a. b.容器内压强保持不变
c.断开键的同时断开键 d.容器内气体密度保持不变
e.的浓度保持不变
(5)若要增大反应速率,可采取的措施____________(写一条即可).
(6)与的反应可将化学能转化为电能,其工作原理如图所示.图中从_______(填A或B)通入,b电极附近溶液将___________(填升高、降低或不变).
17.(16分)某化学兴趣小组利用以下装置探究氯气与氨气之间
的反应.其中装置A、F分别为氨气和氯气的发生装置,装置C为纯净、干燥的氯气与氨气发生反应的装置.回答下列问题:
(1)装置F中发生反应的化学方程式是_______________________________.
(2)盛有浓氨水的仪器名称是________________,E中的试剂是________________.
(3)C中的装置应选用图中的_________(填甲或乙).
(4)装置C中集气瓶中有大量白烟产生,另一产物是空气主要成分,写出发生反应的化学方程式_____________________________________.
(5)兴趣小组查资料得知,在催化剂作用下,与能反应生成无污染的产物.另外收集了少量充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入(两端用夹子夹好).
操作步骤 | 实验现象 | 解释原因 |
打开,推动注射器活塞,使X中的气体缓慢入Y管中 | Y管中红棕色气体慢慢变浅 | 反应的化学方程式①__________________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开 | ②_______________ | ③__________________ |
18.(14分)钠及其化合物的生产、应用,是化工生产与研究的重要组成部分.
Ⅰ.碳酸钠是一种重要的化工原料,主要采用氨碱法生产.回答下列问题:
Ⅰ.已知:①
②
(1)反应的________
Ⅱ.工业上以侯氏制碱法为基础生产焦亚硫酸钠(,能溶于水)的工艺流程如下:
(2)反应Ⅰ的化学方程式是________________________.
(3)关于上述流程,下列说法不正确的是___________(填字母).
A.氨气溶于水使溶液呈碱性的原因是:
B.在空气中灼烧发生反应的化学方程式为
C.该流程中,可以循环使用
D.溶液乙经过蒸发结晶得到五水硫酸铜晶体
(4)Y溶液中含有阳离子有,和离子X.检验离子X的方法是
_____________________________________________________________________________.
(5)已知与稀硫酸反应放出,其离子方程式为__________________________.
(6)反应Ⅲ包含多步反应:第一步:……;第二步:
为了减少产品中的杂质含量,理论上需控制第一步反应中气体反应物与固体反应物的物质的量之比为___________;若通入气体量不足,则会导致产品中杂质含量增加.检验产品中是否含有碳酸钠杂质,所需试剂是___________(填编号).
①酸性高锰酸钾溶液 ②品红溶液 ③澄清石灰水
④饱和碳酸氢钠溶液 ⑤溶液 ⑥稀盐酸
参考答案
1-5:BDBCD 6-10:AACAB 11-14:CDCB
15.(14分,每空2分)
(1)羟基、羧基 加成反应 (2)平面结构
(3)2CH3CH2OH+O22CH3CHO+2H2O+CH3COOH +H2O
(4)1 (5)c
16.(14分,每空2分)
(1)b (2)0.006
(3)52% (4)be (5)升温(增大反应物浓度或适当的催化剂)
(6)A 升高
17.(16分,每空2分)
(1)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(2)分液漏斗 饱和NaCl溶液
(3)乙 (4)8NH3+3Cl2=N2+6NH4Cl
(5)① 8NH3+6NO2 7N2+12H2O
② Z 中 NaOH 溶液产生倒吸现象
③ 反应后气体分子数减少,Y 管中压强小于外界压强
18.(14分,每空2分)
(1)+135.6
(2)
(3)D
(4)取少量溶液于洁净试管中,加入溶液,再加热,用湿润红色石蕊试纸置于试管口,试纸变蓝,则含有,反之则无
(5) S2O+2H+═2SO2↑+H2O
(6)2∶1 ①③⑥
(解析:焦亚硫酸钠中钠元素与硫元素的原子数比是1:1,由原子个数守恒可知,控制反应Ⅱ中二氧化硫与碳酸氢钠的物质的量之比为2:1可以减少产品中的杂质含量;若二氧化硫不足,焦亚硫酸钠产品中亚硫酸钠、碳酸钠等杂质含量增加;检验产品中是否含有碳酸钠杂质的步骤为取样品,加入足量稀盐酸,生成的气体通入足量的高锰酸钾溶液,除去二氧化硫气体后把气体通入澄清石灰水,若溶液变浑浊,样品含有碳酸钠杂质,则需要的试剂是①③⑥,故答案为:2:1;①③⑥。)
重庆市万州第二高级中学2023-2024学年高二上学期期中考试化学试题(Word版附解析): 这是一份重庆市万州第二高级中学2023-2024学年高二上学期期中考试化学试题(Word版附解析),共19页。试卷主要包含了本试卷分第I卷和第II卷两部分, 下列装置或操作正确的是, 已知常温下,的电离常数, 已知等内容,欢迎下载使用。
重庆市万州第二高级中学教育集团2023-2024学年高二上学期10月月考化学试题(Word版附解析): 这是一份重庆市万州第二高级中学教育集团2023-2024学年高二上学期10月月考化学试题(Word版附解析),共19页。试卷主要包含了本试卷分第I卷和第II卷两部分, 下列说法正确的是等内容,欢迎下载使用。
重庆市万州第二高级中学2022-2023学年高二上学期开学考试化学试题(含答案): 这是一份重庆市万州第二高级中学2022-2023学年高二上学期开学考试化学试题(含答案),共19页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。












