

2021抚顺六中高一上学期期末考试化学试题含答案
展开这是一份2021抚顺六中高一上学期期末考试化学试题含答案,共8页。试卷主要包含了O-16,Fe3都可以由化合反应制得等内容,欢迎下载使用。
抚顺市第六中学2020-2021学年度上学期期末考试
高一化学试卷
(考试时间:90分钟 满分100分)
可能用到的相对原子质量:H-1、O-16、Na-23、S-32、Fe-56
第Ⅰ卷 选择题(共60分)
一.选择题(共20题,每题只有一个正确选项,每题3分,共60分)
1.下列分散系中,分散质微粒直径最大的是( )
A.新制氢氧化铜悬浊液 B.淀粉溶液
C.溴的四氯化碳溶液 D.雾
2.一化学兴趣小组进行化学实验时,按照图1连接线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
A.NaCl不是电解质
B.NaCl溶液是电解质
C.NaCl在水溶液中电离出了可以自由移动的离子
D.NaCl溶液中水电离出大量的离子
3.下列离子方程式中正确的是( )
A.用氯气作为水的消毒剂:Cl2+H2O===2H++Cl-+ClO-
B.用FeCl3溶液腐蚀印刷铜电路板:Cu+2Fe3+===2Fe2++Cu2+
C.用小苏打治疗胃酸过多:CO2+2H+===CO2↑+H2O
D.胃药里含氢氧化铝能降低胃酸:OH-+H+=== H2O
4.在某无色透明的酸性溶液中,能大量共存的离子组是( )
A.Na+、K+、SO、OH-
B.Na+、K+、Cl-、NO
C.Fe3+、K+、Na+、NO
D.Ag+、K+、SO、Cl-
5.重金属离子具有毒性。实验室中有甲、乙两种重金属离子的废液,甲废液经化验呈碱性,主要的有毒离子为Ba2+,如将甲、乙两废液按一定比例混合,毒性明显降低。则乙废液中可能含有的离子是( )
A.Cu2+和SO B.Cu2+和Cl
C.K+和SO D.Ag+和NO
6.下列自然、生活中的事例不属于氧化还原反应的是( )
A.动物呼吸 B.植物光合作用
C.金属生锈 D.石膏点制豆腐
7.下列变化需要加入适当的氧化剂才能完成的是( )
A.CuO→Cu B.Fe→FeCl2
C.H2SO4→H2 D.HNO3→N2
8.科学家指出,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒,这是因为对人体无害的+5价砷类物质在维生素C的作用下,能够转化为有毒的+3价砷类化合物。下列说法不正确的是( )
A.维生素C具有还原性
B.上述过程中砷元素发生还原反应
C.上述过程中+5价砷类物质作氧化剂
D.+5价砷转化为+3价砷时,失去电子
9.如图所示,在小烧杯中加入水和煤油各20 mL,然后将一小粒金属钠放入烧杯中,观察到的现象可能为( )
A.钠在水层中反应并四处游动
B.钠停留在煤油层中不发生反应
C.钠在煤油的液面上反应并四处游动
D.钠在水与煤油的界面处反应并上下跳动
10.下列说法不正确的是( )
A.Na2O2可用于呼吸面具中氧气的来源
B.Na2O和Na2O2投入水中都能生成NaOH,都是氧化还原反应
C.Na2CO3可用于制玻璃、肥皂、造纸、纺织等工业,NaHCO3可用于治疗胃酸过多、制造发酵粉等
D.NaCl可用作调味品
11.下列说法正确的是( )
A.焰色试验为黄色,说明该物质中含有钠元素
B.某物质的焰色试验不显紫色(未透过蓝色钴玻璃),说明该物质中肯定没有钾元素
C.焰色试验不能用于物质的鉴别
D.焰色试验是化学变化
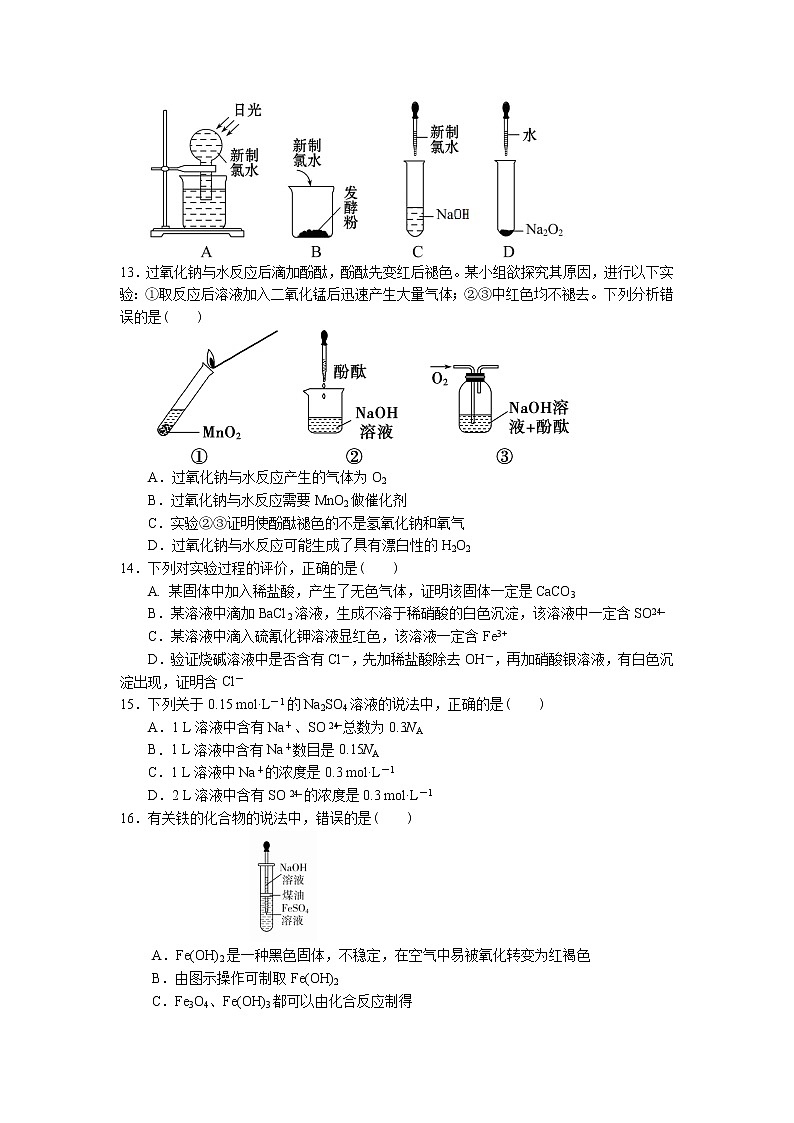
12.下列实验过程中,不会产生气体的是( )
13.过氧化钠与水反应后滴加酚酞,酚酞先变红后褪色。某小组欲探究其原因,进行以下实验:①取反应后溶液加入二氧化锰后迅速产生大量气体;②③中红色均不褪去。下列分析错误的是( )
A.过氧化钠与水反应产生的气体为O2
B.过氧化钠与水反应需要MnO2做催化剂
C.实验②③证明使酚酞褪色的不是氢氧化钠和氧气
D.过氧化钠与水反应可能生成了具有漂白性的H2O2
14.下列对实验过程的评价,正确的是( )
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体一定是CaCO3
B.某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO
C.某溶液中滴入硫氰化钾溶液显红色,该溶液一定含Fe3+
D.验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl-
15.下列关于0.15 mol·L-1的Na2SO4溶液的说法中,正确的是( )
A.1 L溶液中含有Na+、SO总数为0.3NA
B.1 L溶液中含有Na+数目是0.15NA
C.1 L溶液中Na+的浓度是0.3 mol·L-1
D.2 L溶液中含有SO的浓度是0.3 mol·L-1
16.有关铁的化合物的说法中,错误的是( )
A.Fe(OH)2是一种黑色固体,不稳定,在空气中易被氧化转变为红褐色
B.由图示操作可制取Fe(OH)2
C.Fe3O4、Fe(OH)3都可以由化合反应制得
D.Fe(OH)3胶体呈红褐色、透明,能发生丁达尔效应
17.铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途。下列关于铝的说法正确的是( )
A.铝的表面容易形成致密的氧化膜,抗腐蚀性能好
B.常温下不与任何酸、碱反应
C.铝元素在地壳中的含量高,储量丰富,仅次于铁
D.工业上通常用钠与铝盐溶液反应来制备铝
18.在500 mL NaOH溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体33.6 L,该NaOH溶液的浓度为( )
A.1.0 mol·L-1 B.2.0 mol·L-1
C.1.5 mol·L-1 D.3.0 mol·L-1
19.简单原子的原子结构可用下图来形象表示:
其中·表示质子或电子,°表示中子,则下列有关的叙述中,正确的是( )
A.①②③为同素异形体
B.①②③互为同位素
C.①②③是三种化学性质不同的粒子
D.①②③具有相同的质量数
20.在元素周期表中位于金属元素和非金属元素交界处最容易找到的材料是( )
A.制催化剂的材料
B.耐高温、耐腐蚀的合金材料
C.制农药的材料
D.半导体材料
第Ⅱ卷 非选择题(共40分)
二.填空题(共4题,共40分)
21.(共12分)用18.4 mol/L的浓H2SO4来配制500 mL 0.2 mol/L的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥托盘天平 ⑦药匙。
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时不需要使用的有________(填代号),还缺少的仪器是____________。
(2)经计算,需浓H2SO4的体积为___________,量取浓硫酸时应选用_______(填序号)(选填①10 mL、②50 mL、③100 mL三种规格)的量筒。
(3)将所配制的稀H2SO4进行测定,发现浓度大于0.2 mol/L。可能引起这种结果的操作是____________。
①定容时俯视刻度线;②未冷却到室温就定容;③用量筒量取浓硫酸时仰视读数;④洗涤量取浓硫酸的量筒并将洗涤液转移到容量瓶;⑤摇匀后,发现液面在刻线以下,未采取其它任何补救操作;⑥洗涤完烧杯的洗液直接倒掉,未转移到容量瓶里;⑦把烧杯中的溶液转移到容量瓶前,容量瓶中含有少量的水;⑧定容时水加多了,用滴管吸出少量水至刻度线。
22.(共10分)如图所示是制取无水氯化铜的实验装置图,已知干燥管E中盛有碱石灰,碱石灰是酸性气体和水的良好吸收剂。现将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请完成下列问题:
(1)盛放浓盐酸的仪器名称为_________________。
(2)写出装置A烧瓶中发生反应的化学方程式,并用单线桥法表示电子转移方向和数目____________________________________________________________。
(3)玻璃管D中发生反应的化学方程式是________________________,反应现象是 。
23.(共8分)室温下,单质A、B、C分别为固体、黄绿色气体、无色气体,在合适的反应条件下,它们可以按下列框图进行反应。又知E溶液是无色的。
请回答:
(1)画出B原子结构示意图:________________________________。
(2)写出反应①的化学方程式:________________________________。
(3)写出反应③的离子方程式:________________________________。
(4)写出反应④的离子方程式:________________________________。
24.(共10分)A、B、C、D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族。C原子核内质子数等于A、B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍。试回答:
(1)写出C元素的名称:________。
(2)这四种元素中的非金属元素的最简单氢化物的稳定性由强到弱的顺序是___________________。
(3)A与B形成的三原子分子的电子式是________。
(4)B与D形成原子个数比为1∶1的化合物中存在的化学键是__________(填“离子键”、“共价健”或“离子键、共价键”)。
(5)A元素某氧化物与D元素某氧化物反应生成单质的化学方程式是___________________。
高一化学答案
一.选择题(共20题,每题只有一个正确选项,每题3分,共60分)
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
答案 | A | C | B | B | A | D | B | D | D | B |
题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
答案 | A | C | B | C | C | A | A | B | B | D |
二.填空题(共4题,共40分)
21.(共12分)
(1)②⑥⑦(2分,漏选、错选不得分)
500 mL容量瓶(2分,不指明规格不得分)
(2) 5.4 mL (2分) ①(2分)
(3)①②③④(4分,错选不得分,漏选一个扣1分)
22.(共10分)
(1)分液漏斗(2分)
(2)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O(单线桥略)(方程式2分,单线桥2分)
(3))Cu+Cl2CuCl2(2分) 产生棕黄色的烟(2分)
23.(共8分)
(1) (2分)
(2)2Fe+3Cl22FeCl3(2分)
(3)Fe+2H+===Fe2++H2↑(2分)
(4)2 Fe2++Cl2=== 2Fe3++ 2Cl-(2分)
24.(共10分)
(1)硅(2分)
(2)H2O > CH4 > SiH4 (2分)
(3) (2分)
(4)离子键、共价键(2分)
(5)2Na2O2+2CO2=2Na2CO3+O2(2分)
相关试卷
这是一份辽宁省抚顺市六校协作体2023-2024学年高一上学期期末考试化学试题含答案,共8页。试卷主要包含了5 Cu-64, 下列各图与对应叙述不相符的是等内容,欢迎下载使用。
这是一份哈尔滨市第六中学校2021-2022学年高一上学期期末考试化学试题(含答案解析),文件包含精品解析哈尔滨市第六中学校2021-2022学年高一上学期期末考试化学试题原卷版docx、精品解析哈尔滨市第六中学校2021-2022学年高一上学期期末考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共32页, 欢迎下载使用。
这是一份2020抚顺六校协作体高一上学期期末考试化学试题PDF版含答案,文件包含首发辽宁省抚顺市六校协作体2019-2020学年高一上学期期末考试化学试题PDF版pdf、首发辽宁省抚顺市六校协作体2019-2020学年高一上学期期末考试化学答案PDF版pdf等2份试卷配套教学资源,其中试卷共6页, 欢迎下载使用。











