

2021鄂州高二下学期期末质量监测化学试题含答案
展开www.ks5u.com鄂州市2020—2021学年度下学期期末质量监测
高 二 化 学
★祝考试顺利★
注意事项:
1.满分100分,考试时间75分钟。
2.答题前,考生务必将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
3.选择题在每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;主观题用0.5毫米黑色墨水签字笔答在答题卡上相对应的答题区域内。答在试题卷上无效。
4.计算中可能用到的相对原子量:H-1;C-12;N-14;O-16;Mg-24;
Cl-35.5;Fe-56;Sn-119
第Ⅰ卷(选择题)(共45分)
一、选择题,共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是最符合题目要求的。
1.化学与社会、生活等有密切关系。下列说法正确的是( )
A.医用消毒酒精中乙醇的体积分数为95%
B.可用聚氯乙烯作食品包装膜
C.可用灼烧的方法区别蚕丝和棉麻制品
D.食用油可反复加热进行油炸食品而无害
2. 基态原子核外电子排布的原理或规则不包括( )
A.能量守恒原理 B.能量最低原理 C.泡利原理 D.洪特规则
3.我国北斗导航卫星使用铷(Rb)原子钟。下列说法正确的是( )
A.Rb和Rb互为同素异形体 B.Rb原子核内中子数为37
C.Rb的价电子排布为4s1 D.Rb和Rb具有相同的质子数
4.下列说法正确的是( )
A.CH4与C3H6互为同系物
B.可用饱和Na2CO3溶液除去乙酸乙酯中混有的杂质乙酸
C.油脂在酸性条件下的水解反应叫皂化反应。
D.纤维素、油脂、蛋白质都属于天然高分子化合物
5.等质量的下列各烃分别完全燃烧,耗O2量最少的是( )
A.C3H8 B.CH4 C.C2H2 D.C2H4
6.为提纯下列物质(括号内为杂质),所选用的除杂试剂和分离方法都正确的是( )
选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
A | 溴苯(溴) | NaOH溶液 | 分液 |
B | 己烷(己烯) | 溴水 | 分液 |
C | 乙烯(SO2) | 酸性KMnO4溶液 | 洗气 |
D | 苯(苯酚) | 浓溴水 | 过滤 |
7.下列有关图示,能直观形象地展示化学知识。以下图示正确的是( )
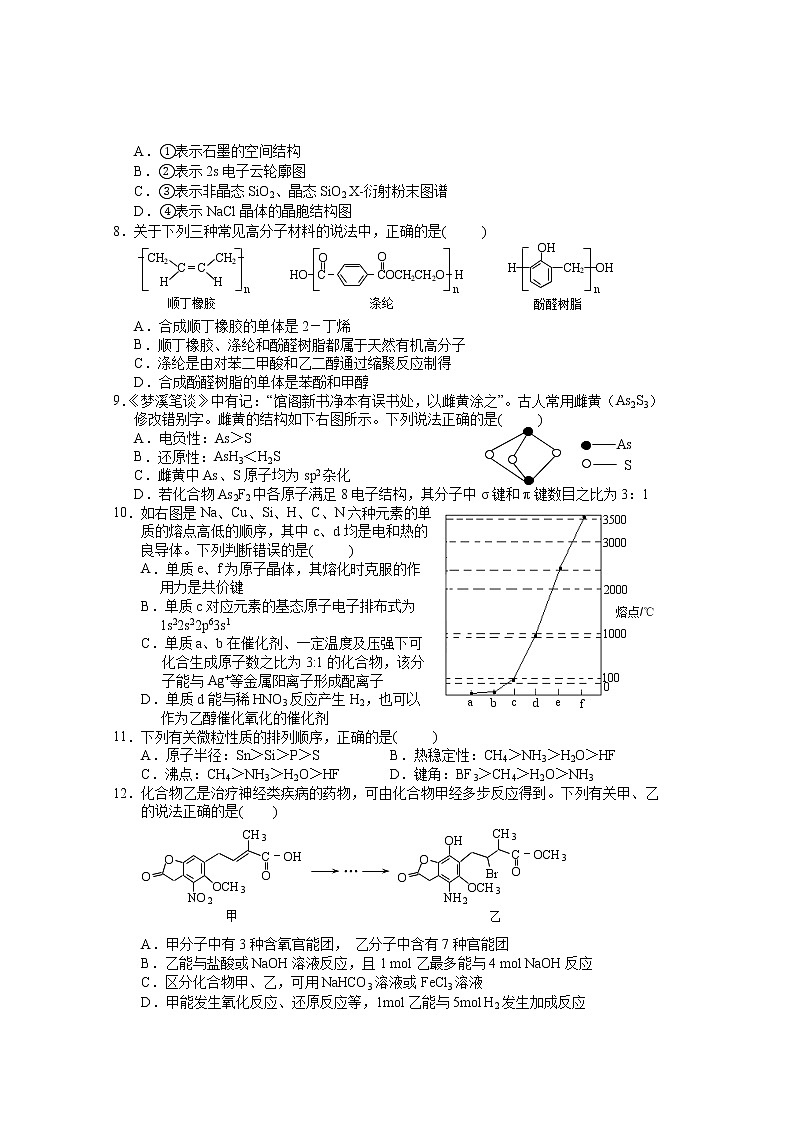
A.①表示石墨的空间结构
B.②表示2s电子云轮廓图
C.③表示非晶态SiO2、晶态SiO2 X-衍射粉末图谱
D.④表示NaCl晶体的晶胞结构图
8.关于下列三种常见高分子材料的说法中,正确的是( )
A.合成顺丁橡胶的单体是2-丁烯
B.顺丁橡胶、涤纶和酚醛树脂都属于天然有机高分子
C.涤纶是由对苯二甲酸和乙二醇通过缩聚反应制得
D.合成酚醛树脂的单体是苯酚和甲醇
9.《梦溪笔谈》中有记:“馆阁新书净本有误书处,以雌黄涂之”。古人常用雌黄(As2S3)
修改错别字。雌黄的结构如下右图所示。下列说法正确的是( )
A.电负性:As>S
B.还原性:AsH3<H2S
C.雌黄中As、S原子均为sp2杂化
D.若化合物As2F2中各原子满足8电子结构,其分子中σ键和π键数目之比为3:1
10.如右图是Na、Cu、Si、H、C、N六种元素的单质的熔点高低的顺序,其中c、d均是电和热的
良导体。下列判断错误的是( )
A.单质e、f为原子晶体,其熔化时克服的作
用力是共价键
B.单质c对应元素的基态原子电子排布式为
1s22s22p63s1
C.单质a、b在催化剂、一定温度及压强下可
化合生成原子数之比为3:1的化合物,该分
子能与Ag+等金属阳离子形成配离子
D.单质d能与稀HNO3反应产生H2,也可以
作为乙醇催化氧化的催化剂
11.下列有关微粒性质的排列顺序,正确的是( )
A.原子半径:Sn>Si>P>S B.热稳定性:CH4>NH3>H2O>HF
C.沸点:CH4>NH3>H2O>HF D.键角:BF3>CH4>H2O>NH3
12.化合物乙是治疗神经类疾病的药物,可由化合物甲经多步反应得到。下列有关甲、乙
的说法正确的是( )
A.甲分子中有3种含氧官能团, 乙分子中含有7种官能团
B.乙能与盐酸或NaOH溶液反应,且1 mol乙最多能与4 mol NaOH反应
C.区分化合物甲、乙,可用NaHCO3溶液或FeCl3溶液
D.甲能发生氧化反应、还原反应等,1mol乙能与5mol H2发生加成反应
13.已知C-C或C-H等单键均可绕键轴旋转,关于结构简式为 的烃,下列有关说法中错误的是( )
A.分子中至少有9个碳原子处于同一平面上
B.分子中至少有10个碳原子处于同一平面上
C.分子中最多有14个碳原子处于同一平面上
D.分子中最多有24个原子处于同一平面上
14.五种前四周期的元素X、Y、Z、Q、T。已知X元素基态原子的M层有6种运动状态不同的电子;Y原子的特征电子构型为3d84s2,基态Z原子的L层p能级有一个空轨道;Q原子的L电子层的p能级只有一对成对电子;基态T原子的M电子层上p轨道半充满。下列说法错误的是( )
A.Y、Q及氢三种元素形成的某化合物,能用于制作可充电电池的电极材料
B.若X、T、Z的最高价的氧化物对应的水化物分别为u、v、w,则酸性为:u>v>w。理由是非羟基氧原子数越多,酸性越强
C.X、Y、T三种元素第一电离能的大小次序是:X>T>Y
D.化合物ZQ2、ZX2均是由极性键构成的非极性分子
15.光刻胶是制造芯片、集成电路的关键材料。某新型的光刻胶(高分子化合物e),可以由
芳香族化合物a、有机物b(丙酮)为原料制备,其合成路线如下:
其中a、c均含有-COOH。下列说法错误的是( )
A.反应①为加成反应 B.有机物c脱水成烯的产物可能有2种
C.反应②为酯化 D.反应③为缩聚反应
第Ⅱ卷(非选择题,共55分)
16.(共13分)
苯胺(C6H5NH2)是重要的化工原料,可合成染料、药物、树脂等,也可作为橡胶硫化促进剂;苯胺是三类致癌物;尽量避免接触皮肤及蒸汽吸入。
实验室拟制取及提纯苯胺,且已知有关信息如下:
① C6H5NH2与NH3类似,与盐酸反应生成易溶于水的盐酸苯胺( )。
②用金属Sn和盐酸还原硝基苯制得苯胺的反应如下:
③下表为某些物质的物理性质(密度为实验条件温度下所测):
物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度/g·mL-1 |
苯胺 | 93 | -6.2 | 184 | 微溶于水,易溶于乙醚 | 1.02 |
硝基苯 | 123 | 5.7 | 210.9 | 难溶于水,易溶于乙醚 | 1.23 |
乙醚 | 74 | -116.2 | 34.6 | 微溶于水 | 0.713 |
步骤I、制备苯胺:
向如下图甲所示的装置中,加入过量的20mL浓盐酸、11.9g金属Sn、5.00mL硝基苯,在热水浴中充分反应约30min;冷却后向三颈烧瓶中加入足量的NaOH溶液至呈碱性。
⑴在进行苯胺的有关实验时,必须戴硅橡胶手套,宜在 中进行。
⑵图甲中,除了三颈烧瓶外,另一种仪器是 ,其作用是 ,冷却水从 进, 出(填:a或b)。
⑶加入NaOH溶液与有机物反应的离子方程式是 。
步骤II、提纯苯胺:
i)取出上图甲中的三瓶烧瓶,改为如上图乙所示的装置。加热装置A产生水蒸气,采用水蒸气蒸馏的方法,将B中的苯胺逐渐吹出至C中(收集到苯胺及水的混合液体);从混合中分离出粗苯胺及水溶液x。
ii)向所得的水溶液x中加入固体NaCl至饱和,再用乙醚萃取,得到乙醚的萃取液。
iii)合并粗苯胺及乙醚的萃取液,用固体KOH干燥后,取干燥后的液体进行蒸馏得到得到2.00mL苯胺。
⑷装置A中玻璃管的作用是 。
⑸该实验中所得苯胺的产率为 (保留三位有效数字)。
17.(共14分)
如下图所示的变化中,有机物I是合成抗凝血药物的中间体。下面是合成I的一种线路,其中省略了部分产物及某些反应条件(已知:酚羟基难与羧基酯化),回答下列问题:
⑴有机物E的结构简式是 ;I中含氧官能团的名称是 。
⑵F的同分异构体中,与F含有相同官能团且为芳香族化合物,其中沸点最高的有机物的名称是 。
⑶D+G→H的有机反应类型是 。
⑷F→G反应的化学方程式是 。
⑸同时具备下列条件的H的同分异构体有 种(不考虑立体异构),其中苯环上的一氯代物只有2种的结构简式为 。
①苯环上有3个取代基
②分子中只含一种官能团,且能发生水解反应
③在水溶液中,1mol的该有机物最与4mol NaOH反应
18.(共14分)
有机化学实验中,常用甲醛与盐酸作为氯甲基(-CH2Cl)化试剂。以下是一种新型有效、副作用小的镇痛消炎药J的合成路线:
⑴若要确定F分子中氢原子的种类,可用下列的 测定(填选项)。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
⑵上述A→J的有机物中,含有手性碳原子的分子有 种。
⑶反应①化学方程式为 ;已知吡啶(C5H5N)分子含有六元环,吡啶的分子结构类似于苯。则反应⑧使用吡啶的理由 。
⑷由I生成J,中间需要经过两步反应。
第1步:在酸性条件下加热水解,生成有机物y;
第2步:在水溶液里y与固体NaHCO3反应,经过一系列操作可得结晶水合物J。
则由I生成y的化学方程式是 。
⑸ 是合成 的重要中间体。参照上述题中的合成路线,请你
设计由1,3-丁二烯合成 的一种合成路线(无机试剂任选):
。
19.(共14分)
铁及其化合物在工农业生产、日常生活、科学实验等中有广泛的用途。
⑴最新科学发现,FeF3用于改进的锂离子电池阴极材料,可以使电池电极的能量密度翻三倍;在工业上,FeCl3主要用于金属刻蚀及污水处理。
下表为F、Cl、Fe三种元素的电负性值:
元素 | 电负性 |
F | 4.0 |
Cl | 3.0 |
Fe | 1.8 |
推测FeF3属于 化合物, FeCl3属于 化合物(填:“共价”、“离子”)。
⑵在水溶液里,铁氰化钾 K3[Fe(CN)6]与FeSO4生成蓝色沉淀,常用于Fe2+ 的检验。
①HCN分子、SO42- 离子的空间构型分别为 、 。
②基态Fe3+ 的价电子排布图为________________。
③组成K3[Fe(CN)6]的各元素电负性由大到小的次序是 。
④与铁氰化钾中配体互为等电子体的两种分子的化学式是 。
⑶铁镁合金是目前发现的储氢密度较高的储氢材料之一,铁镁合金晶胞结构如右图所示。下列说法正确的是 (填字母选项)。
A.若晶胞参数为a,则距离最近的两个铁原子的核间距为
B.晶体中存在的化学键类型只有金属键
C.Fe原子周围距离最近的Mg原子有4个
D.假如X点的坐标为(0,0,0),Y点的坐标为(1,1,0)。则上面心w点的坐标为(0.5,0.5,0.5)
⑷某磁性氮化铁的晶胞结构如下图所示,N原子随机排列在Fe构成的正四面体的空隙中。已知六棱柱底边长为x pm,高为y pm,若阿伏加德罗常数的值为NA,则该磁性氮化铁的晶体的密度为
g/cm3。
鄂州市2020~2021学年度下学期期末考试
高二化学参考答案及评分标准
(卷I每小题3分共45分;卷II共55分。满分100分。注:答案仅供参考)
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 |
选项 | C | A | D | B | C | A | D | C | D | D | A | C | A | C | D |
16.(共13分)
(1)通风橱(1分)
(2)球形冷凝器(2分); 冷凝回流、导气(2分,回答“冷凝回流”可得满分); a;b(2分)
(3) (2分)
(4)安全管,平衡气压,防止装置内部气压过高(2分,回答关键字“安全管”可得满分)
(5)43.9%(2分,或43.8%,可得满分)
17.(共14分,每空2分)
(1) (2分); 羟基、羧基(2分。不分次序,只要写对1个即可得1分)
(2)对羟基苯甲酸(或:4-羟基苯甲酸。2分)
(3)取代反应(2分)
(4) (2分)
(5)16(2分); (2分,各1分)
18.(共14分)
(1)d(2分)。
(2)5(2分)。
(3) (2分);
吡啶为弱碱,吸收反应产生的HCl,使平衡向右移动,提高产率(2分)。
(4) (3分)。
(5) (3分)。
19.(共14分)
(1)离子(1分); 共价(1分)。
(2)①直线形(1分);正四面体(1分)。
② (2分)。
③N>C>Fe>K(2分,见错不给分)。
④CO、N2(2分,不分次序)。
(3)AB(2分,见错不给分,每对1个给1分)。
(4)(或,2分)
2022鄂州高一上学期期末质量监测化学试题含答案: 这是一份2022鄂州高一上学期期末质量监测化学试题含答案,共10页。
2022鄂州高二上学期期末质量监测化学试题含答案: 这是一份2022鄂州高二上学期期末质量监测化学试题含答案,共6页。
2021鄂州高二上学期期末质量监测化学试题含答案: 这是一份2021鄂州高二上学期期末质量监测化学试题含答案













