

2022年安徽年中考化学模拟试卷(四)(word版含答案)
展开2022年安徽中考化学模拟试卷(四)
注意事项:1.本卷共两大题17小题,满分40分。考试时间为50分钟。
2.可能用到的相对原子质量:H-1 C-12 O-16 Ca-40
题号 | 一 | 二 | 总分 |
得分 |
|
|
|
一、选择题(本大题包括12小题,每小题1分,共12分。每小题的4个选项中只有1个符合题意。)
1.我国有着悠久的历史和灿烂的文化。下列传统制作工艺中一定发生化学变化的是( )
A.剪纸成花 B. 纺纱织布 C.玉器雕琢 D.烧制瓷器
2.“绿水青山就是金山银山”,保护环境就是保护我们自己。下列做法符合这一理念的是( )
A.为减少白色污染,将废弃塑料焚烧或掩埋
B.为增加粮食产量,大量使用农药、化肥
C.为防止酸雨的发生,大力推广使用脱硫煤
D.为节约水资源,用工业废水直接灌溉农田
3.每年11月9日是全国消防安全教育日。消防安全无小事,下列图标中,表示“禁止烟火”的是( )
A B C D
4.“关爱生命,拥抱健康”是人类永恒的主题。下列说法错误的是( )
A.人体缺乏维生素A会引起夜盲症
B.甲醛能与蛋白质发生反应,会严重危害人体健康
C.不吃霉变或超过保质期的食物
D.微量元素对人体十分重要,必须大量服用
5.传统中药“金银花”的有效成分“绿原酸”具有抗菌杀毒的作用,在防治新型冠状肺炎中成效明显。绿原酸的化学式为C16H18O9,下列有关绿原酸的说法中正确的是( )
A.绿原酸属于氧化物
B.一个绿原酸分子中含有43个原子
C.绿原酸中氢元素的质量分数最大
D.绿原酸中碳、氢、氧元素的质量比为16:18:9
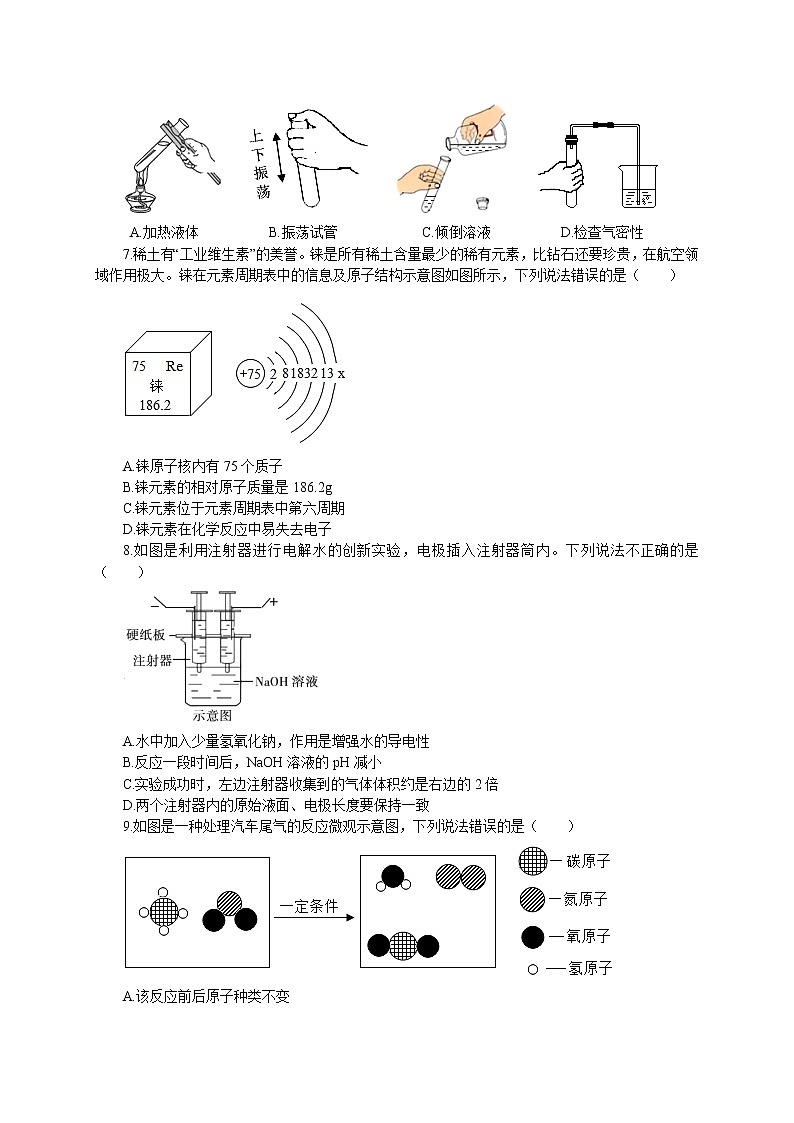
6.规范的实验操作是完成实验的基本保障。下列实验操作正确的是( )
A.加热液体 B.振荡试管 C.倾倒溶液 D.检查气密性
7.稀土有“工业维生素”的美誉。铼是所有稀土含量最少的稀有元素,比钻石还要珍贵,在航空领域作用极大。铼在元素周期表中的信息及原子结构示意图如图所示,下列说法错误的是( )
A.铼原子核内有75个质子
B.铼元素的相对原子质量是186.2g
C.铼元素位于元素周期表中第六周期
D.铼元素在化学反应中易失去电子
8.如图是利用注射器进行电解水的创新实验,电极插入注射器筒内。下列说法不正确的是( )
A.水中加入少量氢氧化钠,作用是增强水的导电性
B.反应一段时间后,NaOH溶液的pH减小
C.实验成功时,左边注射器收集到的气体体积约是右边的2倍
D.两个注射器内的原始液面、电极长度要保持一致
9.如图是一种处理汽车尾气的反应微观示意图,下列说法错误的是( )
A.该反应前后原子种类不变
B.参加反应的~和的分子个数比为1:2
C.该反应前后各元素的化合价均未改变
D.该反应可以减少二氧化氮的排放
10.类比、总结是学好化学的重要方法。下列对化学知识的归纳总结正确的是( )
A.一氧化碳能与氧化铁反应生成铁,一氧化碳也能与氧化铜反应生成铜
B.单质一定由同种元素组成,则有同种元素组成物质一定是单质
C.燃烧都伴随有发光、放热现象,所以有发光、放热现象的变化一定是燃烧
D.酸溶液的pH<7,则pH<7的溶液一定是酸溶液
11.a、b两种固体物质的溶解度曲线如图1所示。下列说法错误的是( )
A. t1℃时,a、b两种物质的溶解度相等
B.a中混有少量b,若要得到较纯净的a,常采用降温结晶的方法
C.t2℃时,由图2可推测物质W是图1中的a物质
D.t2℃时,b物质的饱和溶液降温到t1℃,溶质的质量分数不发生变化
12.正确的设计实验方案是科学探究的重要环节,认真细致地观察和分析实验是获得化学知识的重要途径。以下实验方案设计不能达到相应实验目的的是( )
选项 | 实验目的 | 实验设计 |
A | 比较Zn、Cu、Ag的金属活动性 | 将Zn和Ag分别放入CuSO4溶液中 |
B | 除去NaNO3溶液中混有的Na2SO4 | 加适量Ba(NO3)2溶液,过滤 |
C | 除掉菜刀上的铁锈而不损坏菜刀 | 将菜刀长时间浸泡在稀盐酸中 |
D | 鉴别羊毛和涤纶 | 点燃,闻燃烧产物的气味 |
二、非选择题(本大题包括5小题,共28分。)
13.(6分)(6分)阅读下列材料,回答问题。
航行在大洋上的巨轮中,有一种我国自主研、制造难度堪比航母的巨轮,它就是LNG液化天然气运输船,被喻为世界造船业“皇冠上的明珠”。
天然气装载时,应该在-163℃环境下将其变为液态。液化后的体积是气态的1/600,大大提高了运输效率。一般17万立方米的运输船,它装载的液态天然气经汽化后形成的容量,可满足2418万人一个月的使用量,是一种“海上超级冷冻车”。
装载这类货物的运货系统所用钢板,含镍量达到36%。称为殷瓦钢,它非常薄,只有0.7mm,在-196℃之内它的收缩量膨胀系数非常低,它在空气中对温度的要求非常高,如在施工过程中沾上汗水,24小时内就会被锈穿,使得钢板报废。殷瓦钢还在制造精密仪器,仪表零部件中有着广泛的应用。
(1)殷瓦钢属于__________。
A.天然材料 B.合成材料 C.金属材料 D.复合材料
(2)殷瓦钢具有的性质是_________(写一条)。
(3)天然气完全燃烧时发生反应的化学方程式为___________。
(4)LNG船可通过降温加压使天然气液化后再运输的原因是__________,液化后分子间的间隔会_________。
14.(5分) 通过一年的化学学习,你已经掌握了实验室制取气体的有关知识,请结合下图回答相关问题。
(1)仪器a的名称是___________。
(2)实验室用B装置作为制取二氧化碳气体的发生装置,该装置的优点是________,制取时应将大理石放在________(填“b”或“c”)。
(3)若用F装置收集并测量氧气的体积,应在________(填“d”或“e”)段连接量筒。
(4)实验室里用氯化铵固体和氢氧化钙固体混合加热制得NH3,NH3在水中容易发生如下反应:NH3+H2O=NH3•H2O,请选用上述装置___________(填字母)来制取并收集NH3。
15.(6分)制造芯片需要用到高纯硅,工业上利用石英砂(主要成分为SiO2)制备高纯硅的工艺流程如下图:
(1)玻璃的主要成分也是SiO2,SiO2属于 (填“金属氧化物”或“非金属氧化物”)。
(2)反应Ⅰ的化学方程式是_____________________。
(3)过滤所得粗硅应充分洗涤,以除去表面可能吸附的HCl和____________(填化学式)。
(4)反应Ⅱ要在无氧气环境中进行,原因是____________(答出一种即可)。
(5)上述生产流程中,可以循环利用的物质是____________(填化学式)。
16.(6分)某班级兴趣小组在实验室进行高锰酸钾制取氧气的实验。
(1)写出实验室用高锰酸钾制取氧气的化学方程式___________。
(2)小组同学称取6g高锰酸钾,控制温度在250℃制取氧气,实验结束后,发现收集的氧气大于理论产量,就此问题,大家提出了如下猜想:
猜想1:反应生成的二氧化锰分解放出氧气;
猜想2:反应生成的锰酸钾分解放出氧气。
(3)兴趣小组利用如图装置进行探究(测定反应前后质量变化),相关数据如下表:
实验方案 | 反应前固体物质质量/g | 温度/℃ | 待测数据 |
加热二氧化锰 | 4.0 | t | a |
加热锰酸钾 | 4.0 | t | b |
①反应时的温度应该控制在___________。
②加热一段时间,冷却后,称量发现a=4.0g,b<4.0g,最终得出结论:猜想___________正确。
(4)小明认为上述实验中无需称量反应后固体质量,可通过在导管口放一根带火星的木条进行验证,你是否赞同小明的方法?说明理由___________。
(5)实验室常用高锰酸钾、氯酸钾和过氧化氢制取氧气,请你从原料利用率角度谈谈哪种物质制取氧气最好并说明理由___________。
注意:若答对以下问题奖励3分,化学试卷总分不超过40分。
(6)实验发现,K2MnO4受热只能部分分解,经分析可能是K2MnO4分解的生成物K2O对其分解产生影响。为验证此结论,设计如下实验方案:
①分别取K2MnO4固体于两支试管中,一支试管中加入K2O,一支试管中不加K2O。
②加热,___________。
③比较___________以确定锰酸钾的分解是否与氧化钾有关系。
该过程中还必须控制相同的变量是___________。
17.(5分)为测定某地石灰石样品中碳酸钙的含量,某兴趣小组取20g石灰石样品放在烧杯中,然后向其中滴加某种浓度的稀盐酸,滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(石灰石中含有的杂质不溶于水,也不与稀盐酸反应)。
(1)该石灰石样品中CaCO3的质量分数。
(2)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
参考答案
1.D 2.C 3.B 4.D 5.B 6.D 7.B 8.B 9.C 10.A 11.C 12.C
13.(1)C (2)不耐腐蚀(或收缩量膨胀系数低等合理答案均可) (3)CH4+2O2
14.(1)长颈漏斗 (2)控制反应的发生和停止 b (3)d (4)AD
15(1)非金属氧化物 (2)2Mg+ SiO2
16.(1)2KMnO4K2MnO4+MnO2+O2↑ (3)①250℃ ②2 (4)不赞同,若带火星木条没有复燃可能是氧气浓度较低,不能代表没有氧气产生 (5)氯酸钾,氯酸钾制氧气时其中的氧元素全部转变成氧气,原料利用率为100%(合理即可) (6)②选择相同规格的集气瓶,用排水法分别收集一瓶气体,记录集满氧气所用的时间(合理即可) ③集满一瓶气体所用时间(与上空对应) 锰酸钾固体的质量和加热的温度
17.(1)设石灰石样品中CaCO3的质量为x。
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 6.6g
100:44=x:6.6g
x=15g
该石灰石样品中CaCO3的质量分数= ×100%=75%
答:该石灰石样品中CaCO3的质量分数为70%。
(2)不能,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止(合理即可)
2022年安徽省中考化学模拟试卷(word版含答案): 这是一份2022年安徽省中考化学模拟试卷(word版含答案),共43页。试卷主要包含了5 Na-23,9g,用化学用语填空,化学与我们的生活息息相关等内容,欢迎下载使用。
2022年安徽省中考仿真模拟化学试题(四) (word版含答案): 这是一份2022年安徽省中考仿真模拟化学试题(四) (word版含答案),共8页。试卷主要包含了96 B,下列有关溶液的说法中正确的是,下列实验基本操作中正确的是等内容,欢迎下载使用。
2022年安徽省中考模拟化学试卷(四)(word版含答案): 这是一份2022年安徽省中考模拟化学试卷(四)(word版含答案),共7页。试卷主要包含了化学试卷共17小题,总分40分,可能用到的相对原子质量,二甲双胍,幸福需要辛勤的劳动来创造,建构模型是学习化学的重要方法等内容,欢迎下载使用。













