











第5单元化学方程式(课件+练习)-2022年中考化学一轮复习讲练测
展开
这是一份第5单元化学方程式(课件+练习)-2022年中考化学一轮复习讲练测,文件包含第5单元化学方程式课件-2022年中考化学一轮复习讲练测pptx、第5单元化学方程式练习-2022年中考化学一轮复习讲练测教师版含解析docx、第5单元化学方程式练习-2022年中考化学一轮复习讲练测学生版docx等3份课件配套教学资源,其中PPT共33页, 欢迎下载使用。
第五单元 化学方程式姓名:___________班级:___________考号:___________1.下列现象不能用质量守恒定律解释的是A.铜粉在空气中加热后,生成物的质量比原来铜粉的质量大B.10g的酒精和10g的水混合之后的质量为20g 细铁丝在氧气中燃烧后,生成物的质量比细铁丝质量大 D.纸在空气中燃烧后化为灰烬,灰烬的质量比纸的质量小【答案】B【详解】质量守恒定律是指参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。A、铜粉在空气中加热,铜粉与空气中的氧气反应生成氧化铜,空气中的氧气参与到了反应,故生成物的质量比原来铜粉的质量大,能用质量守恒定律解释,不符合题意;B、10g的酒精和10g的水混合之后的质量为20g,该变化为物理变化,而质量守恒定律只适用于化学变化,选项错误,符合题意;C、细铁丝在氧气中燃烧,铁丝与空气中的氧气反应生成四氧化三铁,空气中的氧气参与到了反应,故生成物的质量比细铁丝的质量大,能用质量守恒定律解释,不符合题意;D、纸在空气中燃烧生成的二氧化碳和水进入到了空气中,故灰烬的质量比纸的质量小,能用质量守恒定律解释,不符合题意。故选B。2.(广东中考)化学是一门以实验为基础的科学,许多化学重大发现和研究成果都是通过实验得到的。下列实验操作或设计中正确的是( ) A.用100ml量筒量取8.5ml盐酸 B.收集氢气 C.验证质量守恒定律 D.过滤【答案】B【详解】试题分析:量取8.5毫升的液体不能用100毫升的量筒,因为会产生太大的误差;收集氢气可以用排水法,因为氢气不溶于水;C装置不能验证质量守恒定律,因为产生的气体会散失到大气中;过滤要用到玻璃棒引流,防止液体冲破滤纸。故选B.3.氨碱法生产纯碱的反应原理之一是2NaHCO3 △ Na2CO3+H2O+CO2↑,某同学从该化学方程式中得出以下信息:①反应前后元素的化合价都没有发生变化;②反应前后元素的种类没有发生变化;③反应前后原子总数、分子总数都没有变化;④反应的速度比较慢;⑤碳酸氢钠受热能分解。其中正确的信息是( )A.①④⑤ B.②③④ C.③④⑤ D.①②⑤【答案】D【详解】该反应是分解反应,反应前后化合价没有发生改变,故①正确;根据质量守恒定律可知反应前后元素的种类、原子的数目没有改变,而分子的数目发生了变化,故②正确,③不正确;根据化学方程式不能判断反应速率,故④不正确;根据化学方程式可知碳酸氢钠受热能分解,故⑤正确.故选D。4.(2021·无锡)如图是甲和乙在一定条件下反应前后分子种类变化的微观示意图。下列叙述正确的是A.甲与丙均属于氧化物B.反应生成的丙与丁的分子个数比为1:1C.反应后原子的数目增加D.该反应能使有害气体转化为无害物质【答案】D【详解】由图可知,该反应的方程式是:2NO+2CO催化剂N2+2CO2;A A、氧化物是由氧元素和另一种元素组成的化合物,甲为一氧化碳,属于氧化物,丙为氮气,属于单质,选项A错误;B、由方程式的意义可知,反应生成的丙与丁的分子个数比为1:2,选项B错误;C、化学反应前后原子的数目不变,选项C错误;D、该反应的反应物均为有害气体,生成物均为无害气体,所以该反应能使有害气体转化为无害物质,选项D正确。故选:D5.(2021·淮安)已知:3Cu+8HNO3(稀)=3Cu(NO3)2+2X↑+4H2O。下列有关该反应说法正确的是A.X的化学式为NO2 B.反应时仅观察到有气泡产生C.铜元素化合价由0变为+2 D.消耗的铜和生成的水质量比为3:4【答案】C【详解】A、根据质量守恒定律可知2X含2个氮原子和2个氧原子,则x的化学式为NO,该选项说法不正确;B、反应时观察到有气泡产生,溶液由无色变蓝色,该选项说法不正确;C、铜中的铜元素化合价是0,硝酸铜中的铜元素的化合价是+2,该选项说法正确;D、消耗的铜和生成的水质量比为:192:72=8:3,该选项说法不正确。故选C。6.(2021·山东滨州)在一密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量见下表,下列说法错误的是A.该反应为分解反应 B.丙可能是该反应的催化剂C.甲、乙两种物质反应前后质量变化之比为2:3 D.x的值为4【答案】C【详解】A、根据表格数据可知甲、丁物质质量增加,乙质量减少,丙质量不变,则是乙反应生成甲与丁,属于分解反应,故选项正确;B、丙质量不变,可能是催化剂,也可能不是催化剂,仅是不参与反应,故选项正确;C、甲、乙两种物质反应前后质量变化之比为(16-8):(32-4)=2:7,故选项错误;D、由质量守恒定律可知X=32+8+5+4-16-5-24-4,故选项正确。故选C。7.(辽宁·锦州)某纯净物3.2g在氧气中完全燃烧,生成4.4g二氧化碳和3.6g水,关于该物质的下列说法中正确的是A.该物质是由碳原子、氢原子、氧原子构成B.该物质由碳、氢两种元素组成C.该物质由碳、氢、氧三种元素组成D.该物质中碳、氢原子个数比为3:1【答案】C【解析】根据质量守恒定律,化学反应前后,元素的种类和质量不变,该物质在氧气中燃烧生成二氧化碳和水,故该物质一定含C、H元素,碳元素的质量为:4.4g×格×100%=1.2g,氢元素的质量为:3.6g×k×100%=0.4g,1.2g+04g-1.6g<3.2g,故该物质中还含有氧元素。A、该物质是由分子构成的,该物质的分子是由碳原子、氢原子、氧原子构成的,不符合题意;B、由分析可知,该物质由碳、氢、氧三种元素组成,不符合题意;C、由分析可知,该物质由碳、氢、氧三种元素组成,符合题意;D、该物质中碳、氢原子个数比为:g:04g1:4.不符合题意。故选C。8.(2021·湖北黄石)下列反应的化学方程式书写正确的是A.高炉炼铁:Fe2O3+3CO高温2Fe+3CO2B.盐酸除铁锈:2Fe+6HC1=2FeC13+3H2C.小苏打治疗胃酸过多:Na2CO3+2HCl=2NaCl+H2O+CO2↑D.铝制品耐腐蚀:2Al+3O2=Al2O3【答案】A【详解】A、高炉炼铁:Fe2O3+3CO高温2Fe+3CO2,A正确。B、铁锈主要成分是氧化铁,化学方程式2Fe+6HC1=2FeC13+3H2O,B错误。C、小苏打是碳酸氢钠,化学方程式NaHCO3+HCl=NaCl+H2O+CO2↑,C错误。D、铝和氧气反应生成氧化铝,4Al+3O2=2Al2O3,D错误。故选:A。9.铜制品长期暴露在空气中表面生成铜锈【主要成分Cu2(OH)2CO3】,下列物质与铜制品生锈无关的是A.N2 B.O2 C.H2O D.CO2【答案】A【详解】表面生成铜锈主要成分Cu2(OH)2CO3,由Cu、O、H、C元素组成,不含氮元素,故与铜制品生锈无关的是氮气,故选:A。10.下列图像与事实不一致的是A. B. C. D.A.一定量的镁条在密闭容器中燃烧B.红磷在密封锥形瓶中燃烧C.用浓度为5%的过氧化氢溶液制取氧气D.用氢氧化钠与硫酸铜溶液验证质量守恒定律【答案】B【详解】A、根据质量守恒定律,一定量的镁条在密闭容器中燃烧和氧气反应生成氧化镁,固体质量变大了,反应结束后固体质量不再改变,正确;B、红磷在密封锥形瓶中燃烧,开始燃烧放出热量,温度升高,压强变大;反应结束后消耗了氧气,装置中气体减少,压强减小,反应后压强不再改变,故压强应该先变大再变小,最后不变,错误;C、用浓度为5%的过氧化氢溶液制取氧气,催化剂可以改变反应速率但是不改变生成氧气质量,故有催化剂的反应速率快,但是最后生成氧气的质量相同,图像正确;D、用氢氧化钠与硫酸铜溶液反应,反应前后元素种类质量不变,正确。故选B。11.(广西中考)在休渔期间,北海渔港停泊了大量的渔船,请回答下列问题:(1)铁制渔船表面发生锈蚀,这是因为 。(2)渔民用洗涤剂清洗机舱油污,这是利用洗涤剂 的功能。请从元素组成的角度说明“水变柴油”不可能的原因是 。(3)渔船上的木制品,为燃烧提供了 (填燃烧的条件之一)。渔船上携带有干粉灭火器,干粉主要成分是NaHCO3,受热后生成了Na2CO3、CO2和一种氧化物,请写该反应的化学方程式 。【答案】铁与氧气、水接触 乳化 化学变化中元素守恒 可燃物2NaHCO3 △ Na2CO3+H2O+CO2↑【详解】(1)铁制渔船表面发生锈蚀,这是因为铁与氧气、水接触;(2)渔民用洗涤剂清洗机舱油污,这是利用洗涤剂的乳化作用;根据质量守恒定律可知:化学反应前后元素的种类不变,“水变柴油”不可能的原因是化学变化中元素守恒;(3)渔船上的木制品,为燃烧提供了可燃物;碳酸氢钠在加热条件下反应生成碳酸钠、水、二氧化碳,化学反应方程式为2NaHCO3 △ Na2CO3+H2O+CO2↑12.为验证质量守恒定律,某同学设计了如图实验。该实验能否达到实验目的?请说明理由。【答案】不能;因为稀盐酸与硫酸钠溶液不能发生化学反应(或不能发生复分解反应》。【详解】试题分析:稀盐酸与碳酸钠溶液反应生成氯化钠、水和二氧化碳,二氧化碳会逸散到空气中导致两边的质量不相等,天平不平衡,不能用于验证质量守恒定律。13.质量守恒定律是自然科学的基本定律之一。某同学按如图装置加入稀硫酸和Na2CO3粉末,称得其总质量为m克,引发反应后可观察到的现象是 ,反应结束后称得其总质量小于m克。该同学认为此反应不符合质量守恒定律,你认为该同学的结论 (填正确错误)。【答案】有大量气泡生成错误【详解】碳酸钠和稀硫酸反应生成二氧化碳气体逸出,故观察到现象为:有大量气泡产生;该反应为化学变化,遵循质量守恒定律,反应结束后称得其总质量小于m克,是因为生成气体逸出,导致剩余物质质量减少;故该同学的结论错误。14.(2021·吉林)根据下图回答问题。(1)标号为a的仪器名称是 。(2)实验室用过氧化氢溶液与二氧化锰混合制取氧气,应选择的气体发生装置是 ,该反应的化学方程式为 。(3)若选择装置B和C组合制取某种干燥的气体,能够完成的实验是 。①氯酸钾与二氧化锰混合加热制取氧气②锌粒与稀硫酸反应制取氢气③大理石与稀盐酸反应制取二氧化碳【答案】酒精灯 B 2H2O2 MnO2 2H2O+O2↑ ②【详解】(1)标号为a的仪器名称是酒精灯;(2)实验室用过氧化氢溶液与二氧化锰混合制取氧气,药品的状态是固体和液体,反应不需要加热,故应选择的气体发生装置是B,过氧化氢在二氧化锰的催化作用下会生成水和氧气。故该反应的化学方程式为2H2O2 MnO2 2H2O+O2↑;(3)若选择装置B和C组合制取某种干燥的气体,由万用瓶收集气体是短管进气,长管出气可知,该气体的密度比空气小,易于聚集在空气的上方;①氯酸钾与二氧化锰混合加热制取氧气,氧气的密度比空气比空气大,不符合题意;②锌粒与稀硫酸反应制取氢气,氢气的密度比空气比空气小,符合题意;③大理石与稀盐酸反应制取二氧化碳,二氧化碳的密度比空气比空气大,不符合题意;故选②。15.(2021·湖北黄冈)某工厂化验室用20%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液20g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?(写出计算过程)【答案】解:设这一定量石油产品中含H2SO4的质量是xH2SO4+2NaOH=Na2SO4+2H2O98 80x 20g×20% x=4.9g答:这一定量石油产品中含H2SO4的质量是4.9g。
相关课件
这是一份第5单元 化学方程式(课件)2025年中考化学一轮复习讲练测,共60页。PPT课件主要包含了考点一质量守恒定律等内容,欢迎下载使用。
这是一份最新中考化学一轮复习讲练测课件+综合检测(人教版) 第05单元 化学方程式(课件),文件包含2023年中考化学一轮复习讲练测人教版第05单元化学方程式课件pptx、第五单元化学方程式测试-2023年中考化学一轮复习讲练测人教版原卷版docx、第五单元化学方程式测试-2023年中考化学一轮复习讲练测人教版解析版docx等3份课件配套教学资源,其中PPT共60页, 欢迎下载使用。
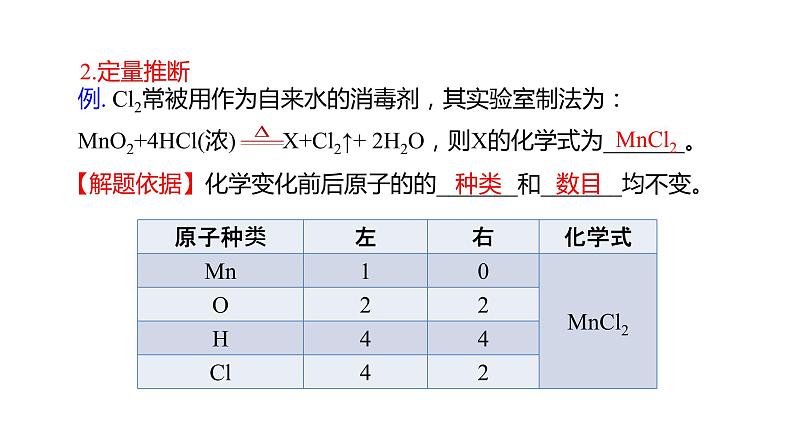
这是一份第五单元 化学方程式(课件)-2022年中考化学一轮复习讲练测(人教版),共33页。PPT课件主要包含了第五单元化学方程式,定性推断,MnCl2,定量推断,系数比,分子个数比系数比,通分将分数变为整数,图表计算题等内容,欢迎下载使用。









