

苏教版(2019)高考一轮复习考点规范练27 物质的检验、分离和提纯
展开考点规范练27 物质的检验、分离和提纯
一、选择题
1.(2021广西高三开学考试)下列叙述正确的是( )。
A.蛋白质属于天然高分子化合物,在福尔马林作用下可发生变性
B.利用乙烷和氯气在光照条件下反应可以制备纯净的C2H5Cl
C.动物油皂化反应液中加入热的饱和食盐水,析出的硬脂酸钠沉淀是肥皂的主要成分
D.利用溴水可以鉴别苯与甲苯
2.(2021广东)化学是以实验为基础的科学。下列实验操作或做法正确且能达到目的的是( )。
选项 | 操作或做法 | 目的 |
A | 将铜丝插入浓硝酸中 | 制备NO |
B | 将密闭烧瓶中的NO2降温 | 探究温度对平衡移动的影响 |
C | 将溴水滴入KI溶液中,加入乙醇并振荡 | 萃取溶液中生成的碘 |
D | 实验结束,将剩余NaCl固体放回原试剂瓶 | 节约试剂 |
3.(2021广西南宁二中三模)用如图所示装置进行下列实验,装置正确并能达到实验目的的是( )。
选项 | ①中试剂 | ②中溶液 | 实验目的 |
A | 浓硫酸、木炭粒 | 澄清石灰水 | 检验反应生成物有CO2气体 |
B | 乙醇、乙酸、浓硫酸 | 饱和碳酸钠溶液 | 制取乙酸乙酯 |
C | NaHCO3(s) | 澄清石灰水 | 验证NaHCO3(s)的热稳定性 |
D | Na2SO3(s),H2SO4 | 溴水 | 验证SO2的还原性 |
4.(2020山东)实验室分离Fe3+和Al3+的流程如下:
已知Fe3+在浓盐酸中生成黄色配离子[FeCl4]-,该配离子在乙醚(Et2O,沸点34.6 ℃)中生成缔合物Et2O·H+·[FeCl4]-。下列说法错误的是( )。
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
5.下列实验内容得出的结论正确的是( )。
选项 | 实验内容 | 结论 |
A | 某气体的水溶液能使红色石蕊试纸变蓝 | 该气体一定是NH3 |
B | 某气体能使酸性高锰酸钾溶液褪色 | 该气体一定是SO2 |
C | 某物质的水溶液中加入盐酸产生能使澄清石灰水变浑浊的无色气体 | 该溶液一定含有C |
D | 某气体完全燃烧,火焰呈淡蓝色 | 该气体一定是H2S |
6.(2021广西柳州三模)下列实验方案中,能达到实验目的的是( )。
选项 | 实验目的 | 实验方案 |
A | 比较HCl和HClO的酸性强弱 | 分别测定等浓度的HCl和HClO溶液的导电能力大小 |
B | 验证Na2S2O3是否氧化变质 | 在Na2S2O3溶液中滴加稀盐酸,然后滴加BaCl2溶液观察是否产生白色沉淀 |
C | 证明Fe2+有还原性 | 向较浓的FeCl2溶液中滴入少量酸性KMnO4溶液,观察KMnO4溶液紫色是否褪去 |
D | 比较 Ksp(AgBr)<Ksp(AgCl) | 向NaCl与NaBr混合溶液中滴加AgNO3溶液,观察是否出现淡黄色沉淀 |
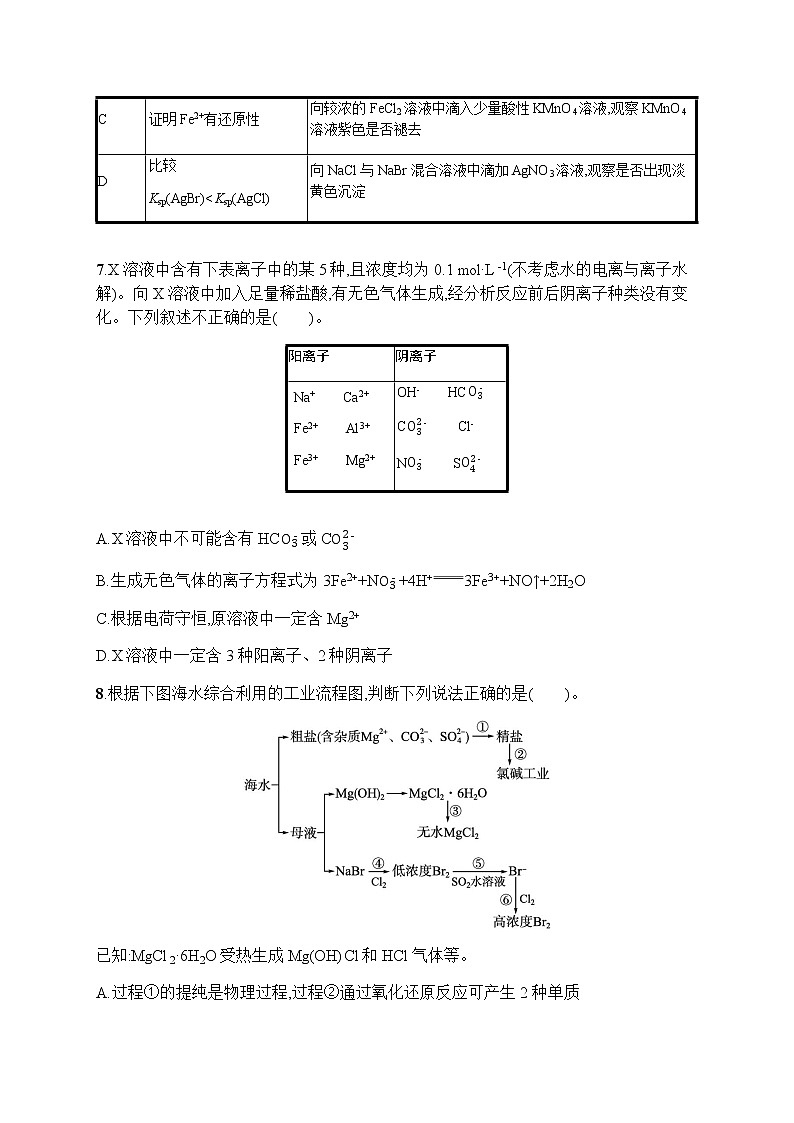
7.X溶液中含有下表离子中的某5种,且浓度均为0.1 mol·L-1(不考虑水的电离与离子水解)。向X溶液中加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化。下列叙述不正确的是( )。
阳离子 | 阴离子 |
Na+ Ca2+ Fe2+ Al3+ Fe3+ Mg2+ | OH- HC C Cl- N S |
A.X溶液中不可能含有HC或C
B.生成无色气体的离子方程式为3Fe2++N+4H+3Fe3++NO↑+2H2O
C.根据电荷守恒,原溶液中一定含Mg2+
D.X溶液中一定含3种阳离子、2种阴离子
8.根据下图海水综合利用的工业流程图,判断下列说法正确的是( )。
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2 种单质
B.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题
C.在过程④⑥反应中每氧化0.2 mol Br-需消耗2.24 L Cl2
D.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2
二、非选择题
9.(2020江苏)羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。制备少量羟基乙酸钠的反应为
ClCH2COOH+2NaOHHOCH2COONa+NaCl+H2O ΔH<0
实验步骤如下:
步骤1:在如图所示装置的反应瓶中,加入40 g氯乙酸、50 mL水,搅拌。逐步加入40%NaOH溶液,在95 ℃继续搅拌反应2小时,反应过程中控制pH约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。滤液冷却至15 ℃,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15 ℃以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A的名称是 ;逐步加入NaOH溶液的目的是 。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是 。
(3)步骤3中,粗产品溶解于过量水会导致产率 (填“增大”或“减小”);去除活性炭的操作名称是 。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是 。
10.(2021广西柳州三模)某校化学课外小组的同学依据反应S2Cl2+3Cl2+2SO24SOCl2,设计如图装置(夹持及加热装置已省略)制备SOCl2(氯化亚砜)。
相关物质的数据及性质如下表:
物质 | 主要性状 | 熔点/℃ | 沸点/℃ | 主要化学性质 |
SOCl2 | 淡黄至红色发烟液体 | -105 | 78.8 | 遇水分解, 140 ℃开始分解 |
S2Cl2 | 浅黄色油状液体 | -80 | 138 | 遇水分解,高于100 ℃时开始分解 |
回答下列问题:
(1)装置A中w管的作用是 。
(2)装置C球形冷凝管中水应从 (填“a”或“b”)处进入,冷凝管装置的作用是 ;装置C合适的加热方式是 。
(3)装置E中生成SO2的化学方程式为 。
(4)装置中碱石灰的作用是 。
(5)上述装置存在一处缺陷,导致SOCl2产率降低,改进的方法是 。
(6)反应后从装置C的反应液纯化得到SOCl2需要的玻璃仪器有:酒精灯、牛角管、锥形瓶外,还缺少 (从下列图中选择,填标号)。
考点规范练27 物质的检验、分离和提纯
1.A 蛋白质属于高分子化合物,在福尔马林作用下可发生变性,A项正确;乙烷和氯气在光照条件下的反应是连锁反应,除生成C2H5Cl外,还会生成其他氯代烷,不能得到纯净的C2H5Cl,B项错误;动物油皂化反应液中加入热的饱和食盐水,析出的硬脂酸钠是肥皂的主要成分,但不是沉淀,C项错误;苯和甲苯的密度均小于水,与溴水混合均发生萃取,无法区分,D项错误。
2.B 将铜丝插入浓硝酸中开始会产生二氧化氮,不能达到实验目的,A不符合题意;二氧化氮气体在一定条件下存在平衡:2NO2N2O4,正反应为放热反应,NO2为红棕色气体,将密闭烧瓶中的NO2降温,会使该平衡向正反应方向移动,气体颜色变浅,因此可达到实验目的,B符合题意;乙醇与水互溶,不能作碘单质的萃取剂,做法不正确,C不符合题意;一般情况下,剩余试剂需放到指定的容器中,不能放回原试剂瓶,以防污染原试剂,操作错误,D不符合题意。
3.D 浓硫酸在加热条件下与木炭反应生成CO2和SO2两种气体,都能使澄清石灰水变浑浊,故A项错误;制取乙酸乙酯时导管口应置于饱和碳酸钠溶液液面上方,不应插入液面下,以防止倒吸,故B项错误;在试管中加热固体物质时,试管口应略向下倾斜,故C项错误;Na2SO3(s)和H2SO4反应生成SO2,SO2可以使溴水褪色,体现的是SO2的还原性,故D项正确。
4.A 萃取振荡时,分液漏斗下口应倾斜向上,A项错误。分液时,密度大的液体在下层,密度小的液体在上层,下层液体由分液漏斗下口放出,下层液体放完后,密度小的上层液体从分液漏斗上口倒出,B项正确。Fe3+在浓盐酸中生成黄色配离子,该离子在乙醚中生成缔合物,乙醚与水不互溶,故分液后水相为无色,则水相中不再含有Fe3+,说明已经达到分离目的,C项正确。蒸馏时选用直形冷凝管,能使馏分全部转移到锥形瓶中,而不会残留在冷凝管中,D项正确。
5.A 某气体的水溶液能使红色石蕊试纸变蓝,说明该气体溶于水后溶液呈碱性,则该气体为氨气,A项正确。二氧化硫、乙烯等无色气体均能使酸性高锰酸钾溶液褪色,B项错误。某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该气体可能为二氧化碳、二氧化硫,则溶液中可能存在亚硫酸根离子、亚硫酸氢根离子、碳酸氢根离子等,所以该溶液中不一定存在大量C,C项错误。某气体完全燃烧,火焰呈淡蓝色,则该气体可能是H2S、氢气或甲烷等,D项错误。
6.A 强酸、强碱属于强电解质,弱酸弱碱属于弱电解质,强电解质在溶液中完全电离,弱电解质在溶液中部分电离,等浓度的HCl和HClO溶液在溶液中的电离程度不同,电离程度大的,溶液中氢离子浓度大,导电能力强,酸性也就越强,则A能达到实验目的;在Na2S2O3溶液中滴加盐酸会发生反应:Na2S2O3+2HCl2NaCl+SO2↑+S↓+H2O,产生浅黄色沉淀,会对后续白色沉淀的观察产生影响,故B不能达到实验目的;浓盐酸能与KMnO4反应,向较浓的FeCl2溶液中加少量酸性KMnO4溶液,KMnO4溶液紫色褪去可能是与Cl-反应导致的,无法证明Fe2+有还原性,故C不能达到实验目的;向1 L浓度均为0.1 mol·L-1 的NaCl和NaBr的混合溶液中滴加AgNO3溶液,先出现淡黄色沉淀,说明先生成了AgBr沉淀,即在浓度相同的前提下,溴离子优先于氯离子沉淀,所以Ksp(AgCl)>Ksp(AgBr),选项中未指明NaCl与NaBr的浓度关系,不能比较二者的Ksp,故D不能达到实验目的。
7.D 加入足量稀盐酸后,阴离子种类没有变化,说明X溶液中不含OH-、HC、C,含有Cl-,有无色气体生成,应是N与Fe2+在酸性条件下发生氧化还原反应生成NO气体:3Fe2++N+4H+3Fe3++NO↑+2H2O,因此X溶液中肯定含有N和Fe2+。由于Cl-、N、Fe2+的浓度均为0.1 mol·L-1,此时电荷已守恒,但已知X溶液中含有5种离子,则还应含有阴、阳离子各一种,阴离子只能是S,则由电荷守恒可知,阳离子可能是Ca2+或Mg2+,由于Ca2+与S不能大量共存,所以只能是Mg2+。综上所述,溶液中含有2种阳离子:Fe2+、Mg2+,3种阴离子:Cl-、N、S,故D项不正确。
8.B 过程①的提纯是通过化学反应除去杂质,A项错误。过程⑤反应生成硫酸和氢溴酸,溶液呈强酸性,生产中需解决其对设备的腐蚀问题,B项正确。在过程④⑥反应中每氧化0.2 mol Br-需消耗标准状况下的2.24 L Cl2,C项错误。MgCl2·6H2O在灼烧时会发生水解,D项错误。
9.答案 (1)(回流)冷凝管 防止升温太快、控制反应体系pH (2)防止暴沸 (3)减小 趁热过滤 (4)提高羟基乙酸钠的析出量(产率)
解析 (1)仪器A为(回流)冷凝管,因制备反应为放热反应,逐步加入NaOH溶液可防止升温太快,同时还可控制反应体系pH。
(2)沸石或碎瓷片的作用是防止暴沸。
(3)粗产品溶解于过量水会导致产率减小,因羟基乙酸钠易溶于热水,则采用趁热过滤操作以去除活性炭。
(4)因羟基乙酸钠不溶于醇,将溶液加到适量乙醇中,能提高羟基乙酸钠的析出量(产率)。
10.答案 (1)平衡气压,使浓盐酸顺利滴下
(2)a 冷凝回流SOCl2 80 ℃热水浴
(3)Cu +2H2SO4(浓)CuSO4+SO2↑+2H2O
(4)吸收SO2、Cl2等气体,防止空气中的水蒸气进入装置C
(5)将装置B中饱和食盐水换成浓硫酸(或B、C间加装盛有浓硫酸的洗气瓶)
(6)ade
解析 根据实验原理及实验装置分析,装置A是用浓盐酸和漂白粉制备氯气,B中的饱和食盐水目的是除去杂质HCl;E装置是用浓硫酸与铜反应制备二氧化硫气体,D中浓硫酸的作用是干燥二氧化硫气体;将氯气及二氧化硫气体通入C中与S2Cl2反应制备SOCl2,冷凝管的作用为冷凝回流S2Cl2和SOCl2,连接的干燥管的作用是防止空气中水分进入和剩余气体的尾气处理。
(1)根据图示装置特点分析,装置A中w管的作用是平衡气压,使浓盐酸顺利滴下;
(2)为了使冷凝水充满冷凝管,装置C球形冷凝管中水应从下端通入,即a处进入;由题干信息知SOCl2的沸点为78.8 ℃,且反应温度为80 ℃,所以冷凝管的作用是冷凝回流SOCl2;反应温度应该控制在80 ℃,所以适合的加热方式为80 ℃水浴加热;
(3)装置E中铜和浓硫酸在加热的条件下反应生成硫酸铜、SO2和水,化学方程式为:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O;
(4)根据上述分析,装置中碱石灰的作用是吸收未反应的SO2、Cl2等气体,同时防止空气中的水蒸气进入装置C;
(5)已知SOCl2易水解,在氯气进入C中时未干燥,会导致SOCl2产率降低,应该增加干燥装置;
(6)由题干信息知,SOCl2与S2Cl2沸点不同,可以用蒸馏的方法得到纯净的SOCl2,蒸馏装置所需的玻璃仪器含有蒸馏烧瓶、冷凝管、温度计,故答案为:ade。
高考化学一轮复习考点规范练29物质的检验分离和提纯 人教版(含答案解析): 这是一份高考化学一轮复习考点规范练29物质的检验分离和提纯 人教版(含答案解析),共6页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
人教版高考化学一轮复习课时练28物质的检验分离和提纯含答案: 这是一份人教版高考化学一轮复习课时练28物质的检验分离和提纯含答案
2023年高考化学一轮复习课时练35《物质的检验、分离和提纯》(含答案): 这是一份2023年高考化学一轮复习课时练35《物质的检验、分离和提纯》(含答案),共6页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。












