
2022年安徽省中考化学专项训练:工艺流程图题
展开
这是一份2022年安徽省中考化学专项训练:工艺流程图题,共13页。试卷主要包含了15/2019等内容,欢迎下载使用。
工艺流程图题
类型一 物质制备类 (5年3考,2020.15/2019.13/2017.13)
1.[2021·安徽]某燃煤电厂产生的固体废弃物粉煤灰中含有较多的氧化铝。从粉煤灰中提取氧化铝的工艺流程如图1所示。
图1
(1)“酸浸”中使用的酸是 (填序号)。
A.HCl B.H2SO4 C.Na2SO4
(2)流程中涉及的氧化物有 (写出1种即可)。
(3)“煅烧”过程发生反应的化学方程式为 ,基本反应类型是 。
(4)该工艺的价值在于 。
2.[2020·安徽]硫酸亚铁晶体是重要的化学试剂。传统制备方法是用铁屑与稀硫酸反应,因铁屑中含有硫、磷等杂质,与稀硫酸反应会产生刺鼻、呛人的有毒气体。某科技小组改用铁屑与硫酸铜溶液反应制备硫酸亚铁晶体,流程如图2所示。
图2
(1)步骤①中反应的化学方程式为 。
(2)操作Ⅰ的名称是 。步骤②涉及蒸发,蒸发时必需的仪器有铁架台(含铁圈)、酒精灯、玻璃棒、 。
(3)用硫酸铜溶液代替稀硫酸制备硫酸亚铁晶体,优点是 。
3.[2021·合肥包河一模]还原铁粉是冶金工业的重要原料,工业上利用硫酸亚铁制备还原铁粉。如图3是利用硫酸亚铁制备还原铁粉的流程图。
图3
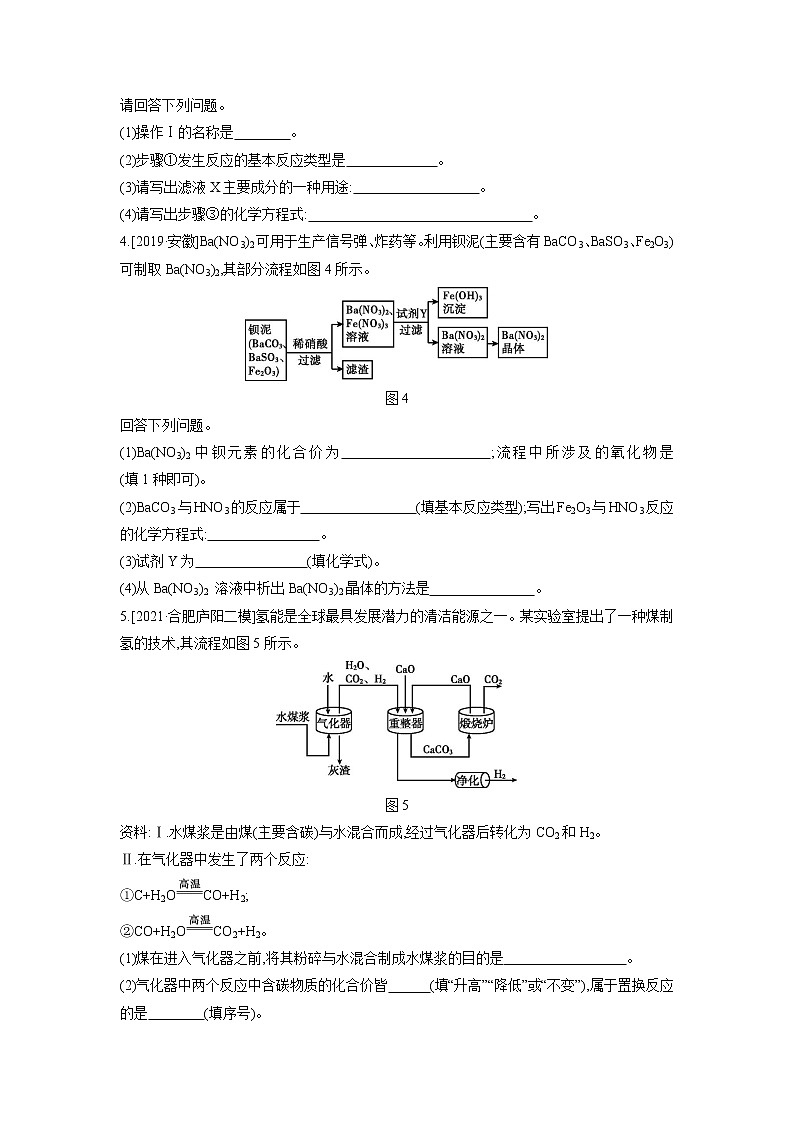
请回答下列问题。
(1)操作Ⅰ的名称是 。
(2)步骤①发生反应的基本反应类型是 。
(3)请写出滤液X主要成分的一种用途: 。
(4)请写出步骤③的化学方程式: 。
4.[2019·安徽]Ba(NO3)2可用于生产信号弹、炸药等。利用钡泥(主要含有BaCO3、BaSO3、Fe2O3)可制取Ba(NO3)2,其部分流程如图4所示。
图4
回答下列问题。
(1)Ba(NO3)2中钡元素的化合价为 ;流程中所涉及的氧化物是 (填1种即可)。
(2)BaCO3与HNO3的反应属于 (填基本反应类型);写出Fe2O3与HNO3反应的化学方程式: 。
(3)试剂Y为 (填化学式)。
(4)从Ba(NO3)2 溶液中析出Ba(NO3)2晶体的方法是 。
5.[2021·合肥庐阳二模]氢能是全球最具发展潜力的清洁能源之一。某实验室提出了一种煤制氢的技术,其流程如图5所示。
图5
资料:Ⅰ.水煤浆是由煤(主要含碳)与水混合而成,经过气化器后转化为CO2和H2。
Ⅱ.在气化器中发生了两个反应:
①C+H2OCO+H2;
②CO+H2OCO2+H2。
(1)煤在进入气化器之前,将其粉碎与水混合制成水煤浆的目的是 。
(2)气化器中两个反应中含碳物质的化合价皆 (填“升高”“降低”或“不变”),属于置换反应的是 (填序号)。
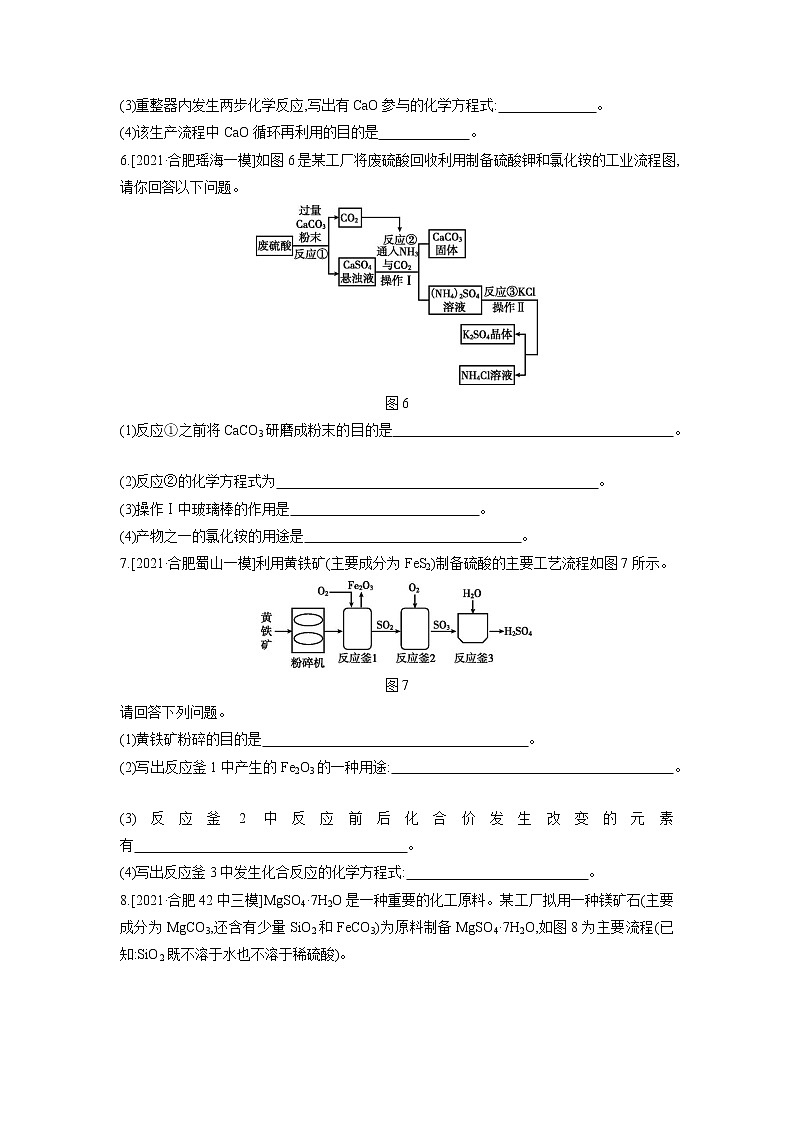
(3)重整器内发生两步化学反应,写出有CaO参与的化学方程式: 。
(4)该生产流程中CaO循环再利用的目的是 。
6.[2021·合肥瑶海一模]如图6是某工厂将废硫酸回收利用制备硫酸钾和氯化铵的工业流程图,请你回答以下问题。
图6
(1)反应①之前将CaCO3研磨成粉末的目的是 。
(2)反应②的化学方程式为 。
(3)操作Ⅰ中玻璃棒的作用是 。
(4)产物之一的氯化铵的用途是 。
7.[2021·合肥蜀山一模]利用黄铁矿(主要成分为FeS2)制备硫酸的主要工艺流程如图7所示。
图7
请回答下列问题。
(1)黄铁矿粉碎的目的是 。
(2)写出反应釜1中产生的Fe2O3的一种用途: 。
(3)反应釜2中反应前后化合价发生改变的元素有 。
(4)写出反应釜3中发生化合反应的化学方程式: 。
8.[2021·合肥42中三模]MgSO4·7H2O是一种重要的化工原料。某工厂拟用一种镁矿石(主要成分为MgCO3,还含有少量SiO2和FeCO3)为原料制备MgSO4·7H2O,如图8为主要流程(已知:SiO2既不溶于水也不溶于稀硫酸)。
图8
(1)实验室进行“操作a”的名称是 ;该操作所需要的玻璃仪器有烧杯、漏斗和 。
(2)“溶液A”含有三种溶质,除了硫酸镁外,另外两种溶质加入H2O2溶液后,一同被转化为Fe2(SO4)3溶液,该反应的化学方程式为 。
(3)流程采用“加MgO调节pH”,目的是使Fe3+转化为Fe(OH)3沉淀, (填“可以”或“不可以”)用NaOH代替MgO,理由是 。
9.[2021·合肥长丰二模]氧化镁广泛应用于国防、医药、化工、造纸、造船等行业。学校科技小组的同学以镁矿石(主要成分为MgCO3、SiO2)为原料制取氧化镁,工艺流程如图9所示。
图9
(1)操作Ⅱ的名称是 。
(2)流程中所涉及的氧化物有 (填1种即可)。
(3)步骤①中发生反应的基本反应类型是 。
(4)写出步骤②中MgSO4与NH3·H2O发生反应的化学方程式: 。
类型二 提纯回收类 (5年2考,2021.15/2018.13)
10.[2018·安徽]废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如图10所示。已知:Sn+SnCl42SnCl2。
图10
请回答下列问题。
(1)SnCl4中锡元素的化合价是 。
(2)铜的金属活动性比锡的 (填“强”或“弱”),固体A中一定含有的金属元素是 。
(3)写出步骤②发生反应的化学方程式: 。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是 (回答一点即可)。
11.[2021·合肥168中一模]废旧金属可回收利用,某化学兴趣小组用合金废料(含Fe、Cu和Al)制取FeSO4溶液和回收金属铜,实验流程如图11所示(部分生成物已略去)。已知:2Al+2NaOH+2H2O2NaAlO2+3H2↑。
图11
(1)铁的金属活动性比铜 (填“强”或“弱”)。
(2)操作Ⅱ用到的玻璃仪器有烧杯、漏斗和 (填仪器名称)。
(3)步骤B发生反应的化学方程式为 ,该反应属于基本反应类型中的 反应。
(4)铝制品在空气中耐腐蚀的原因是 。
12.[2021·合肥45中一模]利用废旧电池铜帽(含铜和锌),制取海绵铜(Cu),并得到硫酸锌溶液E,主要流程如图12所示(反应条件已略去)。已知:2Cu+O2+2H2SO42CuSO4+2H2O。
图12
(1)流程中氧气是利用工业分离液态空气得到的,该过程是 (填“物理变化”或“化学变化”)。
(2)生产中通常要先将电池铜帽粉碎处理,这样做的目的是 。
(3)步骤Ⅱ的操作名称是 ,该操作中玻璃棒的作用是 。
(4)加入物质B发生反应的化学方程式为 (任写一个)。
(5)海绵铜在很多方面可以代替铜来使用,铜在生活中的用途是 。
13.黄铜是以Zn为主要添加元素的铜合金。黄铜渣中约含Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质。某工厂处理黄铜渣可得到硫酸锌晶体,其主要流程如图13所示(杂质不溶于水,不参与反应)。
已知:ZnO+H2SO4ZnSO4+H2O,CuO+H2SO4CuSO4+H2O。
图13
(1)步骤Ⅰ中需要通风并远离火源,其原因是 。
(2)步骤Ⅰ中产生气体的化学方程式是 。
(3)溶液A中的阳离子有 (填离子符号)。
(4)固体B是 (填“纯净物”或“混合物”)。
(5)溶液A的质量 (填“>”“
相关试卷
这是一份专题20 工艺流程图题:三年(2021-2023)中考化学真题分项汇编(全国通用),文件包含专题20工艺流程图题三年2021-2023中考化学真题分项汇编全国通用原卷版docx、专题20工艺流程图题三年2021-2023中考化学真题分项汇编全国通用解析版docx等2份试卷配套教学资源,其中试卷共43页, 欢迎下载使用。
这是一份中考化学三轮冲刺压轴题 专题05 化学工艺与流程图(讲练测)(含解析),共35页。
这是一份中考化学复习课前小测第25课时工艺流程图题含答案,共2页。









