






浙江专用高中化学课时检测23离子键课件新人教版必修第一册
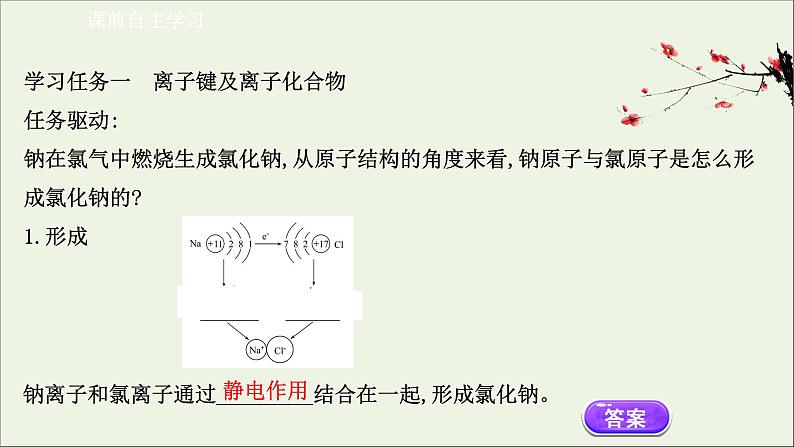
展开学习任务一 离子键及离子化合物任务驱动:钠在氯气中燃烧生成氯化钠,从原子结构的角度来看,钠原子与氯原子是怎么形成氯化钠的?1.形成
钠离子和氯离子通过_________结合在一起,形成氯化钠。
(1)含义:_______________之间的相互作用称为离子键。(2)成键粒子:_______和_______。(3)成键元素:一般是_________元素和___________元素。2.离子化合物(1)含义:由_______构成的化合物。(2)常见物质①绝大多数盐,如____、_____、_____等。②强碱,如_____、Ba(OH)2等。③碱性氧化物,如____、____等。
【想一想】1.静电作用是否是指静电引力?提示:静电作用包括:①带正电的离子与带负电的离子间的吸引作用;②原子核与原子核、核外电子与核外电子间的排斥作用;③原子核与核外电子间的吸引作用。2.活泼金属元素原子与活泼非金属元素原子之间一定形成离子键吗?提示:不一定。AlCl3中Al与Cl之间形成的是共价键。
学习任务二 电子式任务驱动:元素的化学性质主要取决于最外层电子数,怎么用符号(电子式)来表示离子化合物的形成过程呢?1.电子式在_________周围用“___”或“___”来表示原子的最外层电子,以简明地表示原子、离子的最外电子层的电子排布,这种式子称为电子式。例如:Mg:______,Cl: 。2.用电子式表示离子化合物的形成过程NaCl:
【做一做】写出以下微粒的电子式。
探究任务 离子键和离子化合物科技情境氯离子和钠离子可以构成氯化钠这种离子化合物。离子化合物的种类很多,绝大多数盐都属于离子化合物,熔融盐燃料电池具有较高的发电效率,有着长远的发展前景。
【问题探究】1.哪些微粒间易形成离子键?提示:第ⅠA族、第ⅡA族的金属元素的单质与第ⅥA族、第ⅦA族的非金属元素的单质发生反应时,一般通过离子键形成离子化合物;金属阳离子与某些原子团(如 、 、 、OH-等)之间,通过离子键形成离子化合物;铵根离子与酸根(或酸式酸根)离子之间形成离子键,构成离子化合物;活泼金属的氧化物、过氧化物(如Na2O2)中存在离子键。
2.离子化合物中一定含金属元素吗?含金属元素的化合物一定是离子化合物吗?提示:离子化合物中不一定含有金属元素,如氯化铵、硝酸铵等;含有金属元素的化合物不一定是离子化合物,如氯化铝等。
【探究总结】1.离子键的三个“一定”和两个“不一定”(1)三个“一定”。①离子化合物中一定含有离子键。②含有离子键的物质一定是离子化合物。③离子化合物中一定含有阴离子和阳离子。(2)两个“不一定”。①离子化合物中不一定含有金属元素,如NH4Cl、NH4NO3等。②含有金属元素的化合物不一定是离子化合物,如AlCl3。
【探究特训】1.下列原子序数所对应的元素组中,两者可形成离子键的是( )A.1和17 B.12和9C.14和6D.15和8【解析】选B。根据离子键的形成条件,活泼金属元素与活泼非金属元素一般形成离子键,根据原子序数,B项中分别是Mg和F,符合题意。
2.(2020·海口高一检测)下列离子化合物的电子式书写正确的是( )
【解析】选D。A项不正确,每个离子均要单独写,不能合并在一起表示,应改为 。离子电荷表示法(如R2-)与化合价表示法(如 )不同。“2-”表示带两个单位负电荷,而“-2”则表示化合价为-2。另外,化合价应写在元素符号正上方,B项不正确,应改为 。简单阳离子符号不用“[ ]”,只用离子符号表示即可,C项不正确,应改为 。
【补偿训练】(2019·锦西高一检测)有关离子键和离子化合物有很多说法。(1)凡含离子键的化合物,一定含金属元素,这种说法是否正确?提示:不正确。NH4Cl晶体中含有离子键,但不含金属元素。(2)在化合物BaCl2中,两个氯离子之间是否存在离子键?提示:离子键必须是阴、阳离子间的相互作用,两个氯离子之间不存在离子键。(3)离子化合物一定能导电吗?提示:离子化合物处于晶体状态时不能导电,只有在熔融状态或溶于水时才能导电。
(4)原子序数为11与9的元素能够形成离子键吗?提示:原子序数为11与9的元素分别是Na、F,属于活泼金属元素与活泼非金属元素,可形成离子键。(5)用电子式表示BaCl2、NaF的形成过程。提示:
1.(2020·成都高一检测)固体A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,则下列有关说法中不正确的是( )A.1 ml NH5中含有5NA个N—H键(NA表示阿伏加德罗常数)B.NH5是离子化合物C.NH5的电子式为D.NH5与水反应的化学方程式为NH5+H2O====NH3·H2O+H2↑
【解析】选A。根据NH5中各原子的最外层都符合相应的稀有气体原子的最外层电子结构可知,A只能是 与H-通过离子键结合的离子化合物,其电子式为 ,其中 内部存在N—H键,因此1 ml NH5中含有4NA个N—H键。H-具有很强的还原性,能与H2O发生氧化还原反应:NH5+H2O====NH3·H2O+H2↑。
2.下列关于离子化合物的叙述正确的是( )A.离子化合物中都含有离子键B.离子化合物中的阳离子只能是金属离子C.离子化合物一定可以导电D.溶于水可以导电的化合物一定是离子化合物【解析】选A。离子化合物的构成粒子为阴、阳离子,一定含有离子键,A正确;离子化合物中的阳离子可以全部由非金属元素构成,如铵盐,B错误;离子化合物在熔融状态或水溶液中能导电,固态时不导电,C错误;溶于水可以导电的化合物不一定为离子化合物,如HCl等,D错误。
【易错提醒】离子化合物熔融状态下一定导电,其晶体不导电。
【补偿训练】1.A、B两元素的原子序数分别为11和8,两者化合生成离子化合物Z,则下列说法中正确的是( )A.A一定形成+1价的阳离子B.B一定形成-2价的单核阴离子C.Z一定能与水反应产生B单质D.Z一定是A2B型化合物【解析】选A。原子序数为11和8的元素分别为Na和O,两者化合可生成离子化合物Na2O或Na2O2,它们都能与水反应,但只有Na2O2能产生O2。
2.以下叙述中,错误的是( )A.钠原子和氯原子作用生成NaCl后,其结构的稳定性增强B.在氯化钠中,除氯离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用C.任何离子键在形成的过程中必定有电子的得与失D.金属钠与氯气反应生成氯化钠后,体系能量降低【解析】选C。活泼的金属原子和活泼的非金属原子之间形成离子化合物,阳离子和阴离子均达稳定结构,这样体系的能量降低,其结构的稳定性增强,故A、D正确,B也正确。离子键的形成只是阴、阳离子间的静电作用,并不一定发生电子的得失,如Na+与OH-结合成NaOH,故C错误。
3.(双选)(2020·济南高一检测)传说老子过函谷关之前,关尹喜见有紫气从东而来,知道将有圣人过关, 果然老子骑着青牛而来,后来人们用“紫气东来”比喻吉祥的征兆。碘晶体受热转变成碘蒸气也有紫气东来之象。下列关于碘等物质的说法中正确的是( )
A.HCl溶于水能电离出H+、Cl-,所以HCl是离子化合物B.碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力C.NaI属于离子化合物D.NaHCO3受热分解生成Na2CO3、CO2和H2O,既破坏了离子键,也破坏了共价键
【解析】选C、D。HCl属于共价化合物,属于电解质,在溶液中可发生电离,故A错误;碘晶体受热转变成碘蒸气,克服分子间作用力,而碘原子间的作用力属于共价键,故B错误;Na是活泼金属元素,与I2反应生成的NaI属于离子化合物,故C正确;NaHCO3为离子化合物,含有离子键和共价键,受热分解生成Na2CO3、CO2和H2O,阴阳离子间的离子键断裂,也破坏了共价键,故D正确。
4.按要求完成下列填空:(1)一核10电子的原子的电子式__________。 (2)双核10电子的阴离子的电子式__________。 (3)五核10电子的阳离子的电子式__________。 (4)XY2型的离子化合物,X所在的族为__________,Y所在族为__________。 (5)用电子式表示K2S的形成过程______________________________。
【解析】(1)一核10电子的原子即质子数为10的元素为Ne,电子式为 。(2)双核10电子的阴离子为OH-,电子式为 。(3)五核10电子的阳离子是 ,电子式为 。(4)一般位于第ⅠA、ⅡA族的活泼金属与位于第ⅥA、ⅦA族的活泼非金属形成离子化合物,XY2型的离子化合物中的化合价为 ,故X为第ⅡA族,Y为第ⅦA族。(5)
浙江专用高中化学课时检测1物质的分类课件新人教版必修第一册: 这是一份浙江专用高中化学课时检测1物质的分类课件新人教版必修第一册,共60页。PPT课件主要包含了课前自主学习,同一种元素,C60,混合物,~100,FeCl3饱和溶液,一条光亮的“通,丁达尔效应,课堂合作探究,酸能和活泼金属反等内容,欢迎下载使用。
浙江专用高中化学课时检测24共价键课件新人教版必修第一册: 这是一份浙江专用高中化学课时检测24共价键课件新人教版必修第一册,共49页。PPT课件主要包含了课前自主学习,共用电子对,共价化合物,电子式,旧化学键,新化学键,HCl,分子聚集在一起,化学键,课堂合作探究等内容,欢迎下载使用。
浙江专用高中化学课时检测19核素课件新人教版必修第一册: 这是一份浙江专用高中化学课时检测19核素课件新人教版必修第一册,共60页。PPT课件主要包含了课前自主学习,编排原则,元素周期表的结构,质子数,中子数,课堂合作探究,元素周期表,纵行16个,第4-7周期,横行7个等内容,欢迎下载使用。












