
2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期末试卷(通用)
展开最新人教版九年级上册化学第六单元碳和碳的氧化物期末试卷(通用)
(考试时间:90分钟,总分100分)
班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
1、下列关于物质反应现象的描述中,正确的是
A.含碳燃料不充分燃烧产生黑烟
B.硫在空气中燃烧产生明亮的蓝紫色火焰
C.软水中加入肥皂水振荡后泡沫少、浮渣多
D.在二氧化碳中变红的石蕊小花烘干后变回无色
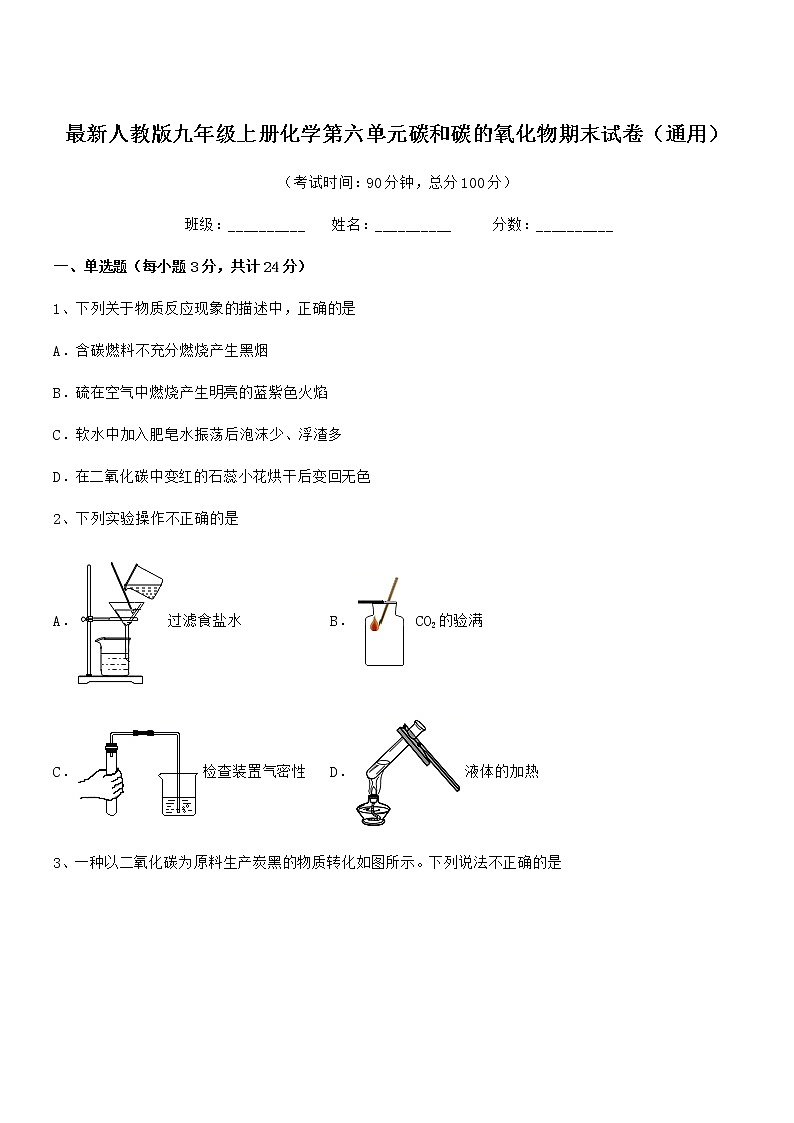
2、下列实验操作不正确的是
A.过滤食盐水 B.CO2的验满
C.检查装置气密性 D.液体的加热
3、一种以二氧化碳为原料生产炭黑的物质转化如图所示。下列说法不正确的是
A.反应Ⅰ发生后,固体物质所含铁元素质量分数变大
B.反应Ⅱ发生后,碳元素化合价降低
C.反应Ⅱ中,FeO与C的质量比为18:1
D.整个循环过程可将CO2转化为C和O2
4、物质的用途只利用其物理性质的是
A.氧气用于气焊 B.焦炭用于冶炼金属
C.干冰用于灭火 D.稀有气体用于电光源
5、下列用途既利用其物理性质又利用其化学性质的是
A.活性炭用于防毒面具吸附毒气 B.干冰用于人工降雨
C.一氧化碳作燃料 D.二氧化碳用于灭火
6、某小组利用如图装置进行创新实验。实验时,先加热炭粉,一段时间后将酒精喷灯移至CuO处加热。下列说法错误的是
A.实验过程中,CO2既是反应物,又是生成物
B.气球可以收集尾气,防止污染空气
C.反应过程中,固体由黑色变为红色
D.装置内发生的化学反应:
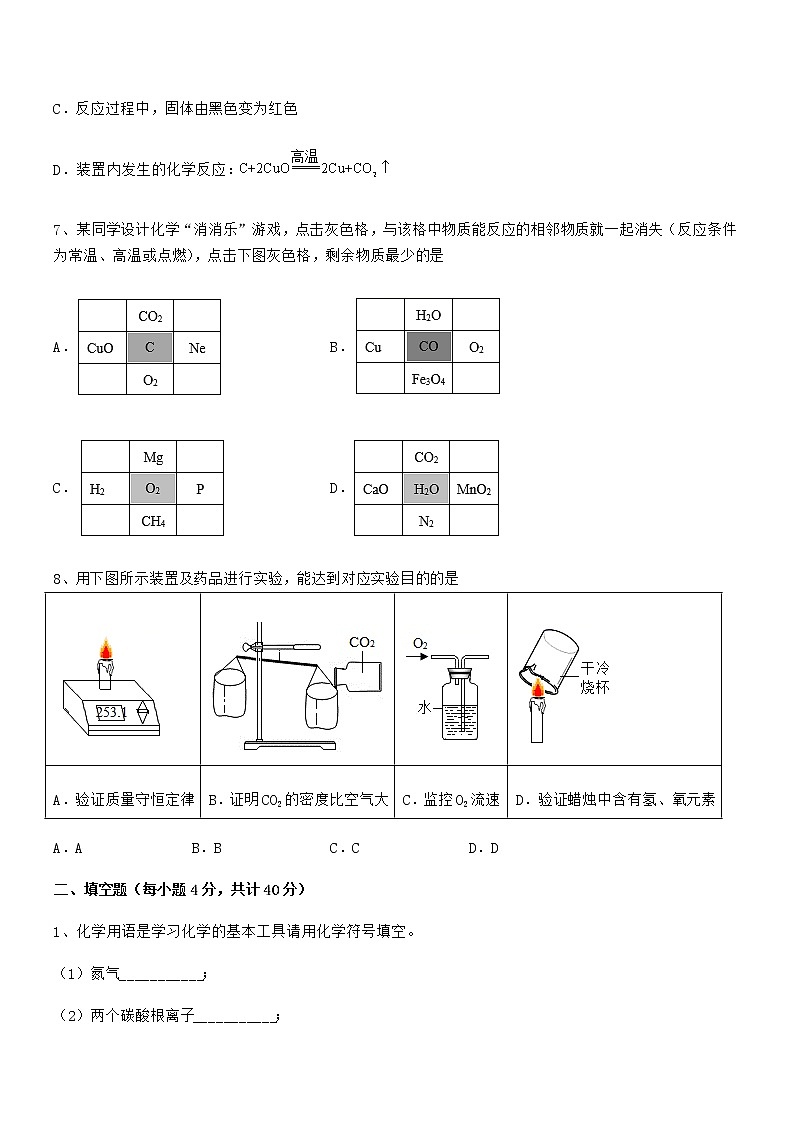
7、某同学设计化学“消消乐”游戏,点击灰色格,与该格中物质能反应的相邻物质就一起消失(反应条件为常温、高温或点燃),点击下图灰色格,剩余物质最少的是
A. B.
C. D.
8、用下图所示装置及药品进行实验,能达到对应实验目的的是
A.验证质量守恒定律 | B.证明CO2的密度比空气大 | C.监控O2流速 | D.验证蜡烛中含有氢、氧元素 |
A.A B.B C.C D.D
二、填空题(每小题4分,共计40分)
1、化学用语是学习化学的基本工具请用化学符号填空。
(1)氮气___________;
(2)两个碳酸根离子___________;
(3)氧化铝中铝元素显+3价___________;
(4)自然界中最硬的物质的化学式是___________;
(5)淡黄色固体燃烧后生成有刺激性气味的气体的化学式为___________;
(6)人体中含量最多的金属元素是___________。
2、某同学用如图装置,进行有关碳及其氧化物的实验(图中夹持已略去),在完成气密性检査后加入药品,并已在装置中充满二氧化碳。
(1)填写表格中的空白内容:
实验步骤 | 实验现象 | 实验分析 |
①缓缓通入CO2,点燃A处酒精喷灯,加热一段时间 | 木炭粉减少,D中有气泡产生,澄清石灰水______且D装置中的液体进入到E装置。 | 硬质玻璃管中A处发生反应的化学方程式为:______ |
②点燃B处酒精喷灯,加热一段时间 | B处玻璃管内______ | 以上实验说明______具有还原性 |
③停止通入二氧化碳,熄灭A、B两处的火焰 | C中有D中液体进入 | C装置的作用是:______ |
(2)有同学认为该装罝需要添加尾气处理装置,你认为是否需要并说明理由:______。
(3)写出D处集气瓶内发生反应的化学反应方程式______。
3、我国科学家以二氧化碳、氢气为原料,通过十步反应制得淀粉[化学式为(C6H10O5)n],实现了二氧化碳到淀粉的人工合成。
(1)二氧化碳、氢气、淀粉三种物质中,属于单质的是______。
(2)关于二氧化碳合成淀粉的意义,下列说法正确的是______(填序号)。
a.能够消耗二氧化碳,将有助于减少温室效应
b.能够合成淀粉,将有利于解决粮食短缺问题
4、小强是个爱思考的同学,他以化合价为纵坐标,以物质类别为横坐标绘制图象,这种图象叫价类图。如图是有关碳的价类图,回答下列问题。
(1)A在自然界存在多种单质,其物理性质差异很大,请从微观角度解释原因______。
(2)B点表示的物质的化学式为______。
(3)能够表示碳酸的点是______。(选填“A~E”)
(4)C点转化为碳酸钙的化学方程式为______。
5、下图是初中化学部分物质间相互转化关系图,“→”表示物质间存在转化关系,部分反应物、生成物或反应条件已略去,请结合关系图回答下列问题。
(1)由此关系图可推知水有_______点化学性质。
(2)在CO2→CO的反应中表现出CO2的_______性。
(3)H2、CO都有可燃性和还原性,都可通过________反应(填基本反应类型)生成对应的氧化物。
(4)请写出下列物质间转化的化学方程式。
CaCO3→CO2:_________;
Ca(OH)2→H2O:________。
6、实验室制取并收集二氧化碳,选用______(填数字符号)组合,化学方程式为______,收集装置不能采用另外两个装置的原因是______。
7、从A或B两题中任选一个做答,若两题均作答,按A计分。
A | B |
固体二氧化碳的用途之一是______。 | 固体二氧化碳的俗称是______。 |
8、从下列选项中选择一种适当的物质填空,并将字母序号填写在横线上。
A.石墨 B.金刚石 C.乙醇 D.稀有气体 E.一氧化碳 F.炭黑
(1)可用来治炼金属的是_____________。
(2)用于多种电光源的是_____________。
(3)添加到橡胶中,增强耐磨性的_____________。
(4)可作干电池电极的是_____________。
(5)可用于裁切玻璃的是_____________。
(6)充分燃烧时,可生成两种氧化物的是_____________。
9、请用下列物质的序号填空:
A.干冰 B.氖气 C.金刚石 D.氮气 E.氧气
(1)占空气体积约78%的气体是___________;
(2)可用于人工降雨的是___________;
(3)天然最硬的物质是___________;
(4)用于医疗急救的是___________;
(5)可用作电光源的是___________。
10、每年的3月22日是“世界水日”,水与人类的生产、生活密切相关。
(1)水是由 ___________ (填“分子”、“原子”或“离子”)构成的化合物。
(2)二氧化氯ClO2是一种常用的自来水消毒剂。将Cl2通入NaClO2溶液中可制得ClO2和一种生活中常见的盐,反应的化学方程式为Cl2+2 NaClO2 =2X+2ClO2,其中X的化学式为 ___________ 。
(3)区分软水和硬水通常加入 ___________ 来检测。加入 ___________ 除去水中的色素和异味。
(4)通过电解水的实验可以得出结论:水是由___________组成的,二者的质量比为___________。
三、计算题(每小题4分,共计36分)
1、小红同学知道了鸡蛋壳的主要成分是碳酸钙,为了测定鸡蛋壳中碳酸钙的含量,她收集了5.5g的干燥鸡蛋壳,研碎后与足量稀盐酸在烧杯中反应(杂质不与盐酸反应),烧杯和稀盐酸总质量为150g。充分反应后,烧杯和剩余物总质量为153.3g。请计算:
(1)反应生成CO2的质量。
(2)鸡蛋壳中碳酸钙的质量分数(计算结果精确到小数点后一位)。
2、学习小组的同学在实验室中制取二氧化碳,称取12g大理石样品,将80g稀盐酸分4次加入样品中(假设杂质不参与反应,也不溶于水),测得实验数据如下:
次数 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 9 | 6 | 3 | 2 |
请完成下列分析与计算:
(1)12g大理石样品中碳酸钙的质量为___________g。
(2)实验结束时制得二氧化碳的质量为多少?
3、某课外活动小组的同学欲测定一种大理石样品中碳酸钙的含量,他们称取25.0g大理右样品,放入盛有100g一定浓度的稀盐酸(足量)的烧杯中,并且隔一定时间使用精确的电子天平称出烧杯中物质的质量,记录如下表:
时间 | T1 | T2 | T3 | T4 | T5 |
烧杯中物质的质量/g | 122.8 | 120.6 | 118.4 | 116.2 | 116.2 |
请计算:
(1)测定过程中产生二氧化碳的质量为________;
(2)大理石样品中碳酸钙的质量分数为多少?
4、为检验某石灰石样品中碳酸钙的质量分数,取该样品25g放入烧杯,将100g稀盐酸分5次加入烧杯中(杂质不与稀盐酸反应),加入稀盐酸的质量与反应后烧杯中剩余物质质量关系如下表所示,请回答以下问题:
实验次数 | 1 | 2 | 3 | 4 | 5 |
稀盐酸质量/g | 20 | 20 | 20 | 20 | 20 |
烧杯中剩余物质质量/g | 42.8 | a | 78.4 | 96.2 | 116.2 |
(1)表中a=______;
(2)反应结束后,生成CO2的质量是______g;
(3)计算该石灰石样品中碳酸钙的质量分数。(请写出计算过程)
(4)请在下图中画出生成CO2质量与加入稀盐酸质量的关系。(标上必要的数据)
5、实验室常用石灰石与稀盐酸反应制取二氧化碳。为了测定石灰石中碳酸钙的含量,小乐进行了如下实验:取12.0g石灰石放于烧杯中,向烧杯中滴加稀盐酸,实验测得烧杯中剩余物质的质量与加入稀盐酸的质量之间的关系如图所示。整个过程不考虑稀盐酸的挥发和气体的溶解,石灰石中的杂质也不与稀盐酸反应。求:
(1)产生CO2的总质量为______g
(2)石灰石中碳酸钙的质量分数(写出计算过程)
6、某学校的学习小组对当地的石灰石矿区进行调查,欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16 g,把80 g稀盐酸分四次加入,实验过程中所得数据如下表。(已知石灰石样品中含有的二氧化硅等杂质不溶于水,也不与稀盐酸反应)
加入次数 | 加入稀盐酸的质量/g | 剩余固体的质量/g |
1 | 20 | 11 |
2 | 20 | 6 |
3 | 20 | 2.4 |
4 | 20 | n |
根据实验数据计算:
(1)表中n的数值为___________。
(2)样品中碳酸钙的质量分数是___________。
(3)取50 kg这种石灰石高温煅烧,可得含杂质的氧化钙多少千克?
7、为测定某种贝壳中碳酸钙的含量,取25g贝壳,将贝壳研碎,逐渐加入稀盐酸,用玻璃棒不断搅拌,测得生成气体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)。请完全下列问题:
(1)将贝壳研碎,并用玻璃棒不断搅拌,目的是_______。
(2)反应生成气体的质量为_______g。
(3)请计算这种贝壳中碳酸钙的质量分数_____(写出计算过程)
8、某化学兴趣小组为测定某石灰石样品中碳酸钙的含量(杂质不溶于水,也不与其它物质反应,受热也不分解)进行如图所示的实验。请根据以下信息回答问题:
(1)上述实验过程中发生反应的化学方程式为 __________。
(2)生成CO2的质量是 多少。
(3)m的数值 。
9、小军同学去我县大仙岩风景区游玩,带回了若干块石灰石样品,他采用了以下方法对样品中碳酸钙的质量分数进行检测:取这种石灰石样品6g,把40g稀盐酸分四次加入,测量过程所得数据如下(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应)。
加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 10 | 10 | 10 | 10 |
剩余固体的质量/g | 4.0 | 2.0 | 0.6 | 0.6 |
求:
(1)6g石灰石样品中含有的杂质为______g。
(2)样品中碳酸钙的质量分数为_________。
(3)实验室用100g这种纯度的石灰石与足量的稀盐酸反应,可得到二氧化碳_____g?(写出计算过程)(化学方程式:CaCO3+2HCl=CaCl2+CO2↑+H2O)
2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期末考试卷【最新】: 这是一份2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期末考试卷【最新】,共10页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。
2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期末复习试卷【汇总】: 这是一份2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期末复习试卷【汇总】,共11页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。
2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期末试卷(学生专用): 这是一份2022年最新人教版九年级上册化学第六单元碳和碳的氧化物期末试卷(学生专用),共11页。试卷主要包含了单选题,填空题,计算题等内容,欢迎下载使用。












