

2021年最新人教版九年级化学下册第九单元溶液期末试卷(A4可打印)
展开班级:__________ 姓名:__________ 分数:__________
一、单选题(每小题3分,共计24分)
1、不能达到实验目的的是
A.AB.BC.CD.D
2、如图是甲、乙两种圉体物质在水中的溶解度曲线。下列说法正确的是
A.甲、乙两物质的溶解度相等
B.由t2℃降温到t1℃,甲饱和溶液比乙饱和溶液析出晶体的质量多
C.t2℃时,将40g甲物质加入50g水中,充分溶解后溶液的质量为90g
D.t2℃时,用甲、乙配制等质量的饱和溶液,甲所需要水的质量比乙少
3、下列饮料中,不属于溶液的是
A.啤酒B.汽水C.冰红茶D.酸奶
4、下列有关溶液的说法错误的是
A.溶液是均一、稳定的混合物
B.溶液中的溶质可以是固体、液体或气体
C.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
D.氯化钠溶于水就是钠离子和氯离子在水分子作用下均匀扩散到水中的过程
5、属于溶液的是
A.蒸馏水B.矿泉水C.泥沙水D.油水
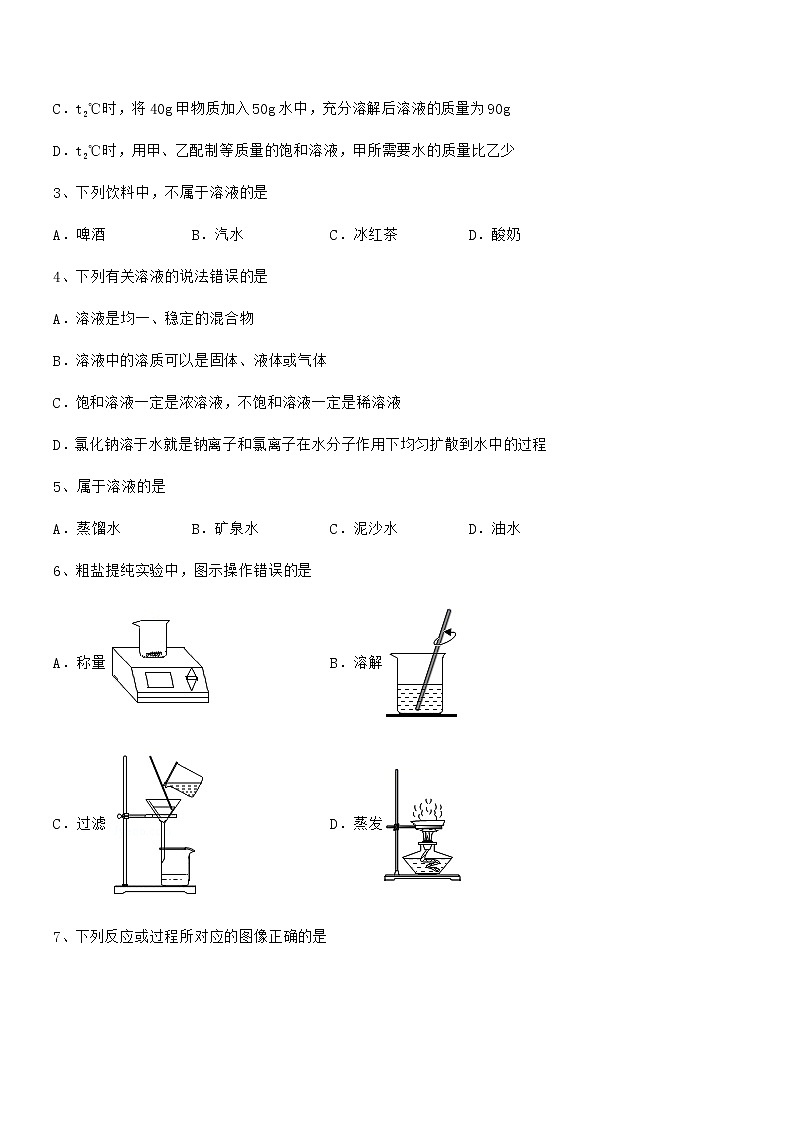
6、粗盐提纯实验中,图示操作错误的是
A.称量B.溶解
C.过滤D.蒸发
7、下列反应或过程所对应的图像正确的是
A. 电解一定质量的水
B. 向等质量的锌粉和铁粉中分别加入足量等浓度的稀盐酸
C. 用两份质量相等、浓度相同的过氧化氢溶液分别制取氧气
D. 向一定质量的硝酸银溶液中加入铜粉
8、察尔汗盐湖是我国西北地区最大的咸水湖,其中含有大量的碳酸钠和氯化钠。如图为两物质的溶解度曲线,下列有关叙述正确的是
A.碳酸钠的溶解度大于氯化钠
B.t2℃时,可以配制溶质质量分数为40%的碳酸钠溶液
C.将t2℃时两种物质的饱和溶液降温至t1℃,碳酸钠析出的固体较多
D.夏天晒盐可以得到氯化钠,冬天捞碱可以得到碳酸钠
二、填空题(每小题4分,共计20分)
1、化学与人类生活、生产息息相关。请回答下列问题:
(1)天然气燃烧的化学方程式_____,燃烧时_____能转化为_____能。
(2)用灯帽盖灭酒精灯火焰的原理是_____。
(3)用洗洁精除去餐具上的油污是因为洗洁精在水中对油污具有_____作用。
(4)家庭用净水器利用活性炭的_____性,除去有色有味的杂质。
2、海水中含有多种物质,某地海水中主要物顶含量如表1,表2为相关物质溶解度。
表1
表2
(1)20℃时,氯化钠的溶解度______硫酸钠的溶解度(填“>”“=”或“<”);
(2)100℃时,硫酸钠的溶解度为______g/100g水;
(3)晒干100g上述海水,所得固体中氯化钠的质量为______g,某化学兴趣小组欲从所得固体中提纯氯化钠,进行如下操作。
(4)步骤1的名称为______;
(5)如图表示步骤3过程中蒸发时间和析出固体的关系,由此可知,步骤2蒸发后所得氯化钠溶液是______(填“饱和”或“不饱和”)溶液;
(6)为了得到尽可能多的纯净的氯化钠,理论上蒸发掉的水的质量约为______g(结果保留一位小数)。
3、硝酸钾、氯化钾的溶解度曲线如图所示。
(1)t2℃时硝酸钾的溶解度为______g/100g水,P点的含义是______。
(2)若硝酸钾中混有少量的氯化钾,可采用______的方法提纯硝酸钾(填“蒸发结晶”或“降温结晶”)。
(3)t2℃时,将30g氯化钾加入到50g水中,充分溶解后形成的溶液的是______(填“饱和溶液”或“不饱和溶液“),其溶液的溶质质量分数为______(结果精确到0.1%)。
(4)将接近饱和的硝酸钾溶液转化为饱和溶液的方法是______(写二种方法)。
(5)t2℃相同质量的硝酸钾和氯化钾饱和溶液,降至t1℃时,析出晶体的质量,硝酸钾______氯化钾(填“大于“或“小于”或"等于”),t2℃,分别将100g和50g两份硝酸钾饱和溶液蒸发10g水,恢复到t2℃,析出晶体的质量,前者______后者(填“大于“或“小于“或“等于“)。
4、下表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答下列问题:
(1)10℃时,KNO3溶解度是____。
(2)T℃时,NaCl和KNO3的饱和溶液溶质的质量分数相同,该温度范围是____。
(3)向50mL水中溶解一定量KNO3固体的操作如图,请根据实验现象和溶解度数据回答:
A、B、C中溶液一定是不饱和溶液的是____;当x=____g时,B中恰好没有固体剩余。
5、正确读写化学符号是学好化学的基础,请回答下列问题。
(1)镁元素的符号为_______;
(2)三个碳酸根离子可用符号表示为________;
(3)保持氧气化学性质的最小粒子是______;
(4)硫酸铜溶液中溶剂的化学式为________。
三、计算题(每小题4分,共计36分)
1、为了测定石灰石中碳酸钙的质量分数(杂质不含钙元素,不溶于水,也不与其他物质发生反应),进行了如下实验。请回答下列问题。
(1)上述实验过程中发生反应的化学方程式为_________。
(2)此石灰石中碳酸钙的质量分数为__________。
(3)若向反应后的滤液中加入 10.8g 水,则所得溶液中溶质的质量分数为__________。
2、实验室常用 3%的过氧化氢溶液制备氧气。
(1)欲配置 100g 3%的过氧化氢溶液,需取用 10%的过氧化氢溶液____________mL。
(2)含 0.04ml 溶质的过氧化氢溶液完全反应,能产生多少克的氧气___________?(根据化学方程式列式计算)
(3)反应结束后,发生装置内剩余气体的主要成分为氧气,请设计实验方案,收集该剩余气体______________。
3、某食品加工厂生产的酱油中氯化钠的质量分数为15%~18%,该厂日产酱油15t。试计算该厂每月(按30天计)消耗氯化钠的质量。
4、实验室常用锌与稀硫酸反应来制取氢气,反应原理为Zn+H2SO4=ZnSO4+H2↑。某同学取锌粒13g,加入200g稀硫酸中,恰好完全反应,气体全部逸出,反应后溶液的质量为212.6g。试计算所用稀硫酸中溶质的质量分数。
5、将20.0g稀盐酸逐滴加入到10.0g溶质质量分数为4.0%的氢氧化钠溶液中,边滴加边搅拌随着稀盐酸的滴加,溶液的pH变化情况如图所示,溶液的温度变化如表所示(不考虑反应过程中热量散失)。
(1)当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是_________℃。
(2)计算稀盐酸溶质的质量分数(精确到0.1%)。
6、在抗击新型冠状病毒肺炎疫情中,“84消毒液”(含次氯酸钠(NaC1O)和氯化钠)是一种常用的消毒剂。请回答下列问题:
(1)“84消毒液”属于______(填“纯净物”或“混合物”),次氯酸钠中Na、Cl、O三种元素的质量比为______。
(2)在200.0g NaClO质量分数为20.0%的“84消毒液”中, NaClO的质量为______g,该消毒液中+1价C1的质量分数为______%(计算结果精确到0.1%)。
7、某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的组成,取黄铜样品50g放入锥形瓶中,向其中分5次共加入250克稀硫酸,测得数据记录如下表:
(1)表中m=______g;
(2)黄铜样品中铜的质量分数______;
(3)求所用稀硫酸中溶质的质量分数?(写出计算过程)
8、某同学为定量研究氢氧化钠溶液与稀盐酸反应,做了如下实验:取适量的溶质质量分数为10%的氢氧化钠溶液,加入到50克溶质质量分数为7.3%的稀盐酸中,恰好完全反应。求:(写计算过程)
(1)加入的氢氧化钠溶液的质量。
(2)反应后所得溶液中溶质的质量分数。
9、实验室用34g5%的过氧化氢的水溶液和2g二氧化锰混合制取氧气。完全反应后剩余物质总质量为35.2g。请计算:
(1)参加反应的过氧化氢的质量为___g。
(2)生成氧气的质量是______?(请列式计算)
四、实验探究(每小题5分,共计20分)
1、某化学兴趣小组的同学准备探究影响化学反应速率的因素有哪些,同学们收集资料后发现:
(1)镁条在空气中可以剧烈燃烧,铁丝在氧气中能够剧烈燃烧,金在高温下也不能燃烧,说明影响反应速率的因素之一是______。分析可知,这三种金属活动性由弱到强的顺序是______。铁丝在空气中不能燃烧,在氧气中可以燃烧,说明影响反应速率的因素之二是______。
(2)同学们又利用压强传感器来探究影响铁和稀盐酸反应速率的因素,实验装置和测得的数据如图所示:
①锥形瓶内发生反应的化学方程式为______,基本反应类型为______。
②图中表示铁片与稀盐酸反应的曲线是______(填“a”或“b”),根据曲线得出的结论是______。
③实验测得的反应达到终点时,压强相等。若取少量锥形瓶中剩余溶液加入紫色石蕊溶液,均无明显现象,说明两锥形瓶内的______(填化学式)一定没有剩余。
附加问:
(3)同学们查阅资料发现工业上运输浓硫酸常用铁罐车,于是提岀疑问:铁能与浓硫酸反应吗?请参与实验设计完成相关探究。
(4)①常温下铁能与浓硫酸反应吗?______(填“能”或“不能”)
②运输浓硫酸的铁罐车能否用水冲洗?请回答并分析原因______。
2、碳酸氢钠 (NaHCO3)是一种重要的化工原料。某化学兴趣小组同学对碳酸氢钠的性质进行探究。
(查阅资料)
①碳酸氢钠的溶解度如下:
②碳酸氢钠固体在潮湿的空气中久置或受热分解均生成 Na2CO3、H2O和CO2。
(实验探究)
探究1:NaHCO3溶液与盐酸反应的热效应
室温下(20℃),边搅拌边向盛有0.5 g NaHCO3固体的烧杯中加入10mL水,测得温度为18.5℃;恢复至室温后,向烧杯中加入过量10mL质量分数为20%的盐酸(20℃),搅拌,测得温度为20.8℃。
(1)实验中配制的 NaHCO3溶液___________(填“是”或“不是”)饱和溶液。
(2)由上述实验可知:NaHCO3固体溶于水___________(填“放热”或“吸热”)。有同学认为由上述实验得出 NaHCO3溶液与盐酸反应放热的结论并不可靠,理由是___________。
探究2:NaHCO3溶液与CaCl2溶液的反应。
分别向10mL0.5%和5% NaHCO3溶液中滴加10%的CaCl2溶液,发现均有白色浑浊出现,通过传感器测得CO2浓度与时间的关系如图所示。
(3)由上图得出的实验结论是___________。
(4)该条件下, NaHCO3溶液和CaC12溶液反应的化学方程式为:________ 。
探究3:久置的 NaHCO3样品中 NaHCO3含量的测定:
将一瓶在潮湿空气中久置的 NaHCO3样品(假设只有NaHCO3和Na2CO3)混合均匀后,称取19.0g混合物,加热至恒重,称其质量为15.9g。
(5)①计算样品中 NaHCO3的质量分数(结果精确至0.01%)________。
②若上述测定过程中未加热至恒重,则测得 NaHCO3的质量分数将___________(填“偏大”、“偏小”或“无影响”)。
3、下面是某小组进行的“哪些因素影响固体物质在水中的溶解度”的实验探究,请你完成探究报告。
(探究实验)哪些因素影响固体物质在水中的溶解度?
(1)溶质种类的影响:
在实验中要改变的因素是:溶质的种类;要保持不变的因素是:___________。
(实验步骤)30℃时,用量筒各取5mL蒸馏水分别加入到①、②两支试管中,再分别加入KNO3、Ca(OH)2各2g振荡,观察各物质溶解情况。
(实验现象)试管①中KNO3全部溶解,试管②中有部分Ca(OH)2未溶。
(实验结论)在___________保持不变的情况下,不同种类的物质在水中的溶解度一般___________(选填“相同”或“不同”)。
(2)温度的影响(以KNO3为例):
在实验中要改变的因素是___________;要保持不变的因素是___________。
(实验步骤)用量筒各取5mL蒸馏水,分别加入①、②二支试管中,再加入5gKNO3晶体,将试管①保持在常温下,将试管②加热并保持在60℃,振荡,观察各试管中KNO3的溶解情况。
(实验现象)试管①中有部分KNO3未溶,试管②中KNO3全部溶解。
(实验结论)在不同___________下,同种固体物质在水中的溶解度不同。
4、对比归纳是学习化学的重要方法。请你根据下列实验装置完成有关问题
(1)图1是探究燃烧的条件。由“①处的白磷不燃烧、②处的白磷燃烧”的现象,说明可燃物燃烧需满足的条件是_______________________。
(2)图2是探究铁生锈的条件。一周后试管A中铁钉生锈,试管B、C中铁钉无明显变化。对比试管______(选填字母序号,下同)中的实验现象,说明铁生锈一定要有水参加;对比试管__________中的现象,说明铁生锈必需水和氧气同时参加。
(3)图3是探究影响物质溶解性的因素。对比A试管和B试管,发现B试管中固体可溶, A试管中固体几乎不溶。该对比实验说明了影响物质溶解性的因素是__________________。某同学又补充了C试管所示实验,他想探究的影响因素是__________________。
(4)图4探究常温下镁与铁的金属活动性。分别向盛有等质量镁条与铁粉的两只试管中同时加入等质量等质量分数的稀盐酸,观察试管中金属表面产生气泡的快慢。请你指出其中的不合理之处:______________。
实验设计
实验目的
A.检查装置的气密性
B.验证蜡烛中含有碳元素
C.室温下比较氯化钠在不同溶剂里的溶解性
D.除去二氧化碳中混有的少量一氧化碳
某地海水中主要物质含量
物质
每100g海水所含质量
水
96.5
氯化钠
2.7
硫酸钠
0.2
…
…
温度(℃)
20
100
氯化钠溶解度(g/100g水)
36.0
39.8
硫酸钠溶解度(g/100g水)
20.2
42.5
温度(℃)
10
20
40
60
80
KNO3
20.9
31.6
63.9
110
169
NaCl
35.8
36
36.6
37.3
38.4
反应时间/s
0
10
20
30
40
50
60
溶液温度/℃
20.5
20.6
20.7
20.8
20.9
20.8
20.7
1
第1次
第2次
第3次
第4次
第5次
累计加入稀硫酸的质量/g
50
100
150
200
250
累计产生气体的质量/g
0.2
m
0.6
0.7
0.7
实验步骤
实验现象
①将一打磨过的铁片放入硫酸铜溶液中
______
②另取一打磨过的铁片先放入浓硫酸中,一段时间后将铁片取出,用水冲洗干净后,放入硫酸铜溶液中,观察现象
在硫酸铜溶液中,铁片表面没有明显现象
温度
10℃
20℃
30℃
40℃
溶解度
8.1g
9.6g
11.1g
12.7g
2022年最新人教版九年级化学下册第九单元溶液期末试卷【A4可打印】: 这是一份2022年最新人教版九年级化学下册第九单元溶液期末试卷【A4可打印】,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2022年度最新人教版九年级化学下册第九单元溶液期末试卷(A4可打印): 这是一份2022年度最新人教版九年级化学下册第九单元溶液期末试卷(A4可打印),共11页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
2022学年最新人教版九年级化学下册第九单元溶液期末试卷A4可打印: 这是一份2022学年最新人教版九年级化学下册第九单元溶液期末试卷A4可打印,共13页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。












