






湖南省中考化学复习专题三物质的化学变化第13课时质量守恒定律和化学方程式课件
展开第13课时┃ 质量守恒定律和化学方程式
考点1 质量守恒定律
考点2 化学方程式
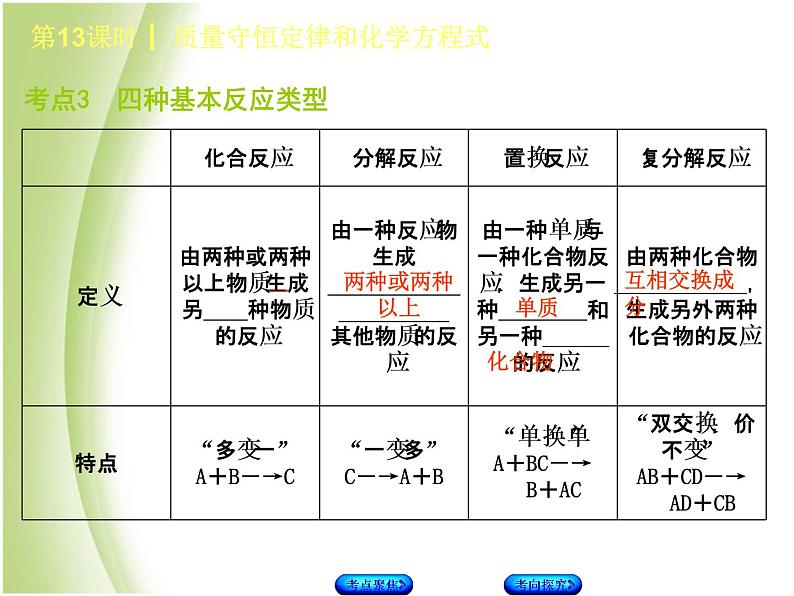
考点3 四种基本反应类型
考点4 有关化学方程式的简单计算
1.依据:____________定律。2.计算步骤设、写、找、列、求、答3.基本类型(1)纯净物之间的化学方程式的计算化学方程式所表示的反应物和生成物都是纯净物,可直接将已知数据代入计算。
(2)不纯物质(杂质不参加反应)的化学方程式的计算遇到含杂质的不纯物质时,需将不纯物质的质量换算成纯净物的质量,才能代入化学方程式按质量比进行计算。计算关系:纯净物的质量=不纯物质的质量×纯净物的质量分数
类型1 质量守恒定律的理解及验证
例1 【2017·淮安】质量守恒定律的发现对化学的发展作出了巨大贡献。
(1)为验证质量守恒定律,小华设计如图13-1甲所示装置进行实验。实验时,先将装有药品的装置放在天平上,添加砝码,移动游码至天平平衡(如图甲所示),然后取下装置,用针筒向锥形瓶中注入少量稀盐酸,反应后再将装置放置于天平上,观察到________,从而验证了质量守恒定律。若将锥形瓶改为烧杯,则不能验证质量守恒定律,原因是________________________。
装置没有密闭,气体逸出
(2)某反应的微观示意图如图乙所示。①X的化学式是________。②根据上述微观示意图,可得出化学反应遵循质量守恒定律的本质原因是____________________________________________________。
化学反应前后,原子的数目和种类不变
[解析] (1)实验时,先将装有药品的装置放在天平上,添加砝码,移动游码至天平平衡,然后取下装置,用针筒向锥形瓶中注入少量稀盐酸,反应后再将装置放置于天平上,由于装置是密封的,因此观察到天平仍平衡,从而验证了质量守恒定律。若将锥形瓶改为烧杯,则不能验证质量守恒定律,原因是装置没有密闭,气体逸出了。(2)①根据质量守恒定律,即化学反应前后各原子的种类和数目不变可知,X的化学式是SO2。②化学反应遵循质量守恒定律的本质原因是化学反应前后,原子的数目和种类不变。
类型2 质量守恒定律的应用
例2 【2017·烟台】清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图13-2(图中的微粒恰好完全反应)。下列说法正确的是( )
A.丁的化学式为H2O,该反应为置换反应 B.参加反应的甲与乙的质量比为3∶1C.甲是单质,乙、丙、丁均为氧化物 D.该反应体现了无机物可以转化为有机物
例3 【2017·兰州】在一密闭容器中,有X、O2、CO2、H2O四种物质,在一定条件下发生某种反应,反应一段时间后,测得反应前后各物质的质量如下表。下列说法正确的是( )
A.表中的待测值为32 B.X中一定含有C、H、O元素C.该反应是置换反应 D.反应中CO2和H2O的质量比为11∶9
[解析] 化学反应前后,原子个数不变,反应物中有1个锰原子,2个氧原子,4个氢原子,4个氯原子,生成物中有2个氯原子,4个氢原子,2个氧原子,所以X是MnCl2。
[解析] 根据质量守恒定律,反应前各物质的质量总和等于反应后生成各物质的质量总和,设生成的D的质量为x,故5.6 g+7.3 g=12.7 g+x,x=0.2 g。
类型3 化学方程式
[解析] 铁在氧气中燃烧生成的是四氧化三铁;烧碱是氢氧化钠,氢氧化钠与硫酸铵反应生成硫酸钠、水和氨气;铝为+3价,硝酸根为-1价,故硝酸铝的化学式为Al(NO3)3;氯化镁和硫酸钾不符合复分解反应发生的条件,不能发生反应。
例7 写出下列反应的化学方程式。(1)用红磷测定空气中氧气含量的原理:________________________________。(2)农业上配制波尔多液:____________________________________________。(3)金属铝耐腐蚀的原因:______________________________________________________。(4)天然气的主要成分在空气中燃烧:____________________。
类型4 化学反应基本类型
[解析] A中是一种单质和一种化合物生成另一种单质和另一种化合物的反应,属于置换反应;B中是两种化合物互相交换成分生成两种新的化合物的反应,属于复分解反应;C中反应符合“一变多”的特征,属于分解反应;D中反应的生成物是两种,不符合“多变一”的特征,不属于化合反应。
[解析] 由图可知,该反应的反应物是一种,而生成物是两种,属于分解反应。
【方法点拨】 解答此类题目的关键是掌握四种基本反应类型的特点。化合反应的特点是“多变一”;分解反应的特点是“一变多”;置换反应的特点是“单换单”;复分解反应的特点是“双交换,价不变”。
中考化学复习物质的化学变化第2节化学反应及质量守恒定律教学课件: 这是一份中考化学复习物质的化学变化第2节化学反应及质量守恒定律教学课件,共58页。PPT课件主要包含了化合物,2其他反应,化学性质,参加化学反应,质量总和,化学变化,生成物,粒子个数,客观事实,质量守恒等内容,欢迎下载使用。
中考化学复习物质的化学变化第2节化学反应及质量守恒定律分层作业课件: 这是一份中考化学复习物质的化学变化第2节化学反应及质量守恒定律分层作业课件,共16页。PPT课件主要包含了分解反应,实验探究等内容,欢迎下载使用。
中考化学复习物质的化学变化主题十二质量守恒定律教学课件: 这是一份中考化学复习物质的化学变化主题十二质量守恒定律教学课件,共26页。PPT课件主要包含了化学反应,质量总和,部受热不均而炸裂,红色固体,浅绿色,烧杯中有气泡产生,化学变化,密闭容器,明显现象,ABCD等内容,欢迎下载使用。












