2022年中考化学一轮复习 强化练 溶解度曲线及应用
展开
这是一份2022年中考化学一轮复习 强化练 溶解度曲线及应用,共8页。
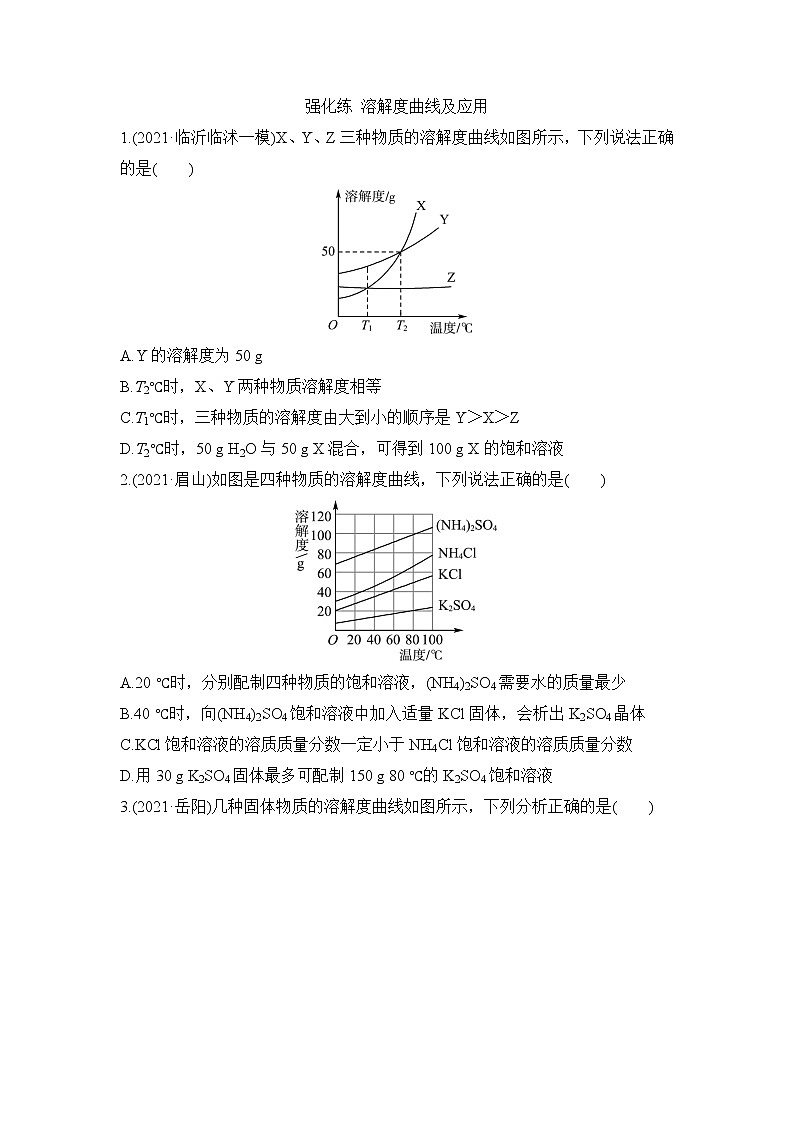
A.Y的溶解度为50 g
B.T2℃时,X、Y两种物质溶解度相等
C.T1℃时,三种物质的溶解度由大到小的顺序是Y>X>Z
D.T2℃时,50 g H2O与50 g X混合,可得到100 g X的饱和溶液
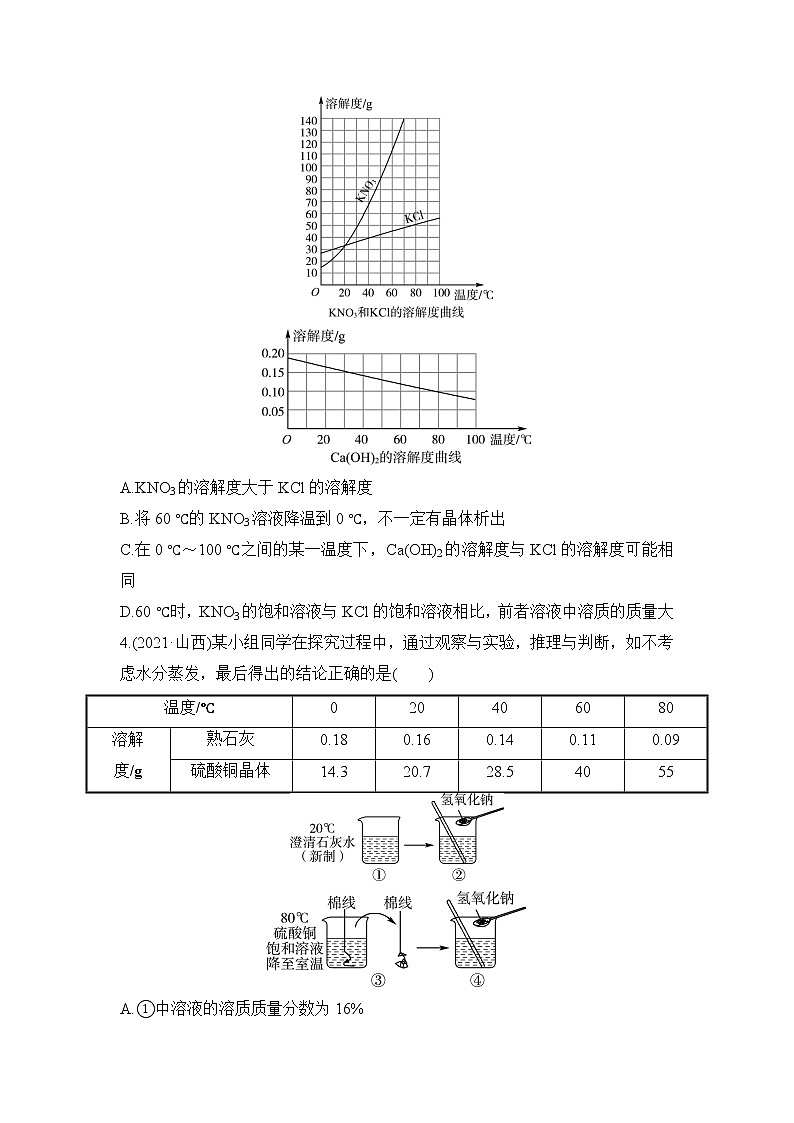
2.(2021·眉山)如图是四种物质的溶解度曲线,下列说法正确的是( )
A.20 ℃时,分别配制四种物质的饱和溶液,(NH4)2SO4需要水的质量最少
B.40 ℃时,向(NH4)2SO4饱和溶液中加入适量KCl固体,会析出K2SO4晶体
C.KCl饱和溶液的溶质质量分数一定小于NH4Cl饱和溶液的溶质质量分数
D.用30 g K2SO4固体最多可配制150 g 80 ℃的K2SO4饱和溶液
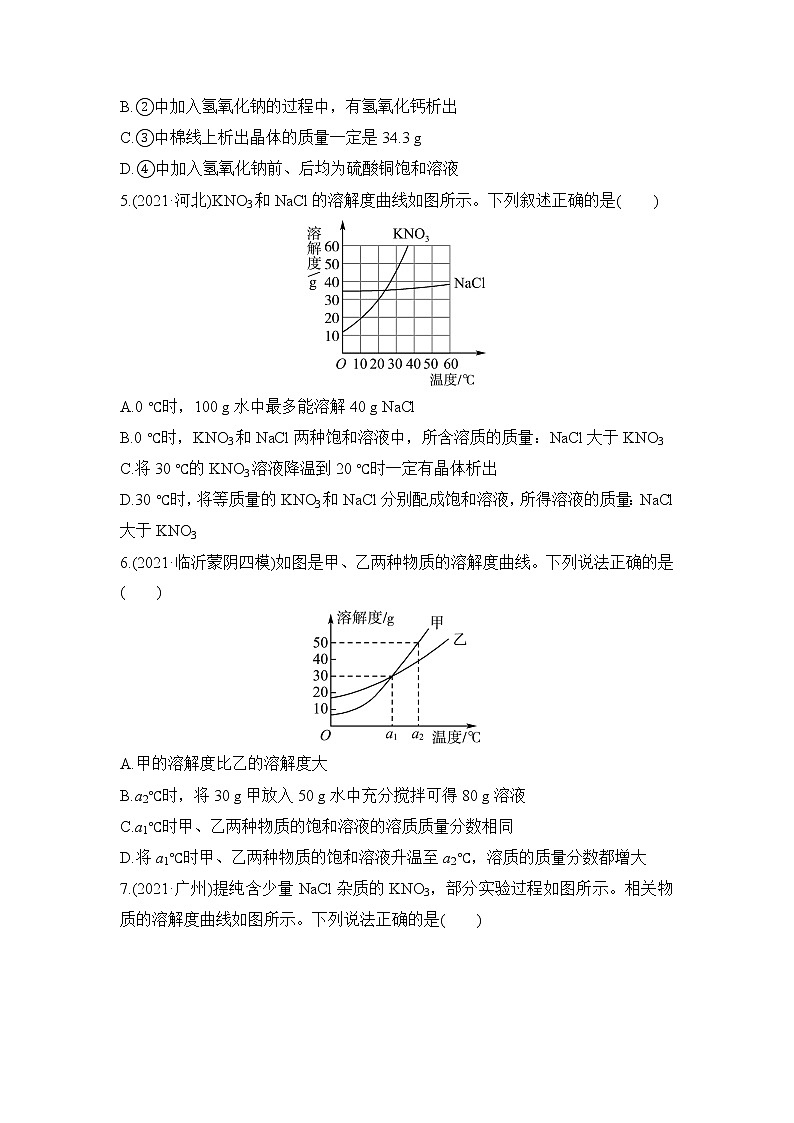
3.(2021·岳阳)几种固体物质的溶解度曲线如图所示,下列分析正确的是( )
A.KNO3的溶解度大于KCl的溶解度
B.将60 ℃的KNO3溶液降温到0 ℃,不一定有晶体析出
C.在0 ℃~100 ℃之间的某一温度下,Ca(OH)2的溶解度与KCl的溶解度可能相同
D.60 ℃时,KNO3的饱和溶液与KCl的饱和溶液相比,前者溶液中溶质的质量大
4.(2021·山西)某小组同学在探究过程中,通过观察与实验,推理与判断,如不考虑水分蒸发,最后得出的结论正确的是( )
A.①中溶液的溶质质量分数为16%
B.②中加入氢氧化钠的过程中,有氢氧化钙析出
C.③中棉线上析出晶体的质量一定是34.3 g
D.④中加入氢氧化钠前、后均为硫酸铜饱和溶液
5.(2021·河北)KNO3和NaCl的溶解度曲线如图所示。下列叙述正确的是( )
A.0 ℃时,100 g水中最多能溶解40 g NaCl
B.0 ℃时,KNO3和NaCl两种饱和溶液中,所含溶质的质量:NaCl大于KNO3
C.将30 ℃的KNO3溶液降温到20 ℃时一定有晶体析出
D.30 ℃时,将等质量的KNO3和NaCl分别配成饱和溶液,所得溶液的质量:NaCl大于KNO3
6.(2021·临沂蒙阴四模)如图是甲、乙两种物质的溶解度曲线。下列说法正确的是( )
A.甲的溶解度比乙的溶解度大
B.a2℃时,将30 g甲放入50 g水中充分搅拌可得80 g溶液
C.a1℃时甲、乙两种物质的饱和溶液的溶质质量分数相同
D.将a1℃时甲、乙两种物质的饱和溶液升温至a2℃,溶质的质量分数都增大
7.(2021·广州)提纯含少量NaCl杂质的KNO3,部分实验过程如图所示。相关物质的溶解度曲线如图所示。下列说法正确的是( )
A.①→②,KNO3的溶解度不变
B.①→②,溶液中KNO3的质量分数不变
C.②→③,溶液中NaCl的质量增大
D.②→③,溶液中KNO3的质量减小
8.(2021·凉山州改编)(单双项)甲、乙、丙三种固体物质的溶解度曲线如图所示,下列相关说法正确的是( )
A.t2 ℃时甲和丙的溶解度都是60
B.t3 ℃时,甲、乙、丙三种物质的饱和溶液中溶质质量分数一定是甲>乙>丙
C.将t3 ℃时甲和丙的饱和溶液降温到t2 ℃,两溶液的溶质质量分数相等
D.将t2 ℃时160 g甲物质的饱和溶液降温到t1 ℃可析出20 g固体(不含结晶水)
9.(2021·兰州改编)(单双项)甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法不正确的是( )
A.P点表示t2 ℃时,甲和乙的溶解度相等
B.t3 ℃时Q点表示甲的不饱和溶液
C.t3 ℃时,将25 g乙放入50 g水中,所得溶液中溶质和溶剂的质量比为2∶5
D.将t3 ℃时甲、乙、丙的饱和溶液降温至出t1 ℃,溶质的质量分数由大到小的顺序为丙>甲>乙
10.(2021·长沙)从物质的溶解度曲线中,可以获得很多信息。甲、乙两种固体物质的溶解度曲线如图所示。
(1)t1℃时,甲、乙两种物质的溶解度________(填“相等”或“不相等”)。
(2)两种物质中,______的溶解度受温度的影响较大。
(3)要使接近饱和的乙溶液变成饱和溶液,可采用的方法有_______________
______________(写一种即可)。
11.(2022·易错题)如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,根据图像回答下列问题。
(1)P点的含义是____________________________________________________。
(2)t2°C时,a、b、c三种物质的溶解度由大到小的顺序是______________。
(3)t1℃时,将25 g a物质加入100 g水中,充分搅拌溶解后恢复到原温度,所得溶液中溶质与溶剂的质量比是__________(最简整数比)。
(4)t2℃时,将a、b、c三种物质的等质量的饱和溶液降温至t1℃,下列说法正确的是________。
A.都是饱和溶液
B.溶质质量分数大小关系是:b>a>c
C.析出晶体质量最多的是a
12.(2021·云南)(1)在1800年,某科学家利用“伏打电池”在常温下对水进行通电分解,当正极产生了10 mL的__________________,负极产生的气体约为__________________mL,再次确认了水的组成。
(2)《茶疏》中对泡茶过程有如下记载:“治壶、投茶、出浴、淋壶、烫杯、酾茶、品茶……”以上过程涉及的操作有溶解、过滤等。在实验室进行过滤操作时玻璃棒的作用是________,过滤时液面高于滤纸边缘会造成的后果是____________。过滤________(填“能”或“不能”)将硬水软化。
(3)如图为A、B、C三种固体物质的溶解度曲线,请据图回答下列问题:
①10 ℃时,A、B、C三种物质中溶解度最大的是______。
②若A中含有少量B时,可用__________________的方法提纯A。
③将等质量的A、B、C饱和溶液由50 ℃降温到20 ℃时,所得溶液中溶质质量由大到小的顺序为______________。
13.(2021·安徽)阅读下列短文,回答问题。
红色经典影片《闪闪的红星》中有一段儿童团员潘冬子给红军送盐的故事。冬子开始把食盐装在竹筒中,打算扮作上山砍柴的人将食盐送给红军。途中发现敌人盘查严格,冬子急中生智跑到河边,把竹筒里的食盐全部溶成盐水,再用棉袄吸收,最终顺利地将食盐送给了红军。
(1)从微观角度分析,氯化钠是由________(填“分子”“原子”或“离子”)构成的;从元素角度分析,氯化钠溶液中+1价的元素有____________(填元素符号)。
(2)从盐水中重新得到食盐固体,需进行操作的名称是____________。
(3)氯化钠的溶解度曲线如下图。假设冬子的竹筒中有358 g氯化钠,10 ℃时最少需用____________g水溶解。
(4)氯化钠在生活中的用途有____________(写出1点即可)。
14.(2021·自贡)某化学兴趣小组通过实验测出了甲、乙、丙三种物质在不同温度下的溶解度,并通过描点法绘制出如下的溶解度曲线图,请根据图示回答问题:
(1)t1 ℃时甲、乙、丙的饱和溶液,升高温度到t2 ℃有固体析出是______。
(2)在温度不变的条件下,将t1 ℃时乙的不饱和溶液转化为饱和溶液,写出一种可采用的方法______________________________。
(3)t2 ℃时甲、乙、丙三种物质的饱和溶液中溶质质量分数最大的是______。
(4)t2 ℃时,将35 g甲物质加入盛有50 g水的烧杯中,充分溶解再降温到t2 ℃后,烧杯中固体质量为______g。
参考答案
1.B 2.B 3.B 4.B 5.D 6.C 7.D 8.BD 9.D
10.(1)相等 (2)甲 (3)增加溶质或恒温蒸发溶剂
11.(1)t1℃时,a、c两物质的溶解度相等,都为20 g
(2)a>b>c (3)1∶5 (4)BC
12.(1)氧气 20 (2)引流 滤液浑浊 不能
(3)C 冷却热饱和溶液 C>B>A
13.(1)离子 Na、H (2)蒸发结晶 (3)1 000
(4)作调味品
14.(1)丙 (2)恒温蒸发溶剂(或增加溶质)
(3)甲 (4)5
温度/℃
0
20
40
60
80
溶解
度/g
熟石灰
0.18
0.16
0.14
0.11
0.09
硫酸铜晶体
14.3
20.7
28.5
40
55
相关试卷
这是一份中考化学一轮复习考点课时练 考点04 溶液及溶解度曲线(含解析),共42页。试卷主要包含了学会配制一定溶质质量分数的溶液,9%=1,下列有关溶液的说法错误的是, B 等内容,欢迎下载使用。
这是一份中考化学一轮复习考点课时练习考点31 溶解度曲线及应用(含解析),共29页。试卷主要包含了溶解度曲线的意义,溶解度曲线的应用,有关溶解度的基本计算,5 500,0%,5 79 84等内容,欢迎下载使用。
这是一份中考化学一轮复习考点过关练习考点31 溶解度曲线及应用(含解析),共29页。试卷主要包含了溶解度曲线的意义,溶解度曲线的应用,有关溶解度的基本计算,5 500,0%,5 79 84等内容,欢迎下载使用。









